Clear Sky Science · es
La deficiencia de esclerostina sensibiliza a los adipocitos blancos a señales termogénicas que inducen el enbeigamiento en ratones
Por qué calentar tu grasa podría enfriar la enfermedad
La mayoría pensamos en el hueso y la grasa corporal como mundos separados: uno nos da estructura y el otro almacena energía. Este estudio en ratones revela que hueso y grasa mantienen una conversación química constante, y que una proteína producida por las células óseas puede decidir si nuestra grasa “blanca” permanece acumulando calorías o se transforma en una grasa más activa y termogénica, la denominada grasa “beige”. Comprender este diálogo oculto podría abrir nuevas vías para abordar la obesidad, la diabetes y la pérdida ósea al mismo tiempo.
Un mensajero silencioso desde el hueso
En el interior de los huesos, células especializadas liberan una pequeña proteína llamada esclerostina al torrente sanguíneo. Los médicos ya apuntan a la esclerostina con fármacos para reforzar el hueso en pacientes con riesgo de fracturas. Estudios previos mostraron que los ratones sin esclerostina no solo tienen huesos muy fuertes, sino que además son más delgados y presentan mayor sensibilidad a la insulina. Su grasa subcutánea, especialmente alrededor de las caderas (grasa blanca inguinal), contiene pequeñas células grasas con múltiples compartimentos que recuerdan a la grasa beige, capaz de quemar combustible para generar calor. Estas pistas llevaron a los investigadores a preguntarse si la esclerostina actúa normalmente como un freno sobre la capacidad del organismo para convertir grasa blanca en beige cuando se expone al frío o a fármacos que imitan las señales nerviosas hacia la grasa.
Señales de frío, señales óseas y el encendido de la grasa
El equipo expuso a ratones normales y a ratones carentes del gen de la esclerostina (Sost-/-) a un fármaco que activa un receptor específico en las células grasas (receptor β3-adrenérgico), o a frío leve. En animales normales, estas señales termogénicas aumentaron la producción de esclerostina en el hueso y elevaron su nivel en sangre. Este aumento se asoció a una pérdida de hueso esponjoso pero solo a cambios modestos en la grasa subcutánea. En contraste, los ratones deficientes en esclerostina mostraron una respuesta mucho más intensa: su grasa inguinal captó más glucosa, liberó más ácidos grasos, se redujo de tamaño y se llenó de células tipo beige repletas de mitocondrias, las centrales energéticas celulares. Genes termogénicos clave se activaron con mayor fuerza en estos ratones, especialmente en la grasa subcutánea, mientras que la grasa parda clásica permaneció en gran medida sin cambios.
Afinando la quema de grasa mediante un interruptor compartido
Para entender cómo ejerce la esclerostina este control, los investigadores se centraron en la β-catenina, una proteína implicada en la vía de señalización Wnt que la esclerostina normalmente suprime en el hueso. En la grasa, activar la β-catenina después del nacimiento empujó a las células blancas hacia un estado tipo beige y aumentó su respuesta a las señales β3-adrenérgicas, pero este efecto desapareció cuando los ratones se mantuvieron en una temperatura cálida, termoneutra, donde el organismo ya no necesita calor extra. Por el contrario, eliminar la β-catenina específicamente en las células grasas de ratones deficientes en esclerostina borró su grasa beige, restauró células grasas blancas más grandes y revirtió las mejoras en insulina y niveles de ácidos grasos. Estos experimentos sugieren que, cuando la esclerostina es baja, la β-catenina en las células grasas se convierte en una palanca interna importante que hace que la grasa blanca sea más sensible a las señales termogénicas.
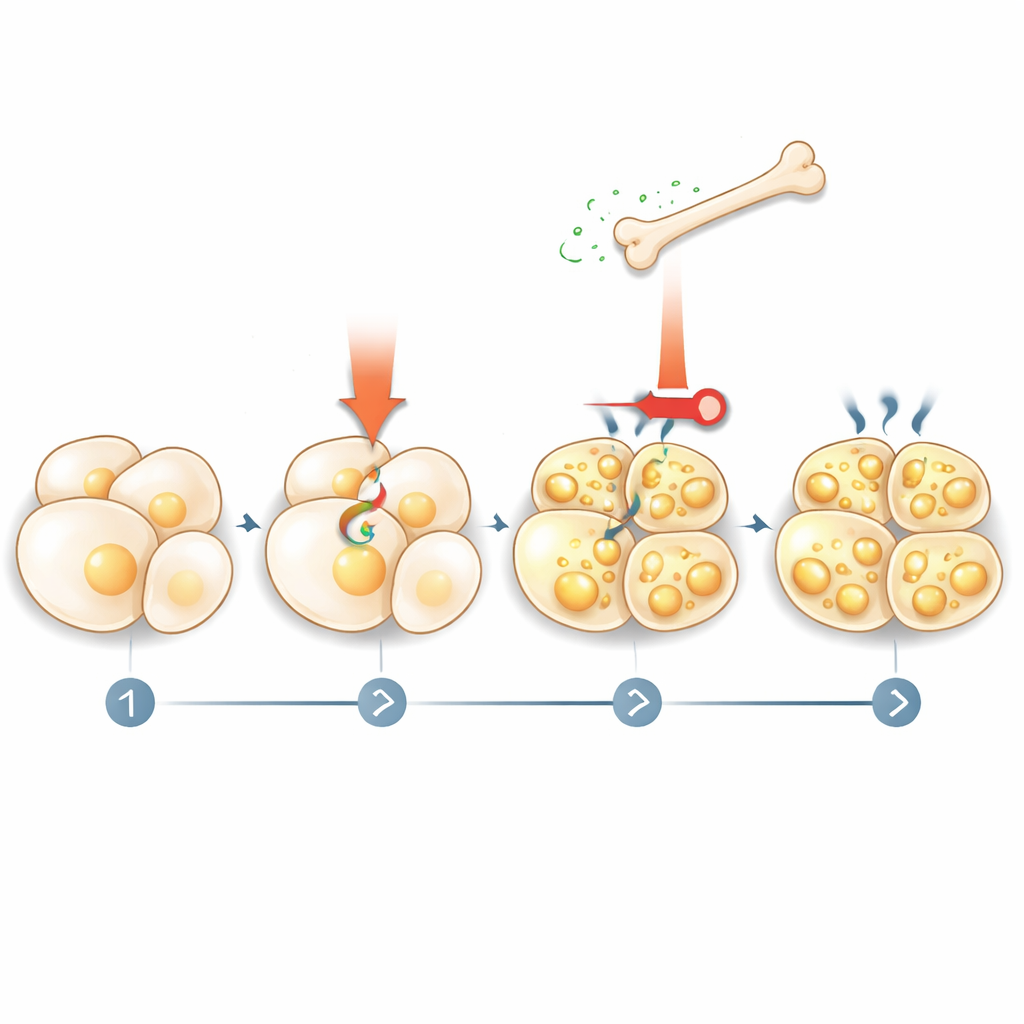
Cómo la grasa responde al hueso
La historia no terminó con el hueso diciéndole a la grasa qué hacer. El equipo encontró que la estimulación termogénica activa la descomposición de la grasa (lipólisis), liberando ácidos grasos a la sangre. Estos ácidos grasos, a su vez, actúan sobre las células óseas mediante un receptor nuclear llamado PPARγ, aumentando la producción de esclerostina. Cuando los investigadores bloquearon la lipólisis en las células grasas o eliminaron PPARγ de las células óseas, los fármacos que imitan el frío ya no pudieron elevar los niveles de esclerostina. Esto revela un circuito de retroalimentación: las señales termogénicas hacen que la grasa libere combustible, ese combustible instruye al hueso para que secreta más esclerostina, y la esclerostina vuelve para frenar más activación y enbeigamiento de la grasa.
Combinar fármacos para hueso y grasa para la salud metabólica
Finalmente, los investigadores probaron si interrumpir este circuito podría ser útil en un contexto similar a la enfermedad. Ratones obesos con dieta alta en grasas recibieron una dosis baja de mirabegrón (un fármaco β3-adrenérgico ya usado para problemas de vejiga), un anticuerpo que neutraliza la esclerostina (romosozumab, aprobado para la osteoporosis), o ambos. Mientras que cada fármaco por sí solo tuvo efectos modestos, la combinación redujo la masa grasa en depósitos clave, desplazó la grasa hacia células más pequeñas y activas, redujo insulina, triglicéridos y colesterol, y preservó la resistencia ósea. El alojamiento en ambiente cálido, que reduce la necesidad de calor del organismo, borró en gran medida los beneficios metabólicos de la pérdida de esclerostina, subrayando que esta vía importa especialmente cuando hay señales termogénicas presentes.
Qué significa esto para tratamientos futuros
En términos sencillos, este trabajo muestra que el hueso no es solo un armazón pasivo, sino un regulador activo de cuánto combustible queman las células grasas. La esclerostina funciona como una perilla que mantiene la actividad de la grasa termogénica, y por tanto el uso de combustible, bajo control. Girar esa perilla hacia abajo —mediante genética o fármacos— hace que ciertos depósitos de grasa blanca estén más predispuestos a cambiar a un modo productor de calor cuando el cuerpo recibe un empujón por el frío o por fármacos específicos. Dado que la misma intervención puede fortalecer el hueso y mejorar la salud metabólica en ratones, combinaciones cuidadosamente diseñadas de terapias dirigidas al hueso y a la grasa podrían algún día ayudar a tratar la obesidad, la diabetes y la osteoporosis de forma conjunta, en lugar de una enfermedad a la vez.
Cita: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
Palabras clave: esclerostina, grasa beige, comunicación hueso–grasa, termogénesis, enfermedad metabólica