Clear Sky Science · es
La síntesis local de PI(4,5)P2 por isoformas de PIPKIγ asociadas a septinas controla la asociación del centralspindlin con el cuerpo medio durante la citocinesis
Cómo las células completan la separación en dos
La citocinesis—el último apretón que divide una célula en dos—es fácil de dar por sentada, pero cuando falla puede contribuir al desarrollo del cáncer y otras enfermedades. Este estudio revela cómo un conjunto específico de moléculas actúa como capataces de obra en el estrecho puente que conecta dos células recién formadas, asegurando que la separación termine de forma limpia en lugar de retroceder o atascarse.
El puente final entre las células hijas
Tras duplicar su material genético y separar los cromosomas, la célula debe dividirse físicamente. Un anillo contráctil de filamentos proteicos se estrecha alrededor del ecuador celular, creando una hendidura profunda llamada surco de segmentación. A medida que este surco se contrae, las dos células hijas permanecen unidas por un delgado puente intercelular que contiene un núcleo denso, el cuerpo medio. El cuerpo medio es una estructura pequeña pero compleja formada por microtúbulos agrupados, proteínas andamio y lípidos señalizadores; actúa tanto de anclaje como de centro de control que coordina los pasos finales de la división y el corte definitivo entre las células. 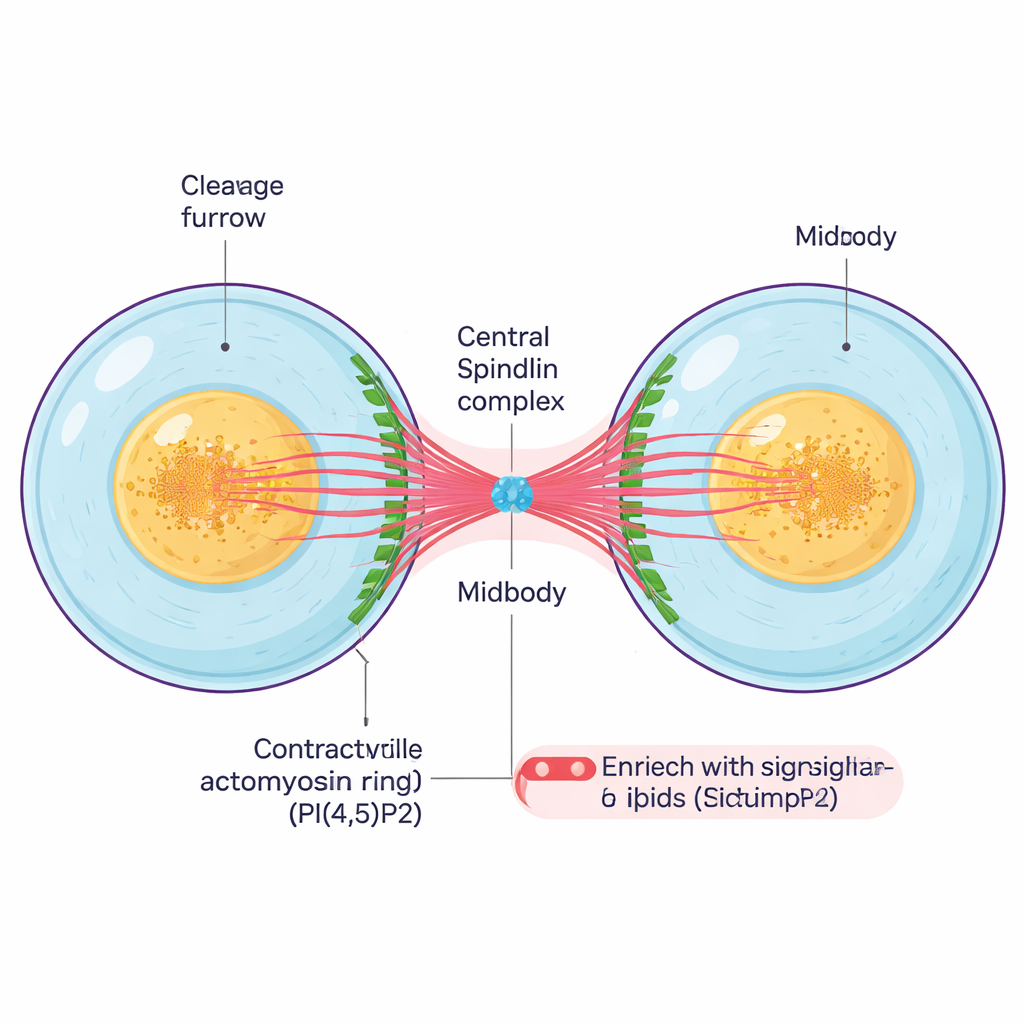
Una señal lipídica que debe estar en el lugar correcto
Un actor clave en este proceso es una molécula grasa señalizadora en la membrana celular llamada PI(4,5)P2. Este lípido ayuda a anclar muchas proteínas que construyen y contraen el anillo contráctil y estabilizan el puente. El enigma ha sido cómo las células controlan dónde y cuándo aparece PI(4,5)P2, dado que puede difundirse en la membrana. Los autores se centraron en enzimas llamadas quinasas PIP de tipo I, que sintetizan PI(4,5)P2, y en particular en un gen, PIPKIγ, que existe en varias formas de empalme ligeramente diferentes. Al reducir selectivamente cada quinasa en células humanas y observar los efectos con microscopía avanzada, encontraron que PIPKIγ tiene un papel especial en las etapas tardías de la citocinesis, cuando se forman el puente y el cuerpo medio, aunque no modifica de forma notable los niveles globales de PI(4,5)P2 en la superficie celular.
Andamios de septinas reclutan una enzima especializada
El equipo descubrió que dos variantes por empalme de PIPKIγ, llamadas i3 e i5, actúan como herramientas de precisión que son llevadas al sitio adecuado por proteínas estructurales conocidas como septinas. Las septinas forman filamentos y anillos que ayudan a dar forma al puente y a organizar otros componentes. Ensayos bioquímicos de captura y microscopía celular mostraron que PIPKIγ-i3 y PIPKIγ-i5 se unen físicamente a complejos de septinas y decoran los filamentos de septina, mientras que otras variantes de PIPKIγ no lo hacen. Cuando los investigadores mutaron dos aminoácidos específicos en estos insertos de empalme, las enzimas ya no podían unirse a las septinas. En células en división, las PIPKIγ-i3/i5 normales pasan de un patrón membranoso difuso a concentrarse en el surco de segmentación y luego delinear el puente intercelular y el cuerpo medio sincronizándose con las septinas y otra proteína andamio, la anillina. Eliminar únicamente las variantes i3 e i5 dispersó la anillina y las septinas lejos del cuerpo medio a lo largo del puente, y muchas células fracasaron en la citocinesis, acabando con múltiples núcleos.
La producción lipídica local fija la maquinaria de división
Para comprobar si estos efectos dependían de la producción local de PI(4,5)P2, los autores midieron PI(4,5)P2 alrededor del cuerpo medio y manipularon enzimas que añaden o eliminan este lípido. La depleción de PIPKIγ-i3/i5 redujo PI(4,5)P2 en el cuerpo medio, mientras que bloquear una enzima degradadora de PI(4,5)P2 tuvo el efecto contrario. De forma importante, restaurar una forma de empalme de PIPKIγ catalíticamente activa y capaz de unirse a las septinas rescató el correcto agrupamiento de la anillina y las septinas en el puente, pero las mutantes sin actividad quinasa o deficientes en unión a septinas no lo hicieron. Usando imagen en vivo y una técnica de microscopía de expansión que infla físicamente la muestra para revelar detalles finos, el equipo mostró que sin PIPKIγ-i3/i5 las septinas ya no se trasladan a los microtúbulos del puente, el puente se vuelve más corto y menos agrupado, y un complejo crucial llamado centralspindlin deja de permanecer fuertemente asociado al cuerpo medio. 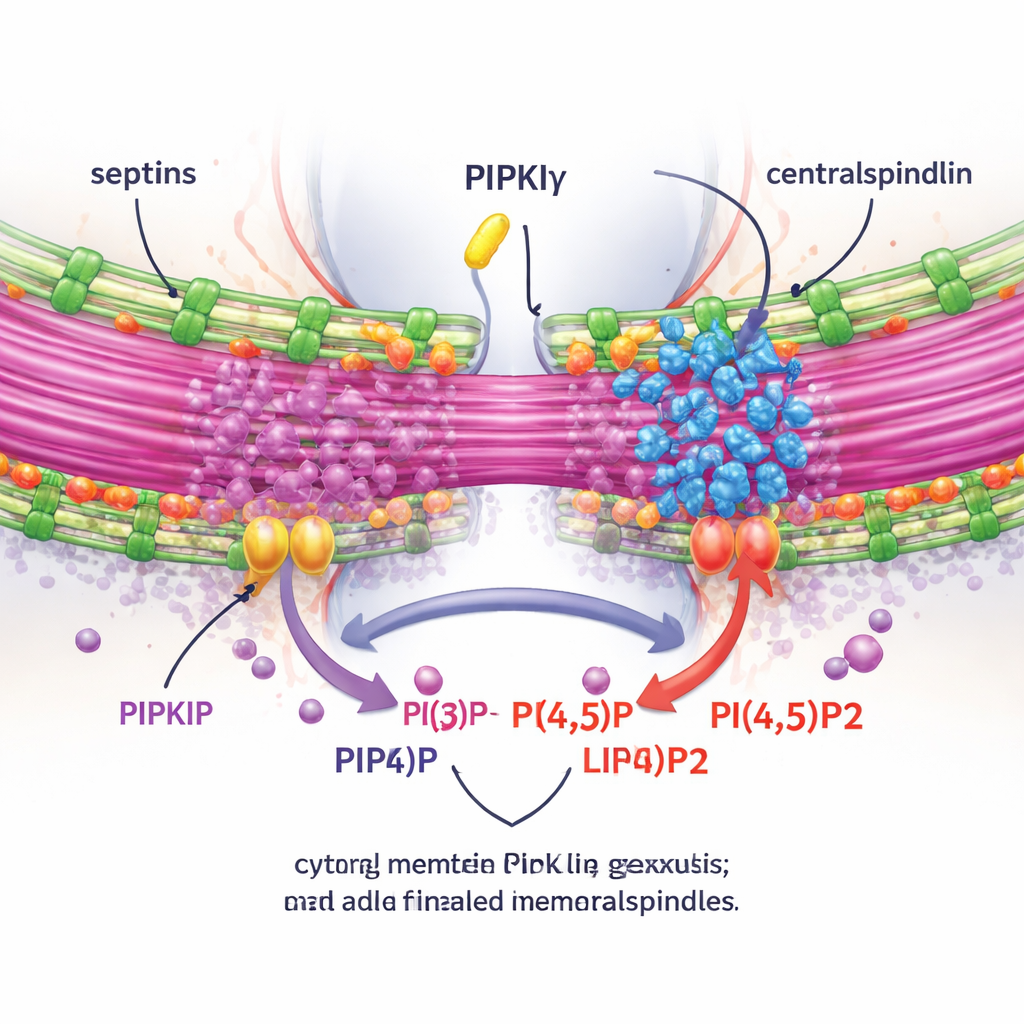
Construir un punto de control para un corte limpio
Centralspindlin ayuda a unir los microtúbulos del cuerpo medio a la membrana circundante y regula interruptores moleculares pequeños que controlan la forma celular. El estudio encuentra que centralspindlin se asocia tanto con septinas como con PIPKIγ, y que perder cualquiera de los dos socios debilita de forma similar su presencia en el cuerpo medio. Los autores proponen que las septinas reclutan PIPKIγ-i3/i5 al surco ingresado, donde estas quinasas crean un parche concentrado de PI(4,5)P2. Esta reserva lipídica local, a su vez, estabiliza la anillina, el centralspindlin y las septinas cerca del cuerpo medio, promueve el agrupamiento y la estabilización de los microtúbulos del puente, y permite que el puente intercelular madure hasta que se produzca el corte final de abscisión. Si este sistema se perturba, PI(4,5)P2 aparece en lugares inadecuados, las proteínas andamio se dispersan, los microtúbulos quedan pobremente agrupados y la citocinesis con frecuencia falla.
Por qué esto importa más allá de la biología celular básica
Al precisar cómo variantes específicas por empalme de PIPKIγ y las septinas cooperan para generar una señal lipídica local en el cuerpo medio, este trabajo explica cómo las células dan precisión espacial a una molécula señalizadora muy móvil. Esa precisión es crucial para la finalización segura de la división celular, ayudando a prevenir la mala segregación de cromosomas y el número anómalo de células que pueden favorecer el desarrollo tumoral. Las mismas estructuras del cuerpo medio también influyen en el destino y la proliferación celular tras la división, por lo que comprender cómo se ensamblan abre nuevas vías para explorar cómo los errores en estos andamios a escala nanométrica podrían contribuir al cáncer y, posiblemente, para manipular células madre.
Cita: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
Palabras clave: división celular, citocinesis, lípidos señalizadores, septinas, biología del cáncer