Clear Sky Science · es
El inhibidor pan‑RAF exarafenib apunta a BRAF clase II/III en NSCLC y revela resistencia ARAF‑KSR1 y estrategias de combinación
Por qué esta investigación importa para pacientes con cáncer de pulmón
La mayoría conoce los fármacos dirigidos que atacan alteraciones genéticas concretas. Pero para muchos pacientes con cáncer de pulmón, en particular aquellos cuyos tumores portan mutaciones menos comunes en un gen llamado BRAF, los tratamientos dirigidos disponibles hoy no funcionan. Este estudio presenta un nuevo fármaco experimental, exarafenib, diseñado para actuar sobre un conjunto más amplio de tumores impulsados por BRAF y explica cómo las células cancerosas intentan escapar de él, revelando combinaciones terapéuticas que podrían mantener estos tumores controlados por más tiempo.
Una mayoría oculta de mutaciones pasadas por alto
Los investigadores comenzaron preguntando algo básico: ¿con qué frecuencia aparecen los distintos tipos de mutaciones de BRAF en cánceres avanzados y, en particular, en el carcinoma de pulmón no microcítico (NSCLC)? Usando una gran base de datos de biopsias líquidas con más de 160.000 pacientes, analizaron fragmentos de ADN tumoral que circulan en la sangre. Encontraron que en cáncer de pulmón las mutaciones de BRAF se dan en torno al 4–5% de los pacientes, lo que sigue representando varios miles de personas en todo el mundo. De forma crucial, alrededor de dos tercios de estos tumores pulmonares presentaban las llamadas mutaciones de BRAF de Clase II y Clase III: tipos que los fármacos BRAF aprobados actualmente no atacan de forma eficaz. Los pacientes con una de estas clases, especialmente Clase II, tendían a tener una supervivencia menor que quienes tenían la más familiar mutación de Clase I, probablemente porque los pacientes con Clase I disponen de terapias dirigidas establecidas mientras que los de Clase II/III reciben mayormente quimioterapia estándar o inmunoterapia.
Un fármaco de próxima generación que apunta a toda la vía
BRAF forma parte de un relevo de proteínas (la vía MAPK) que transmite señales de crecimiento desde la superficie celular hasta el núcleo. Muchos fármacos BRAF existentes fueron diseñados para bloquear solo una forma mutante y pueden incluso estimular involuntariamente proteínas relacionadas en células normales. Exarafenib se diseñó de forma distinta: es un inhibidor “pan‑RAF” pensado para bloquear varios miembros de la familia RAF (ARAF, BRAF y CRAF) en formas individuales y emparejadas, mientras que respeta a la mayoría de las demás enzimas celulares. En pruebas bioquímicas frente a cientos de quinasas humanas, exarafenib inhibió con fuerza las tres proteínas RAF y mostró pocos efectos fuera de diana, lo que sugiere un perfil de seguridad más limpio que compuestos pan‑RAF anteriores.
Efectos potentes en modelos de tumores difíciles de tratar
El equipo probó exarafenib en una batería de líneas celulares y modelos murinos que portan distintas mutaciones en BRAF y RAS, incluidos tumores derivados de pacientes en condiciones realistas. En cultivos celulares, exarafenib frenó el crecimiento y apagó la señalización MAPK no solo en células clásicas con BRAF V600E sino también en las que tenían mutaciones de Clase II y Clase III y en muchas células con mutación en RAS que actualmente carecen de buenas opciones dirigidas. En ratones con tumores pulmonares que presentaban estas alteraciones, exarafenib redujo o ralentizó los tumores de forma dependiente de la dosis y mostró relaciones claras entre los niveles del fármaco, la supresión de la vía y la respuesta tumoral. Datos clínicos tempranos de dos pacientes con cáncer de pulmón avanzado con mutación en BRAF —uno con una fusión BRAF rara y otro con una mutación puntual de Clase II— mostraron respuestas parciales y alivio sintomático significativo, apoyando la relevancia del trabajo preclínico.
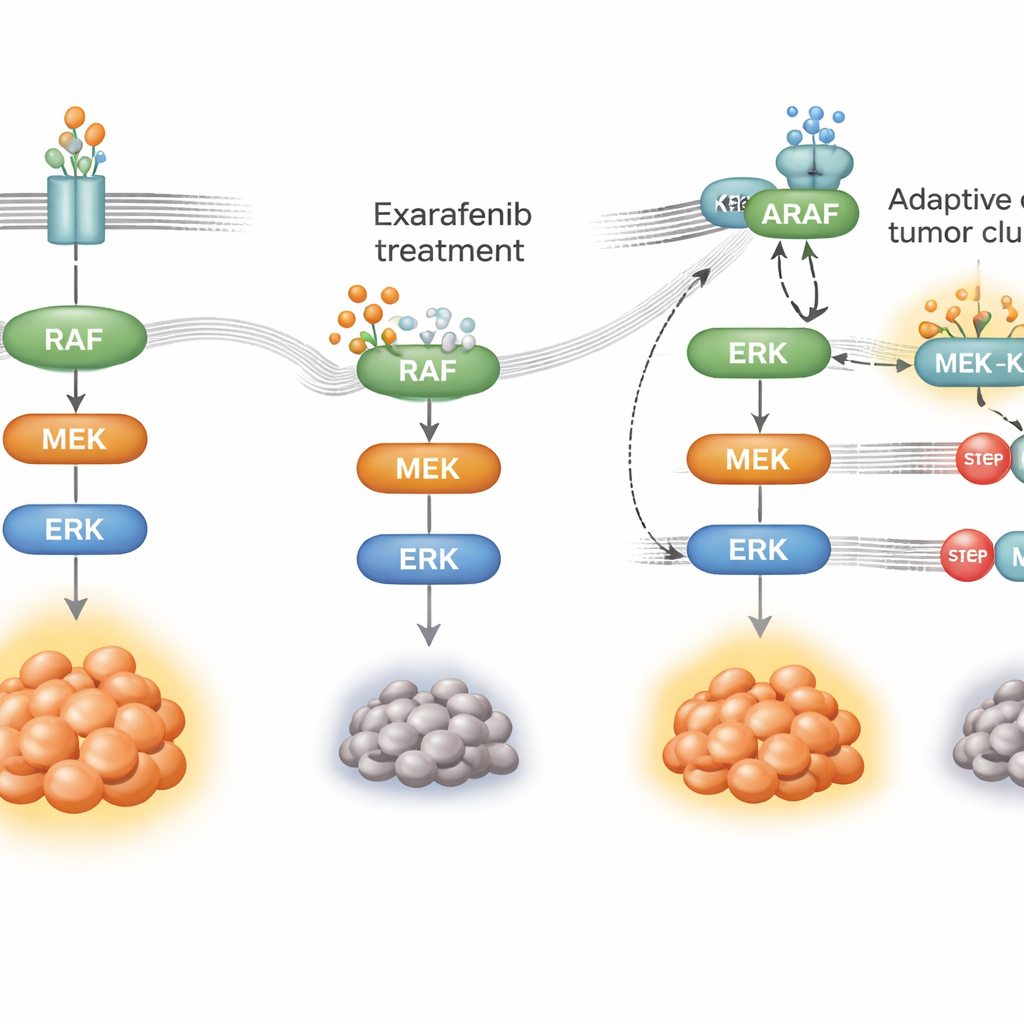
Cómo el cáncer aprende a eludir el fármaco
Ninguna terapia dirigida funciona para siempre; las células cancerosas se adaptan. Para ver cómo los tumores podrían desarrollar resistencia a exarafenib, los investigadores expusieron células de cáncer de pulmón con mutación BRAF al fármaco durante meses hasta que surgieron poblaciones resistentes. Estas células seguían dependiendo de la misma vía de crecimiento pero habían reconfigurado su uso de la misma. En lugar de depender principalmente del BRAF mutante, aumentaron la actividad de un interruptor aguas arriba llamado RAS y derivaron hacia el uso de otro miembro de la familia, ARAF, junto con una proteína andamiaje denominada KSR1. Bajo la presión del fármaco, ARAF y KSR1 formaron complejos estrechos que ayudaban a mantener la transmisión MAPK incluso con exarafenib presente. Cuando los científicos silencieron selectivamente ARAF o KSR1, o redujeron la actividad de RAS, las células resistentes volvieron a ser sensibles a exarafenib y las señales de supervivencia colapsaron.
Estrategias de combinación para adelantarse a la resistencia
Armados con este mapa mecanístico, el equipo buscó fármacos asociados que pudieran bloquear la vía en puntos de estrangulamiento compartidos por la ruta original y las vías de escape. Encontraron que combinar exarafenib con fármacos que inhiben MEK o ERK —pasos clave aguas abajo en el relevo MAPK— produjo una fuerte sinergia en numerosos modelos celulares y murinos, incluidos tumores que eran intrínsecamente menos sensibles o que habían adquirido resistencia. Estas combinaciones mantuvieron la vía cerrada por más tiempo, desencadenaron más muerte celular y en animales a menudo funcionaron tan bien o mejor que dosis más altas de exarafenib solo, sin toxicidad añadida evidente. Agentes que atacan directamente a RAS también potenciaron los efectos de exarafenib en modelos donde RAS impulsaba claramente la resistencia, lo que sugiere otra táctica clínicamente prometedora.
Qué significa esto para los pacientes
Para las personas con NSCLC que portan mutaciones de BRAF Clase II o Clase III —o fusiones complejas de BRAF y co‑mutaciones en RAS— actualmente no existen terapias dirigidas aprobadas y los resultados son inferiores a los de pacientes con alteraciones más comunes. Este estudio aporta un argumento científico sólido de que exarafenib podría ayudar a cubrir esa laguna al bloquear de forma amplia la señalización impulsada por RAF. También explica cómo los tumores pueden adaptarse mediante un bypass ARAF‑KSR1 y muestra que atacar la vía en múltiples niveles, en especial combinando inhibidores de RAF y MEK o añadiendo inhibidores de RAS, podría ofrecer un control tumoral más profundo y duradero. En conjunto, estos hallazgos trazan un camino hacia ensayos clínicos destinados a llevar terapias dirigidas combinadas y personalizadas a un grupo amplio y hasta ahora poco atendido de pacientes con cáncer de pulmón.
Cita: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
Palabras clave: cáncer de pulmón con mutación BRAF, inhibidor pan‑RAF, señalización MAPK, resistencia a fármacos, combinaciones de terapias dirigidas