Clear Sky Science · es
Ingeniería de una enzima citocromo P450 como peroxigenasa para la hidroxilación selectiva de esteroides
Fabricar medicamentos a partir de moléculas difíciles de ajustar
Los fármacos esteroides —desde pastillas antiinflamatorias hasta terapias hormonales— están entre los medicamentos más utilizados en el mundo. Sin embargo, afinar estos compuestos, añadiendo un solo átomo de oxígeno en el lugar exacto, es notoriamente difícil con la química tradicional. Este estudio muestra cómo los científicos rediseñaron una enzima natural para que pueda “pulir” con precisión moléculas esteroides usando peróxido de hidrógeno simple, lo que podría permitir vías más ecológicas y baratas para obtener medicamentos importantes.
Por qué es tan difícil personalizar esteroides
Los esteroides están formados por una apilamiento compacto de anillos de carbono, con muchos enlaces carbono–hidrógeno casi idénticos. Los métodos químicos convencionales tienen dificultades para atacar solo uno de estos enlaces sin afectar a otros, y a menudo requieren reactivos agresivos, altas temperaturas y múltiples pasos de protección que generan residuos. Sin embargo, cambios pequeños —como añadir un único grupo hidroxilo (–OH) en una posición específica— pueden alterar drásticamente el comportamiento de un esteroide en el organismo. Las enzimas de la familia citocromo P450 son las especialistas naturales en este tipo de activación precisa de enlaces C–H, pero en su forma nativa suelen necesitar cofactores caros y maquinaria para manejar el oxígeno, lo que limita su uso directo en la fabricación.
Descubriendo una enzima prometedora como punto de partida
Mediante minería genómica, los investigadores identificaron una enzima P450 autosuficiente, llamada P450stri, proveniente de una bacteria del suelo. A diferencia de la clásica enzima de uso habitual P450BM3, que prefiere ácidos grasos pequeños, P450stri acepta de forma natural moléculas esteroides voluminosas como la testosterona. En sus condiciones nativas, impulsada por el cofactor celular NADH, P450stri añade grupos hidroxilo en tres posiciones de la testosterona, produciendo una mezcla de productos. Esta capacidad intrínseca para reconocer esteroides convirtió a P450stri en un “andamio” atractivo para la ingeniería de un catalizador más selectivo y compatible con la industria.
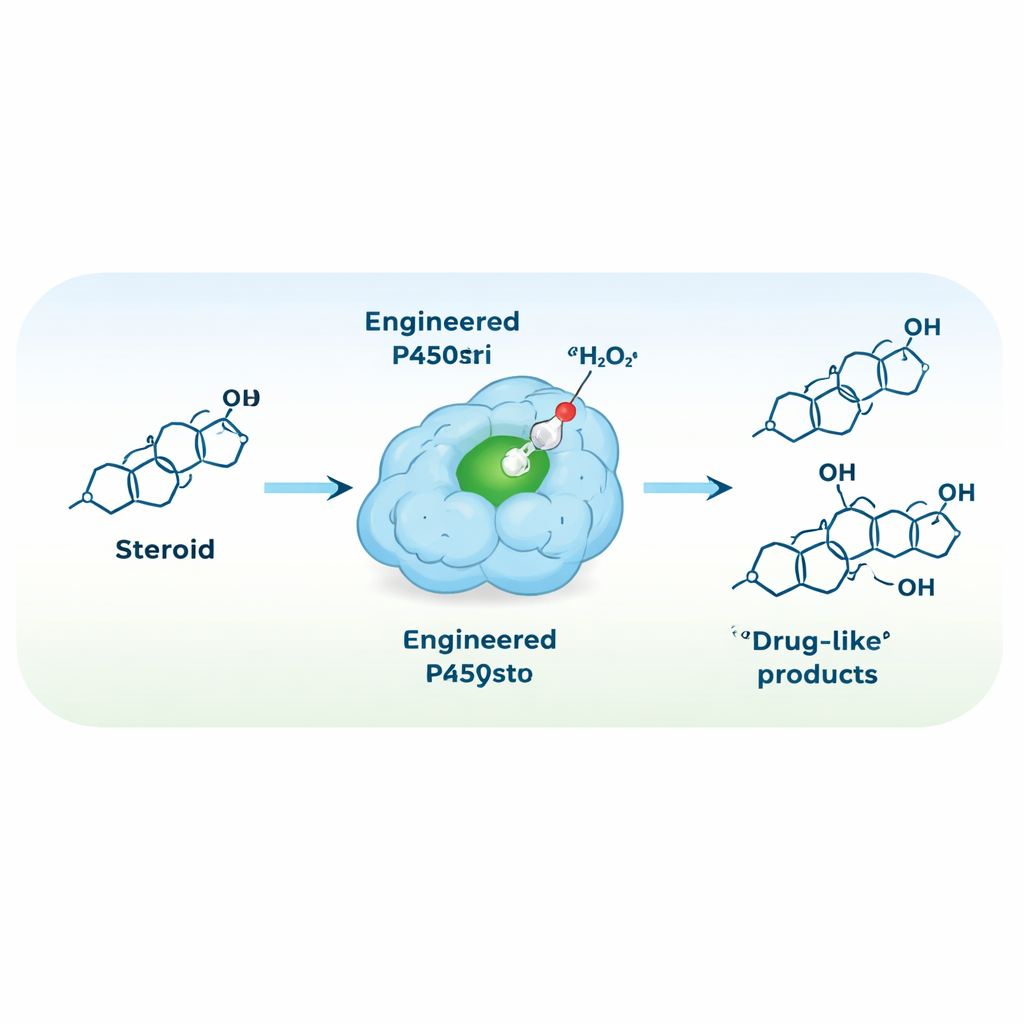
Reconfigurar la enzima para que funcione con peróxido de hidrógeno
Para simplificar el montaje de la reacción, el equipo se propuso convertir P450stri en una peroxigenasa —una enzima que usa peróxido de hidrógeno directamente como oxidante— eliminando la necesidad de cofactores costosos y proteínas auxiliares. Una única mutación estratégica, reemplazando una fenilalanina voluminosa situada justo encima del centro hemo por una alanina más pequeña, creó una variante llamada M1. Este cambio abrió espacio alrededor del centro de hierro reactivo y, sorprendentemente, hizo que la enzima fuera tanto más tolerante a concentraciones altas de peróxido de hidrógeno como mucho más selectiva. En el nuevo modo impulsado por peróxido, M1 convirtió la testosterona principalmente en un solo producto hidroxilado en la posición 15β, con aproximadamente un 94% de selectividad —frente al 35% de la enzima original.
Un modelo de “matraz redondo” para diseñar enzimas con más inteligencia
Para mejorar todavía más el rendimiento, los autores introdujeron un concepto de diseño que llaman el modelo del “Matraz Redondo”. Tratan al sitio activo donde ocurre la química como la base redondeada y a los túneles de acceso estrechos como el cuello y la tapa. La base determina qué posición del esteroide se modifica, mientras que el cuello controla con qué facilidad el esteroide y el peróxido de hidrógeno alcanzan el centro reactivo. Guiados por simulaciones por ordenador y programas de mapeo de túneles, ajustaron de forma sistemática un pequeño conjunto de aminoácidos que recubren esos túneles, afinando su tamaño e hidrofobicidad. Esta estrategia bidimensional dio como resultado una variante destacada, M4, que mantuvo una alta selectividad 15β al tiempo que aumentó considerablemente la velocidad de reacción y toleró concentraciones de peróxido de hidrógeno de hasta varios cientos de milimolares.
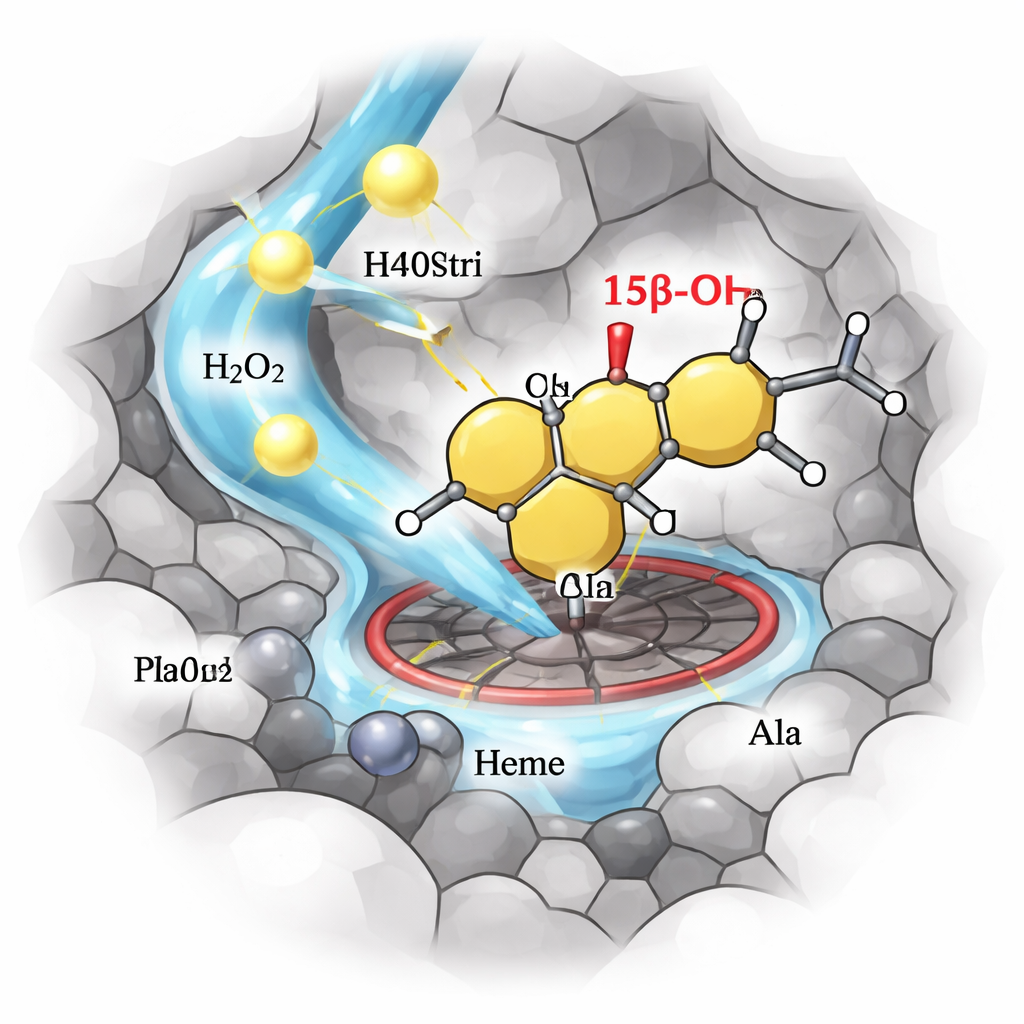
Del banco de laboratorio a mejoras de esteroides escalables
La enzima diseñada M4 se probó posteriormente en reacciones a mayor escala con testosterona y un esteroide relacionado usado en contextos de mejora del rendimiento. En mezclas acuosas simples a temperatura ambiente, impulsada solo por peróxido de hidrógeno, M4 convirtió más del 90% de la materia prima y entregó productos 15β-hidroxilados aislados con rendimientos alrededor del 75–80%. Estas condiciones son mucho más suaves y limpias que las rutas químicas típicas. Finalmente, el equipo mostró que al trasplantar las mutaciones clave a varias enzimas P450 relacionadas en la misma rama evolutiva, podían convertirlas de forma fiable en peroxigenasas igualmente selectivas y eficientes, resaltando la generalidad de sus reglas de diseño.
Qué significa esto para los medicamentos del futuro
Para un público no especializado, la conclusión es que los investigadores han enseñado a una enzima natural a comportarse como una “microfábrica” muy precisa, impulsada por peróxido, para modificar fármacos esteroides. Al combinar un modelo conceptual sencillo con mutaciones dirigidas, crearon una enzima que puede añadir un grupo OH en el lugar justo, en condiciones suaves y escalables, y luego transfirieron esta estrategia a proteínas relacionadas. Este enfoque podría simplificar la producción de esteroides existentes, abrir vías hacia nuevos candidatos a fármacos y servir como plano para diseñar otras enzimas que activen de forma limpia enlaces C–H resistentes en moléculas complejas.
Cita: Tang, T., Wang, R. & Chen, Y. Engineering a cytochrome P450 enzyme as a peroxygenase for selective hydroxylation of steroids. Nat Commun 17, 1996 (2026). https://doi.org/10.1038/s41467-026-69211-8
Palabras clave: biocatálisis de esteroides, ingeniería de citocromo P450, peroxigenasa, catálisis con peróxido de hidrógeno, hidroxilación selectiva