Clear Sky Science · es
Acoplamiento en cadena secuencial sobre sitios click jerárquicos permite una electrosíntesis de urea altamente selectiva
Convertir residuos en alimento para las plantas
El fertilizante ureico alimenta cultivos en todo el mundo, pero fabricarlo de la manera tradicional consume enormes cantidades de combustibles fósiles y libera ingentes cantidades de dióxido de carbono. Este estudio explora una vía distinta: usar electricidad —preferentemente de fuentes renovables— para enlazar carbono y nitrógeno procedentes de gases residuales y aguas contaminadas en nuevas moléculas de urea. Tomando ideas de la “química click”, los autores diseñan un catalizador inteligente que ensambla estos ingredientes de forma limpia y eficiente, apuntando hacia fertilizantes más verdes y un mejor aprovechamiento de corrientes residuales industriales.

¿Por qué repensar la fabricación de urea?
La producción actual de urea se basa en procesos centenarios de alta temperatura y alta presión que consumen hasta el 2 % de la energía global y emiten más de una tonelada de CO2 por cada tonelada de urea producida. Al mismo tiempo, centrales eléctricas, fábricas y corrientes de aguas residuales liberan dióxido de carbono y nitratos que a menudo quedan sin aprovechar o causan daños ambientales. La electrosíntesis de urea ofrece una forma de hacer dos cosas a la vez: limpiar CO2 y nitrato mientras se fabrica un fertilizante valioso a temperatura ambiente. El problema es que, a las diminutas escalas moleculares en una superficie metálica, los fragmentos con carbono y nitrógeno tienden a seguir caminos distintos, formando muchos subproductos en lugar de unirse de forma ordenada en urea.
Una línea de ensamblaje molecular inspirada en click
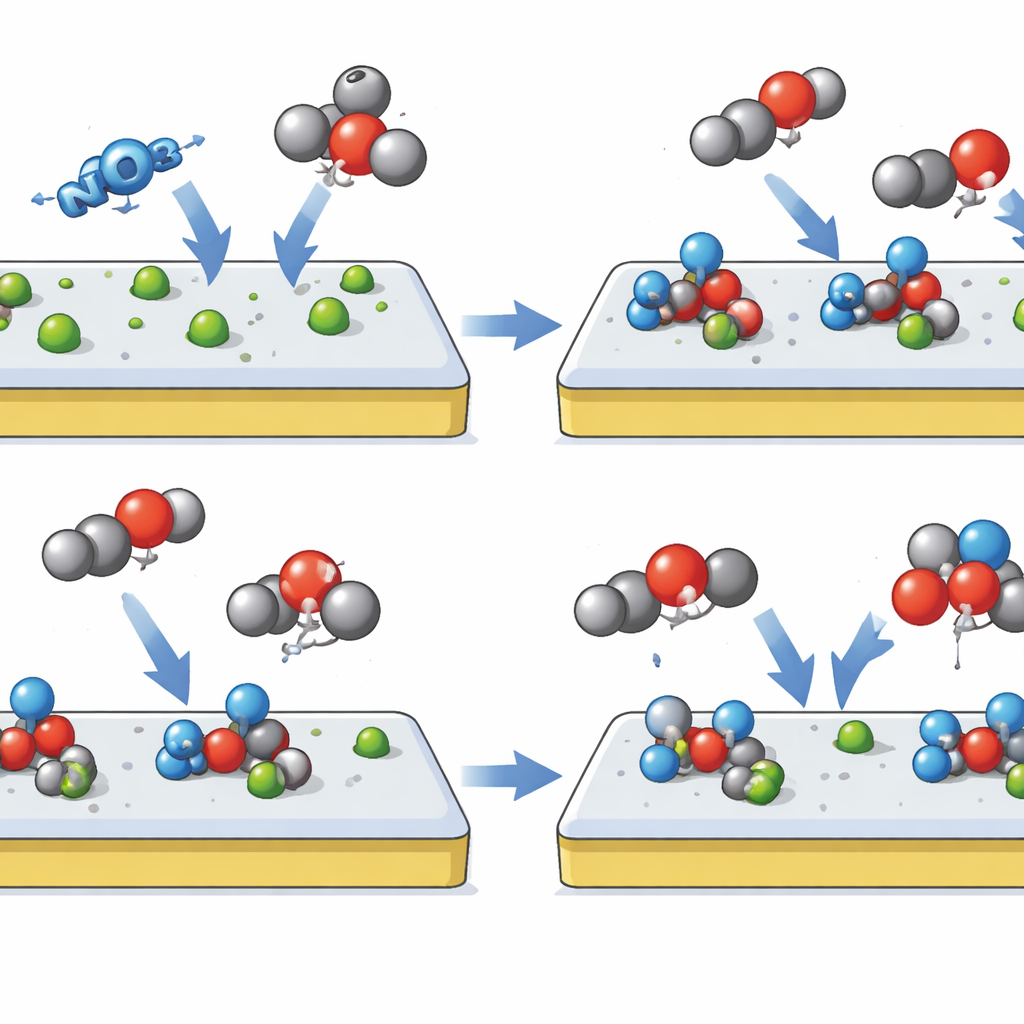
Los investigadores se inspiran en la química click, un conjunto de reacciones valoradas por unir piezas moleculares rápida, selectiva y eficientemente, con poco desperdicio. Traducen esta idea a la superficie de un electrodo construyendo un catalizador de “sitios click jerárquicos” basado en óxido de indio modificado suavemente con el elemento selenio, denominado Se–InOx. El diseño crea dos etapas secuenciales en la misma superficie. En la primera etapa, el catalizador favorece fuertemente la captura de nitrato desde la solución y su conversión en un fragmento estable de tipo nitrito, rechazando deliberadamente la unión del CO2 entrante. En la segunda etapa, ese fragmento de nitrógeno anclado se convierte en un punto de acople que incentiva la llegada del CO2 para conectarse, formando un intermedio clave con enlace carbono‑nitrógeno que conduce directamente a la urea.
Cómo la superficie inteligente hace su trabajo
Para que este comportamiento sea posible, el equipo reajusta sutilmente el paisaje electrónico del óxido de indio sustituyendo una pequeña fracción de sus átomos de oxígeno por selenio. Esta modificación aumenta la densidad electrónica local y distorsiona la red cristalina lo suficiente para que el CO2 encuentre la superficie poco atractiva, mientras que el nitrato y sus derivados tipo nitrito se unen más fuertemente. Simulaciones computacionales muestran que, en esta superficie afinada, formar el enlace crucial carbono‑nitrógeno requiere menos energía y compite favorablemente frente a reacciones secundarias que, de otro modo, transformarían el nitrato en amoníaco o el CO2 en ácido fórmico. Medidas sofisticadas in situ —sondeando la superficie con luz infrarroja y resonancia magnética mientras la reacción ocurre— detectan directamente los intermedios esperados, incluida la especie unida carbono‑nitrógeno, confirmando la línea de ensamblaje paso a paso que los diseñadores imaginaron.
Productos más limpios y alto rendimiento
Al probarse en una celda electroquímica de flujo, el catalizador Se–InOx produce urea con rapidez y alta pureza. En condiciones optimizadas, alcanza una velocidad de producción de urea de aproximadamente 255 milimoles por hora y por gramo de catalizador y convierte casi el 79 % de la carga eléctrica en urea, con más del 85 % del nitrógeno y esencialmente el 100 % del carbono en los productos integrados en urea en lugar de en subproductos. Las vías competidoras que generan amoníaco, ácido fórmico o hidrógeno quedan fuertemente suprimidas. El catalizador mantiene su estructura y actividad tras ciclos repetidos y en una celda escalada de 5 × 5 cm que funciona continuamente durante 20 horas, produciendo más de un gramo de urea sólida que supera las pruebas de pureza por resonancia magnética nuclear.
Costes, impacto climático y promesa futura
Más allá del rendimiento en laboratorio, los autores evalúan si este enfoque podría tener sentido económico y ambiental a mayor escala. Su análisis sugiere que, si se alimenta con electricidad renovable económica y se mejora modestamente la eficiencia, la urea electroquímica podría acercarse o incluso superar en precio a las rutas actuales, especialmente si también se valoran los subproductos. Una evaluación del ciclo de vida muestra que usar electricidad baja en carbono puede reducir las emisiones de gases de efecto invernadero por kilogramo de urea por debajo de las de la ruta convencional. En términos sencillos, este trabajo demuestra que superficies diseñadas al estilo “click” pueden coreografiar cómo se encuentran el carbono y el nitrógeno residuales, convirtiendo un problema de contaminación en una solución fertilizante y ofreciendo un plano para la producción más limpia de otros compuestos complejos.
Cita: Sun, Y., Tian, M., Wu, Q. et al. Sequential-chain coupling over hierarchical click-sites enables highly selective urea electrosynthesis. Nat Commun 17, 2388 (2026). https://doi.org/10.1038/s41467-026-69207-4
Palabras clave: electrosíntesis de urea, utilización de dióxido de carbono, reducción de nitrato, catálisis heterogénea, fertilizante ecológico