Clear Sky Science · es
Biología estructural unicelular con cristalografía electrónica intracelular
Ver la forma de la vida, una célula a la vez
Las proteínas son las pequeñas máquinas que mantienen viva a cada célula, pero para entender realmente cómo funcionan, los científicos necesitan ver sus formas tridimensionales con gran detalle. Tradicionalmente, eso ha implicado purificar grandes cantidades de proteína y hacer crecer cristales grandes y frágiles fuera de la célula; a menudo un proceso lento y propenso al fracaso. Este estudio presenta una nueva forma de leer la estructura proteica directamente a partir de un solo cristal dentro de una única célula, usando electrones en lugar de rayos X. Apunta hacia un futuro en el que la biología estructural de alta resolución pueda realizarse en laboratorios corrientes e incluso a nivel de células individuales.
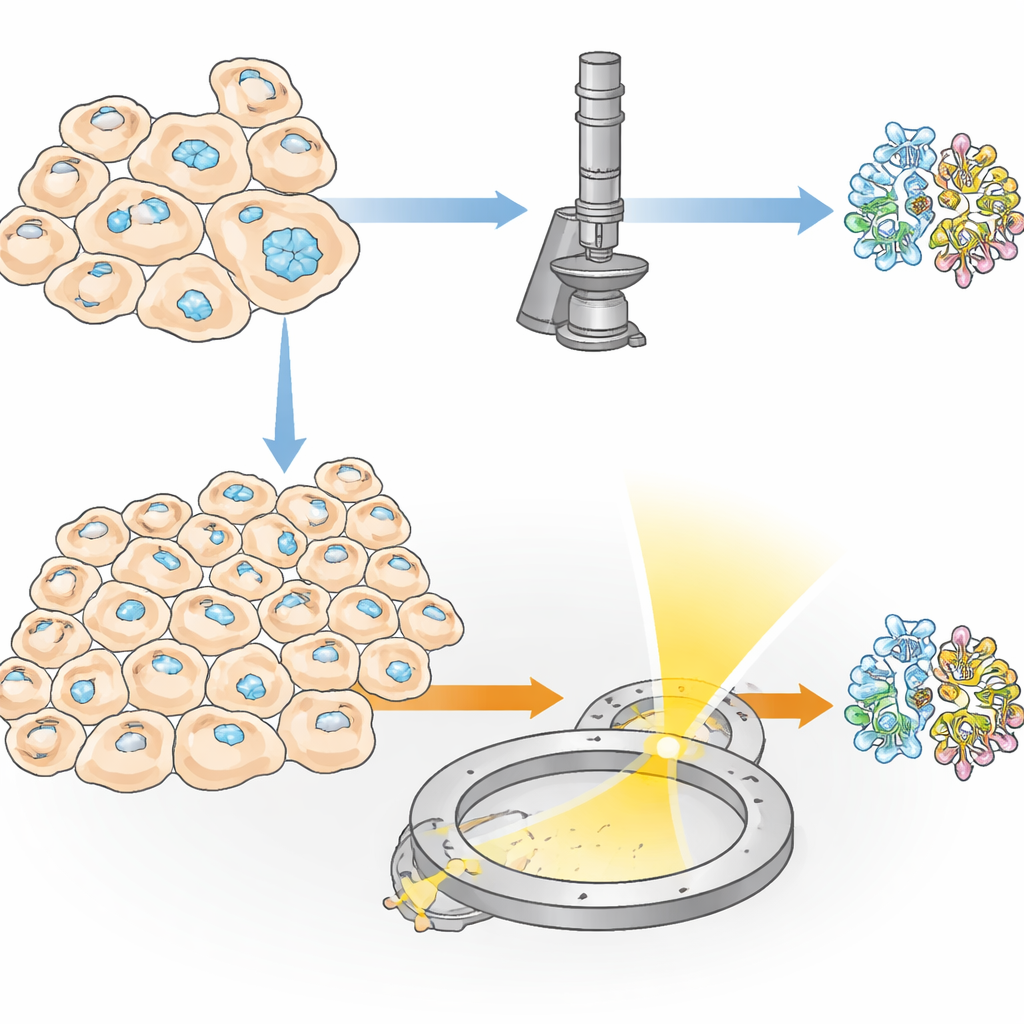
Cristales ocultos dentro de células vivas
Algunas proteínas se agrupan de forma natural en pequeños cristales dentro de células vivas, cumpliendo funciones como almacenamiento, protección o ayudando a las células a responder al estrés. Los investigadores también pueden inducir a las células a producir tales cristales mediante ingeniería para que expresen grandes cantidades de una proteína elegida. Esta cristalización “in‑cell” tiene dos grandes ventajas: la proteína nunca abandona un entorno similar al natural, y rasgos delicados —como modificaciones con azúcares o pequeñas moléculas unidas— pueden conservarse de formas que suelen fallar en la cristalización en tubo de ensayo. Sin embargo, ha persistido un obstáculo importante: en muchos experimentos, sólo una fracción muy pequeña de las células forma cristales, por lo que los métodos tradicionales con rayos X necesitan decenas de miles de cristales y, por tanto, cantidades enormes de células.
Una nueva vía: electrones en lugar de rayos X
Los autores introducen un método que denominan IncelluloED, que combina la cristalización in‑cell con la difracción electrónica tridimensional. Los electrones interactúan mucho más fuertemente con la materia que los rayos X, lo que significa que se pueden obtener datos útiles a partir de cristales más pequeños y en menor número. El equipo eligió una proteína fúngica llamada HEX‑1, que normalmente forma cristales hexagonales que ayudan a taponar pequeños poros entre células fúngicas bajo estrés. Produciendo esta proteína dentro de células de insecto, crearon cristales microscópicos regulares que sirvieron como caso de prueba para la nueva cadena de trabajo.
Convertir un cristal en un mapa detallado
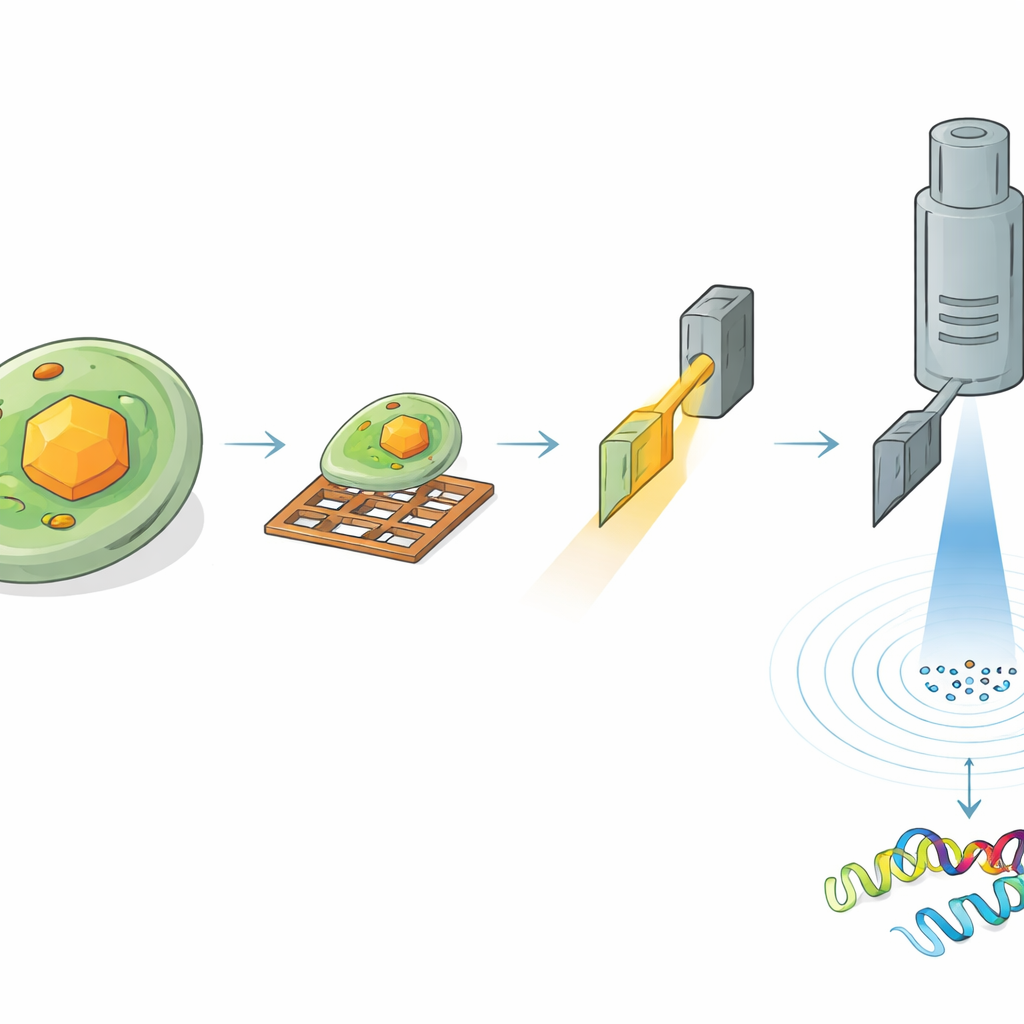
Para leer la estructura de HEX‑1 dentro de una célula, los investigadores tuvieron que localizar y adelgazar cuidadosamente la región adecuada de la muestra. Primero, congelaron las células con cristales sobre pequeñas rejillas metálicas y cubrieron la superficie con una fina capa de platino. Usando microscopía de luz criogénica, escanearon grandes áreas de la rejilla para localizar las células que contenían cristales y midieron las posiciones tridimensionales de los cristales bajo la superficie. A continuación, trasladaron la misma muestra a un instrumento especializado que combina un microscopio electrónico de barrido con un haz de iones enfocado. Guiados por las imágenes de luz previas, fresaron el material circundante para tallar una rebanada ultradelgada, o lamela, que atravesara el cristal elegido, de apenas unos cientos de nanómetros de espesor —ideal para que los electrones la atraviesen.
Los electrones revelan detalle atómico en volúmenes microscópicos
Las lamelas preparadas se transfirieron luego a un microscopio electrónico de alta gama que operaba a temperaturas criogénicas. Mientras la rebanada de cristal se rotaba lentamente en el microscopio, un haz de electrones finamente controlado la atravesaba, creando una serie de patrones de difracción —delicadas disposiciones de puntos que codifican las posiciones de los átomos. A partir de un volumen cristalino de aproximadamente 1,6 micras cúbicas, el equipo reconstruyó la estructura 3D completa de HEX‑1 a 1,9 angstrom de resolución, lo suficientemente nítida como para modelar la mayor parte de las cadenas laterales de la proteína. Volúmenes incluso menores, de alrededor de 0,8 micras cúbicas, produjeron una estructura casi idéntica con una resolución solo ligeramente inferior. Es importante destacar que los modelos resultantes coincidieron estrechamente con los obtenidos mediante un enfoque convencional por rayos X en serie, que requirió más de 60.000 cristales y un volumen cristalino total aproximadamente siete millones de veces mayor.
Cómo esto cambia las reglas del juego en biología estructural
Comparaciones lado a lado mostraron que la estructura determinada a partir de un solo cristal para difracción electrónica in‑cell es esencialmente la misma que la promediada a partir de decenas de miles de cristales con rayos X. Cualquier diferencia fue menor y se concentró principalmente en bucles flexibles, donde se espera movimiento natural. Los investigadores también demostraron que las dosis de electrones usadas fueron lo bastante bajas como para evitar daños por radiación graves, y que cada cristal procesado produjo datos de alta calidad. Aunque preparar las lamelas delgadas aún requiere habilidad y tiempo, los instrumentos necesarios —microscopios de luz criogénicos, sistemas de haz de iones enfocado y microscopios electrónicos criogénicos— ya son comunes en muchos centros de investigación.
De muchas células a un laboratorio estructural de una sola célula
Este trabajo demuestra que ahora es posible determinar la estructura a nivel atómico de una proteína a partir de un solo cristal dentro de una sola célula, sin purificar nunca la proteína. IncelluloED podría ser especialmente potente cuando sólo unas pocas células forman cristales, o cuando las proteínas son difíciles de aislar sin perder socios importantes o grupos químicos. A medida que la cadena de trabajo se automatice y se extienda a otras proteínas, puede permitir a los investigadores explorar cómo varían las estructuras de célula a célula, estudiar cambios relacionados con enfermedades en su entorno nativo e incluso apoyar el descubrimiento de fármacos directamente en células vivas. En efecto, el estudio acerca mucho más a la realidad la visión de un “laboratorio estructural de una sola célula”.
Cita: Bílá, Š., Pinkas, D., Khakurel, K. et al. Single-cell structural biology with intracellular electron crystallography. Nat Commun 17, 2109 (2026). https://doi.org/10.1038/s41467-026-69205-6
Palabras clave: difracción de electrones, cristalografía in cellulo, biología estructural unicelular, estructura de proteínas, crio‑EM