Clear Sky Science · es
14-3-3ζ interactúa con el dominio de unión al ADN de FOXO3a y disocia competitivamente el ADN mediante anclaje de doble motivo
Cómo las células cancerosas desconectan su propio interruptor de autodestrucción
Nuestras células llevan sistemas de seguridad integrados que pueden desencadenar su propia muerte cuando se vuelven demasiado dañadas o peligrosas. Uno de estos sistemas está controlado por una proteína llamada FOXO3a, que activa genes que inducen a las células rebeldes a suicidarse. Sin embargo, muchos cánceres encuentran formas de silenciar a FOXO3a y seguir proliferando. Este estudio explora los detalles moleculares de cómo otra proteína, 14-3-3ζ, ayuda a las células cancerosas a desprender a FOXO3a del ADN y desactivar este interruptor de autodestrucción.
La proteína guardiana que empuja contra el cáncer
FOXO3a actúa como un inspector de seguridad de la célula. Se une a puntos específicos del ADN y activa genes que frenan el crecimiento o desencadenan la muerte programada de la célula (apoptosis) cuando algo va mal. En células sanas, esto ayuda a prevenir la formación de tumores. Sin embargo, en muchos cánceres, una vía promotora del crecimiento impulsada por proteínas Ras mutantes queda permanentemente activada. Esta vía activa una quinasa llamada AKT, que marca químicamente a FOXO3a en varios sitios con grupos fosfato. Esas marcas crean puntos de acoplamiento para 14-3-3ζ, una proteína dimerica “adaptadora” que reconoce motivos fosforilados en muchos blancos. Cuando 14-3-3ζ se engancha a FOXO3a, los frenos internos de la célula empiezan a fallar.
Por qué la simple afinidad de unión no podía explicar el efecto
Trabajos anteriores sobre una proteína relacionada, FOXO4, sugerían que las proteínas 14-3-3 arrancaban los factores FOXO del ADN simplemente porque se unían con más fuerza. Pero FOXO3a prefiere sus dianas de ADN naturales con más afinidad de lo que suponía el modelo anterior. En este estudio, los investigadores produjeron una versión de FOXO3a que incluye el dominio de unión al ADN y dos sitios clave de fosforilación. Midieron cuán fuertemente se une esta proteína al ADN o a 14-3-3ζ y hallaron que las diferencias en la afinidad eran moderadas: 14-3-3ζ era solo aproximadamente dos veces mejor compañero que el ADN. Aun así, en experimentos de mezcla que rastrean cómo viajan las moléculas a través de una columna de cromatografía, 14-3-3ζ fue capaz de provocar la liberación casi completa del ADN de FOXO3a, como si fuera unas 100 veces más competitivo de lo esperado. Esta discrepancia sugería que actuaba un mecanismo adicional.
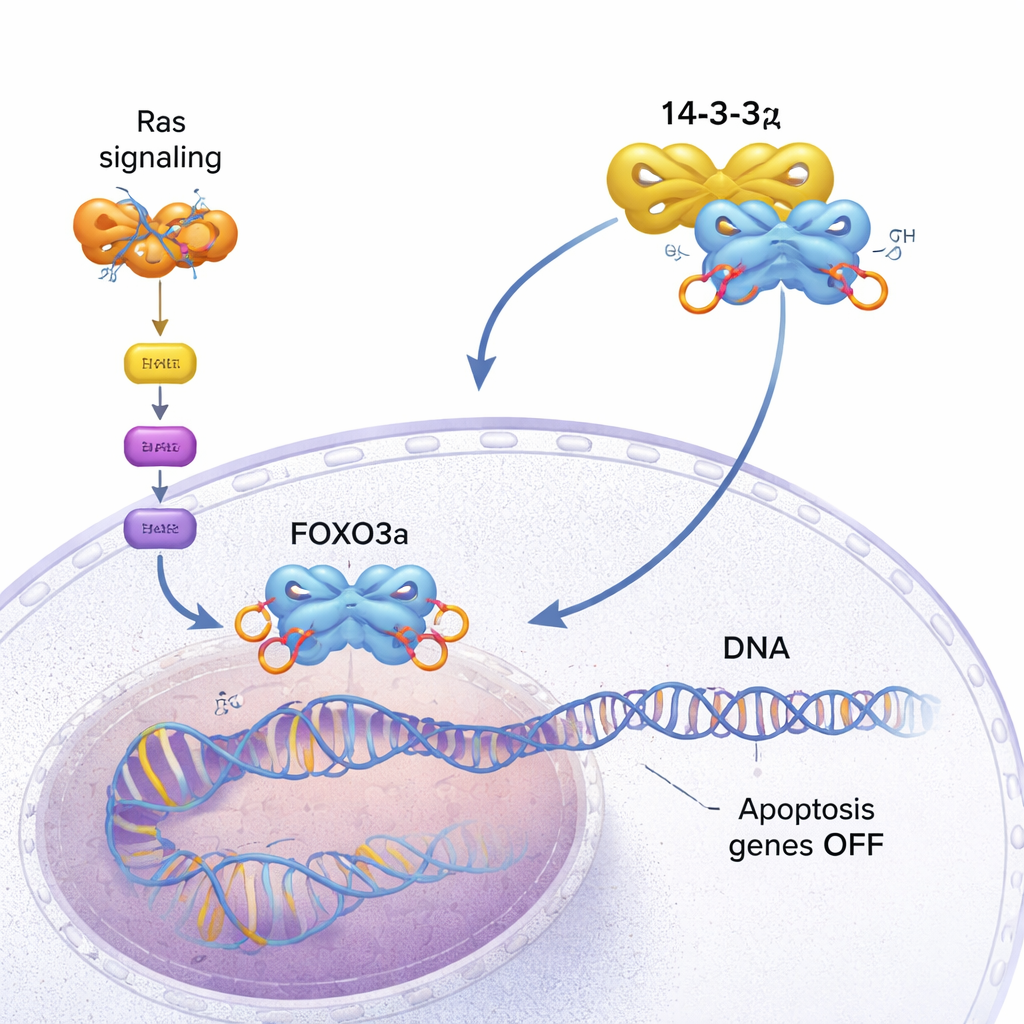
Un agarre de tres puntos que desplaza el ADN
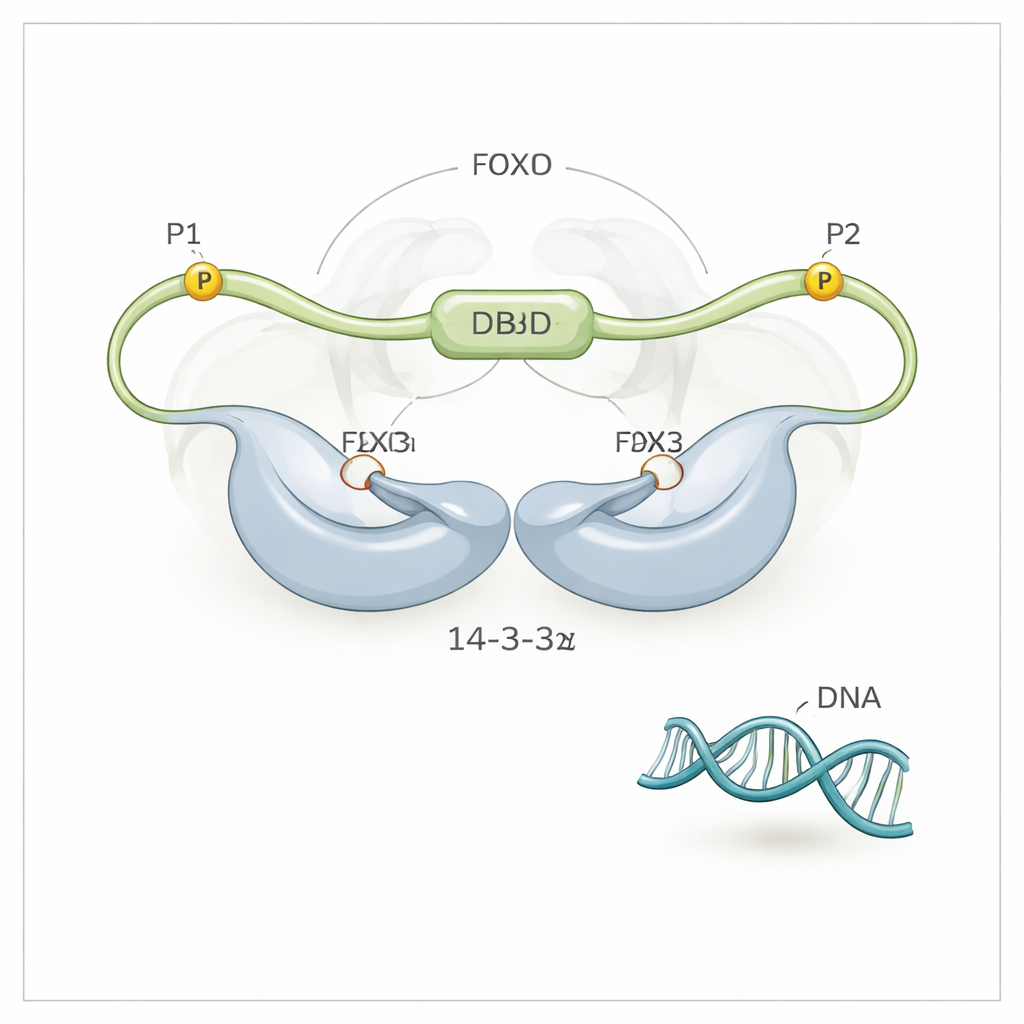
Mediante espectroscopía NMR de alta resolución, el equipo descubrió que 14-3-3ζ hace más que simplemente sujetar a FOXO3a en sus dos motivos fosforilados (denominados P1 y P2). También establece contacto directo, aunque más débil, con el propio dominio de unión al ADN (DBD) de FOXO3a, la misma superficie que normalmente abraza el ADN. La proteína 14-3-3ζ forma un dímero simétrico con dos cavidades. Cada cavidad se cierra sobre uno de los motivos fosforilados de FOXO3a, reteniendo a FOXO3a en dos puntos. Como uno de esos motivos (P2) está muy cerca, a lo largo de la cadena, del dominio de unión al ADN, este “anclaje de doble motivo” mantiene efectivamente a 14-3-3ζ junto al DBD, aumentando considerablemente la probabilidad de que el DBD choque y se una a la superficie de 14-3-3ζ en lugar de al ADN. Los investigadores pudieron incluso ver que el DBD alterna entre los dos lados del dímero 14-3-3ζ, pasando la mayor parte del tiempo protegido del ADN.
Qué etiquetas de fosfato importan más
Para dilucidar los roles de los dos sitios fosforilados, el equipo diseñó variantes de FOXO3a en las que solo uno de los sitios podía fosforilarse a la vez. Cuando solo el sitio P2, cercano al DBD, estaba activo, 14-3-3ζ podía desalojar parcialmente el ADN pero no por completo. Cuando solo el sitio más distante P1 estaba activo, 14-3-3ζ podía unirse a FOXO3a pero apenas afectaba su agarre sobre el ADN. La liberación completa del ADN requirió que ambos sitios funcionaran juntos: P1 proporciona un punto de acoplamiento inicial de alta afinidad para 14-3-3ζ, y P2 posiciona al dímero lo bastante cerca del DBD como para que la concentración local de 14-3-3ζ en ese punto sea efectivamente enorme. Este anclaje en varios pasos amplifica una preferencia de unión modesta en una poderosa capacidad para desalojar el ADN.
De la contienda molecular a nuevas ideas terapéuticas
Para un público no especializado, la conclusión clave es que las células cancerosas explotan un truco geométrico molecular ingenioso, no solo la fuerza bruta de la unión, para silenciar una proteína supresora de tumores importante. 14-3-3ζ utiliza dos pequeñas etiquetas de acoplamiento en FOXO3a como puntos de anclaje y luego se extiende para cubrir la superficie de interacción con el ADN del dominio central de FOXO3a, impidiendo que active genes de muerte celular. Dado que las familias FOXO y 14-3-3 se usan ampliamente en muchos tejidos, esta estrategia de doble anclaje probablemente sea común en otros cánceres también. Interferir ya sea con los anclajes dependientes de fosfato o con el contacto más débil con la cara de unión al ADN de FOXO3a podría restaurar su capacidad para activar los programas de autodestrucción en células tumorales, ofreciendo nuevos ángulos prometedores para el diseño de fármacos anticancerígenos.
Cita: Enomoto, S., Kuwayama, T., Nakatsuka, S. et al. 14-3-3ζ interacts with DNA-binding domain of FOXO3a and competitively dissociates DNA by dual-motif tethering. Nat Commun 17, 1503 (2026). https://doi.org/10.1038/s41467-026-69203-8
Palabras clave: FOXO3a, proteínas 14-3-3, apoptosis, señalización Ras–AKT, terapias contra el cáncer