Clear Sky Science · es
Mecanismos moleculares de los complejos de flotilina en la organización de microdominios de la membrana
Habitaciones ocultas en la superficie celular
Cada célula de tu cuerpo está envuelta por una delgada membrana que a primera vista parece simple, pero en realidad está dividida en innumerables y diminutos “vecindarios”. Estos vecindarios ayudan a controlar cómo se reciben señales, cómo entran los nutrientes y cómo sale la basura. Este estudio revela cómo un par de proteínas largamente enigmáticas, llamadas flotilinas, construyen diminutas habitaciones protegidas en la cara interna de la membrana—estructuras que pueden influir en procesos tan diversos como la señalización celular, el transporte de carga e incluso la diseminación del cáncer. 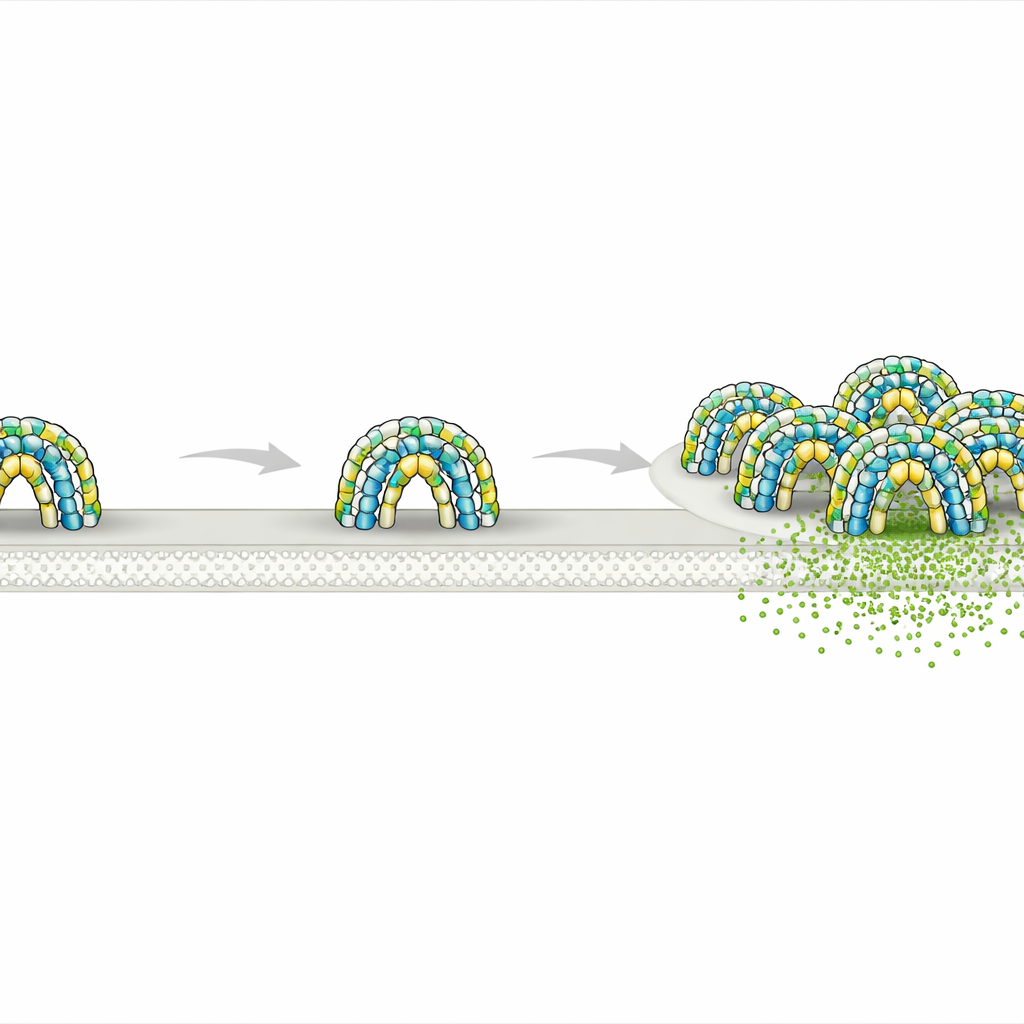
Una mirada más cercana a los diminutos vecindarios de la membrana
Los biólogos llevan tiempo sabiendo que las membranas celulares no son uniformes. En lugar de ello, lípidos y proteínas se agrupan en pequeños parches que actúan como estaciones de trabajo emergentes para tareas específicas como la comunicación o la clasificación de cargas. La flotilina‑1 y la flotilina‑2 son dos proteínas que suelen marcar dichos parches, formando pequeños puntos brillantes en la superficie celular y participando en la endocitosis—el proceso por el cual las células internalizan material—así como en la señalización y el tráfico de proteínas. Sin embargo, nadie sabía qué forma adoptan realmente las estructuras de flotilina ni cómo se reservan su propio territorio en la membrana.
Cúpulas que cercan círculos de membrana
Mediante crio‑microscopía electrónica de alta resolución sobre proteínas humanas purificadas, los investigadores descubrieron que la flotilina‑1 y la flotilina‑2 se ensamblan en un complejo sorprendentemente grande formado por 44 copias de proteína, alternando entre ambos tipos. Juntas forman una cúpula rígida situada en la cara interna de la membrana. La base de esta cúpula está construida a partir de segmentos ancladores de membrana ricos en aminoácidos grasos y en modificaciones lipídicas que se hunden parcialmente en la membrana. Por encima, largos tallos helicoidales forman una pared compacta en forma de barril, y un tejado de segmentos proteicos entrelazados remata la estructura. El anillo de flotilina en la base define un parche circular de membrana de unos 30 nanómetros de diámetro—esencialmente cercando un diminuto disco de membrana y el espacio justo por encima de él.
Cúpulas flexibles observadas dentro de células vivas
Para comprobar si estas cúpulas existen en células reales, el equipo diseñó células T humanas para producir flotilina‑1 y flotilina‑2 etiquetadas con fluorescencia y las observó combinando microscopía óptica y tomografía por crio‑electrónica. Observaron estructuras huecas en forma de cúpula adheridas a la superficie interna de la membrana plasmática, coincidiendo estrechamente con la forma determinada en las muestras purificadas. Muchas cúpulas aparecían ligeramente distorsionadas o parcialmente abiertas, y algunas contenían densidades adicionales en su interior, probablemente otras proteínas temporalmente atrapadas bajo el tejado. En algunas regiones, varias cúpulas se agrupaban en membranas planas o curvas, incluidas endosomas y pequeñas vesículas extracelulares, lo que sugiere que cúpulas individuales pueden unirse para formar plataformas de membrana más grandes. 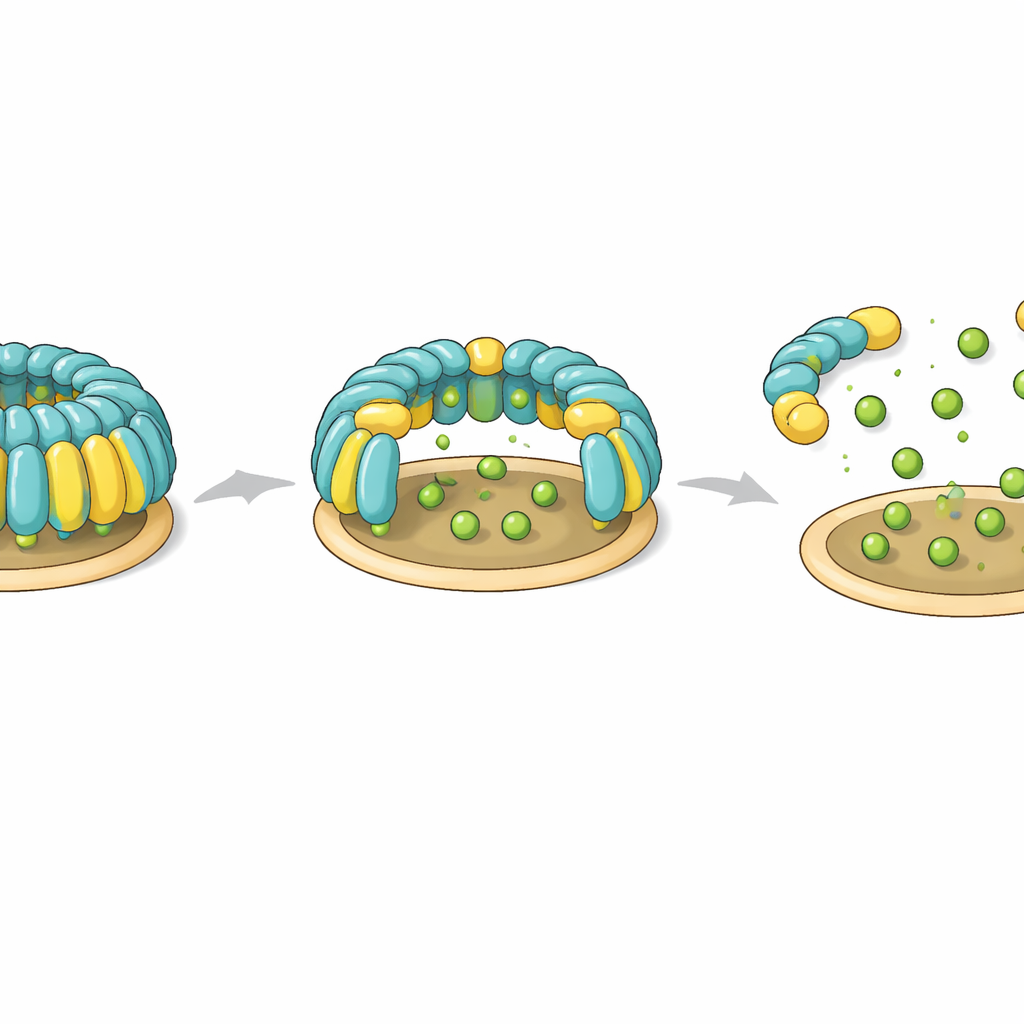
Un interruptor molecular para construir y deshacer cúpulas
El estudio también identifica una posible perilla de control que las células podrían usar para ensamblar o desmantelar las cúpulas de flotilina. Dos residuos de tirosina específicos—uno en cada proteína flotilina—se sitúan en posiciones tipo bisagra que conectan la base anclada a la membrana con la pared helicoidal. En el complejo intacto, estos residuos ayudan a formar un núcleo hidrófobo ajustado que bloquea la orientación de los dominios. Cuando los investigadores introdujeron mutaciones que imitan la adición de una carga negativa, como ocurre cuando las enzimas fosforilan estas tirosinas, toda la cúpula dejó de ensamblarse. Las mutaciones sin carga no afectaron el ensamblaje. Estas observaciones sugieren que la fosforilación en esos puntos de bisagra podría actuar como un interruptor reversible que desestabiliza la cúpula, abriéndola o rompiéndola durante procesos como la endocitosis dependiente de flotilina.
Redefiniendo cómo estos dominios moldean la membrana
Se consideraba que los parches de flotilina eran principalmente “balsas lipídicas” ricas en colesterol y grasas afines. Sorprendentemente, cuando el equipo examinó burbujas de membrana gigantes desprendidas de células, las flotilinas prefirieron las regiones más fluidas, no‑raft, en lugar de las rígidas y densas en colesterol. El análisis lipídico mostró solo un enriquecimiento modesto de una molécula en particular, la esfingosina, dentro de los complejos de flotilina, mientras que otros lípidos asociados a las balsas no estaban concentrados. Esto apunta a un principio organizador distinto: en lugar de ser pasajeros en balsas lipídicas preexistentes, las cúpulas de flotilina actúan como contenedores estructurales que segregan lateralmente fragmentos de membrana, capturando determinadas proteínas y lípidos dentro de su área cercada.
Por qué importa esta diminuta arquitectura
En términos cotidianos, los complejos de flotilina se comportan como toldos modulares que las células pueden desplegar en su superficie interna para cercar pequeños lotes circulares de membrana. Cada cúpula puede alojar una mezcla distintiva de proteínas y lípidos asociados, y, al agruparse con otras, puede construir zonas funcionales mayores para señalización, clasificación de cargas o formación de vesículas. Dado que las cúpulas son flexibles y parecen abrirse y cerrarse, y que su ensamblaje es sensible a la fosforilación, las células pueden remodelar dinámicamente estas estructuras en respuesta a señales. Este trabajo, por lo tanto, reinterpreta a las flotilinas, pasando de ser vagas “marcadoras de balsas” a elementos arquitectónicos concretos que ayudan a esculpir la membrana en micro‑espacios de trabajo especializados.
Cita: Lu, MA., Qian, Y., Ma, L. et al. Molecular mechanisms of flotillin complexes in organizing membrane microdomains. Nat Commun 17, 2541 (2026). https://doi.org/10.1038/s41467-026-69197-3
Palabras clave: flotilina, microdominios de membrana, crio‑microscopía electrónica, endocitosis, balsas lipídicas