Clear Sky Science · es
La supervivencia de macrófagos residentes en tejidos depende de la función mitocondrial regulada por SerpinB2 en la inflamación crónica
Por qué importan las células inmunitarias de la grasa
La mayoría de la gente piensa en la grasa corporal como un depósito pasivo, pero en realidad es un tejido dinámico lleno de células inmunitarias que ayudan a controlar la inflamación y la glucemia. Este estudio revela cómo un grupo específico de células inmunitarias de larga vida en la grasa abdominal profunda actúa como guardianes frente a la diabetes tipo 2 —y cómo la inflamación crónica en la obesidad las elimina silenciosamente al dañar sus pequeñas centrales energéticas, las mitocondrias.
Dos tipos de guardianes en la grasa
El tejido adiposo visceral —la grasa alojada alrededor de los órganos internos— contiene dos tipos principales de células inmunitarias llamadas macrófagos. Un tipo es de corta vida y se renueva constantemente desde la sangre; estos macrófagos “inflamatorios” tienden a alimentar la inflamación y la resistencia a la insulina. El otro tipo es de larga duración, macrófagos residentes del tejido que nacen temprano en la vida y normalmente ayudan a mantener la calma del tejido, apoyan el almacenamiento saludable de grasa y promueven la sensibilidad a la insulina a nivel corporal. Al seguir estas células en ratones y comparar la actividad génica, los investigadores mostraron que los macrófagos residentes están enriquecidos en genes antiinflamatorios y que mejoran la sensibilidad a la insulina, mientras que los macrófagos derivados de monocitos entrantes expresan genes que empeoran el control de la glucosa.
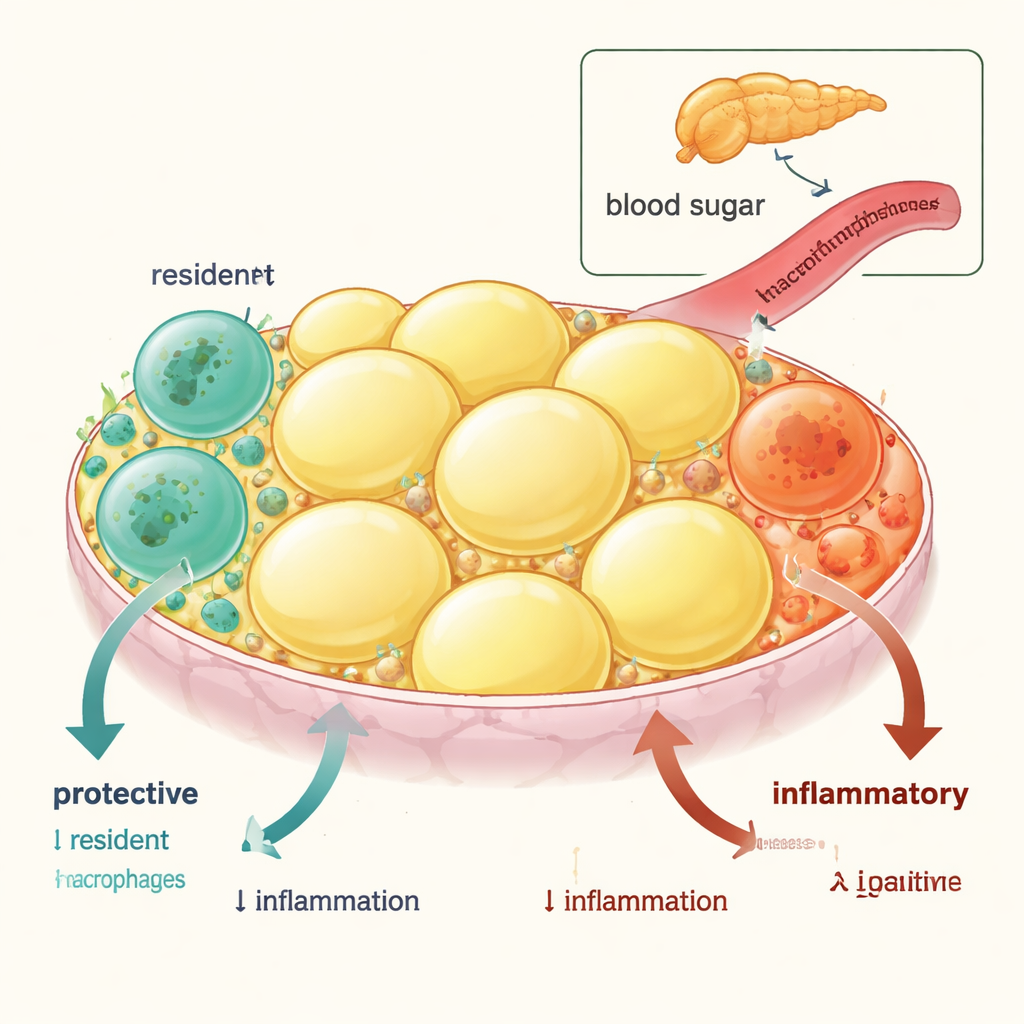
Cuando la inflamación mata a los buenos
En la obesidad, este equilibrio protector se desplaza. El equipo encontró que tanto en ratones obesos como en personas obesas o diabéticas, el número de macrófagos residentes en la grasa visceral disminuye, mientras que aumentan los macrófagos inflamatorios. Imágenes detalladas y marcadores de muerte celular revelaron la razón: los macrófagos residentes sufren más muerte celular programada (apoptosis), mientras que las células inflamatorias no. De forma notable, cuando ratones obesos fueron retirados de una dieta alta en grasas, la población residente se recuperó lentamente mediante proliferación local y la salud metabólica mejoró —demostrando que esta pérdida está impulsada por el estado inflamatorio y puede revertirse.
Una única proteína vincula las mitocondrias con la supervivencia
Una pista clave fue una proteína llamada SerpinB2, conocida sobre todo por sus funciones en la coagulación sanguínea. Los investigadores descubrieron que SerpinB2 se produce a niveles muy altos dentro de los macrófagos residentes, pero mucho menos en los inflamatorios. En humanos y ratones obesos, los macrófagos residentes redujeron de forma pronunciada la expresión de SerpinB2, y un índice de masa corporal más alto se asoció con menos células SerpinB2‑positivas. Experimentos en células sin SerpinB2 mostraron un mayor escape de citocromo c —una proteína crucial— desde las mitocondrias hacia el citoplasma, un desencadenante clásico de apoptosis. Estos macrófagos deficientes en SerpinB2 tenían menos defensas antioxidantes, más especies reactivas de oxígeno (ROS) mitocondriales y mayor consumo de oxígeno, signos de mitocondrias estresadas y sobrecargadas que empujan a las células hacia un comportamiento inflamatorio y la muerte.
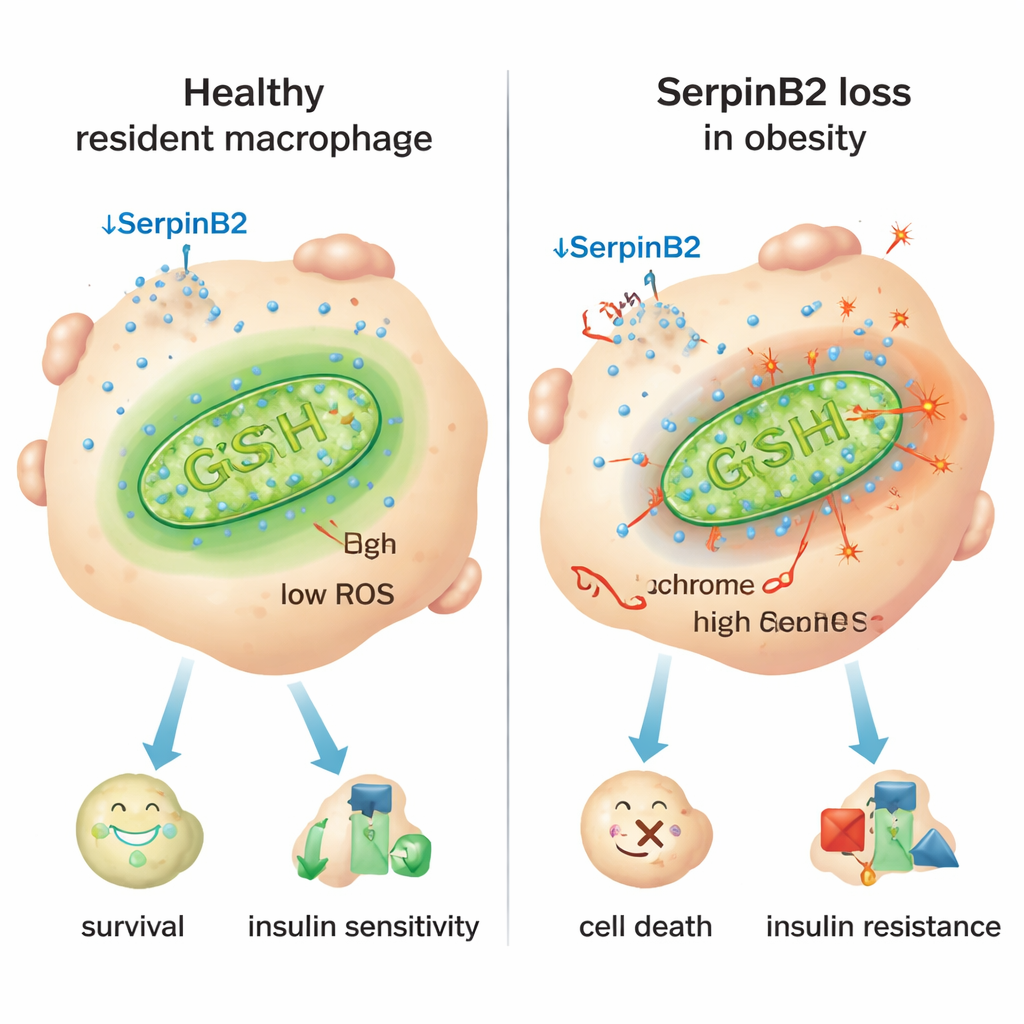
El interruptor inflamatorio y una posible solución
El estudio rastreó este estrés mitocondrial hasta señales inflamatorias crónicas en la obesidad, sobre todo la citocina interferón‑γ (IFN‑γ), que se produce en exceso en el tejido adiposo. IFN‑γ activa un represor transcripcional llamado Ikaros que se une a la región de control del gen SerpinB2 y lo reprime. En ratones diseñados para que sus células mieloides no respondieran a IFN‑γ, los macrófagos residentes conservaron SerpinB2, sobrevivieron mejor y los animales mostraron glucemia más baja, mejor sensibilidad a la insulina y adipocitos más pequeños. Por el contrario, la eliminación específica de SerpinB2 en macrófagos empeoró la intolerancia a la glucosa y la resistencia a la insulina, en parte porque el tejido adiposo se volvió más inflamado y se expandió. Aumentar los niveles del antioxidante glutatión con el suplemento N‑acetilcisteína (NAC) restauró la protección mitocondrial, rescató la supervivencia de los macrófagos residentes, redujo el tamaño de los adipocitos y mejoró medidas metabólicas incluso cuando faltaba SerpinB2.
Qué significa esto para la salud metabólica
Para un lector general, el mensaje central es que no toda la grasa ni todas las células inmunitarias residentes en la grasa son dañinas. Un grupo especializado y de larga vida de macrófagos en la grasa visceral nos protege de la inflamación descontrolada y de la hiperglucemia manteniendo sus mitocondrias sanas mediante defensas antioxidantes impulsadas por SerpinB2. En la obesidad, las señales inflamatorias crónicas apagan SerpinB2, las mitocondrias se estresan, estas células protectoras mueren y macrófagos más dañinos toman el relevo, contribuyendo a la resistencia a la insulina. El trabajo sugiere que terapias destinadas a preservar los macrófagos residentes —bloqueando el freno IFN‑γ/Ikaros sobre SerpinB2 o apoyando las defensas antioxidantes basadas en glutatión— podrían ayudar a prevenir o tratar enfermedades metabólicas vinculadas a la obesidad.
Cita: Vasamsetti, S.B., Sadaf, S., Uddin, M.A. et al. Tissue-resident macrophage survival depends on mitochondrial function regulated by SerpinB2 in chronic inflammation. Nat Commun 17, 1493 (2026). https://doi.org/10.1038/s41467-026-69196-4
Palabras clave: grasa visceral, macrófagos, mitocondrias, resistencia a la insulina, SerpinB2