Clear Sky Science · es
TANGO: Análisis y curación de partículas en crio‑electrón tomografía
Ver las células en 3D y luego entender la multitud
La crio‑electrón tomografía permite a los científicos congelar células vivas en acción y capturarlas en tres dimensiones, casi como pausar una película con detalle atómico. Pero una vez que miles de pequeños «puntos» moleculares se han mapeado dentro de una célula, surge un nuevo problema: ¿cómo entendemos quién está junto a quién, quién forma equipos y dónde se esconden los patrones importantes en esta ciudad molecular abarrotada? Este estudio presenta TANGO, un marco de software que transforma mapas 3D de partículas en bruto en relatos comprensibles sobre cómo se organizan las moléculas y cómo cooperan.
De puntos en el hielo a un mapa de vecinos moleculares
La crio‑electrón tomografía comienza inclinando una muestra congelada en el microscopio para registrar muchas imágenes 2D. Estas se combinan en un volumen 3D, llamado tomograma, donde complejos moleculares individuales aparecen como manchas borrosas. Los métodos existentes ya usan estos datos para afinar las formas de las moléculas promediando muchas copias, pero en gran medida ignoran un tesoro igualmente rico: las posiciones y orientaciones exactas de cada partícula. TANGO está diseñado para explotar esta información desatendida. Trata todas las partículas como puntos en el espacio, cada uno con una dirección, y analiza cómo están posicionados y orientados entre sí. Al hacerlo, va más allá de preguntar simplemente “¿cómo es esta molécula?” para plantear “¿cómo se organizan estas moléculas en la célula?” 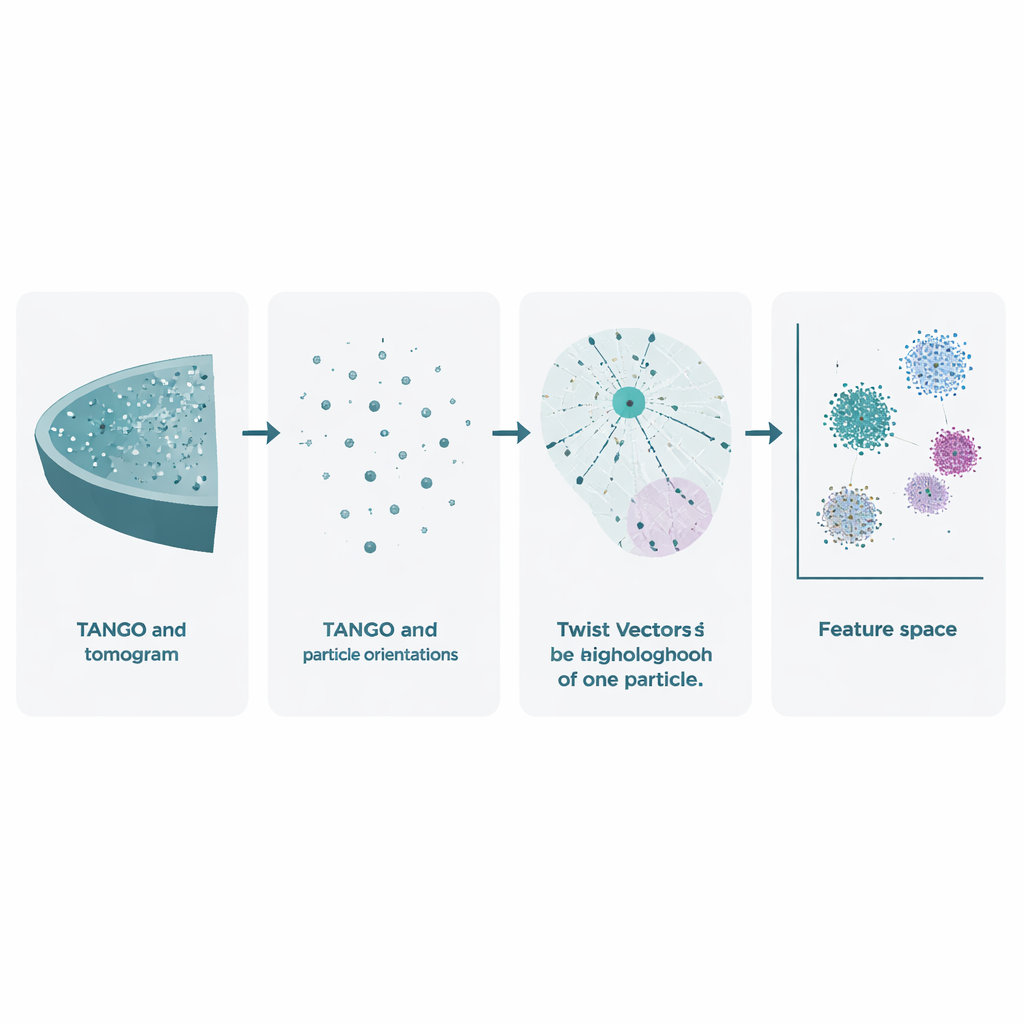
Capturar giros y torsiones con un nuevo descriptor
En el núcleo de TANGO está la idea de los «vectores de giro» (twist vectors). Para una partícula dada, el software examina todos sus vecinos dentro de un radio elegido y registra dos cosas: dónde se encuentra cada vecino en el espacio 3D y cómo está rotado respecto a la partícula central. Estas relaciones combinadas de posición y ángulo se codifican como descripciones numéricas concisas conocidas como descriptores de giro. Dado que TANGO siempre reorienta los vecindarios a un marco de referencia común, estos descriptores son insensibles a cómo esté rotada la muestra en el microscopio. Esto posibilita comparar vecindarios locales entre diferentes tomogramas y experimentos de forma coherente.
Limpiar datos ruidosos y reconstruir ensamblajes moleculares
Los datos experimentales reales son desordenados: los métodos automáticos de selección pueden incluir muchas partículas falsas y perder la pista de qué fragmentos pequeños pertenecen a qué estructura grande. TANGO aborda esto convirtiendo la red de relaciones de giro en un grafo, donde las partículas son nodos y los enlaces de vecindario son aristas. Analizando cómo se conectan los nodos, TANGO puede reagrupar las partículas en sus ensamblajes parentales correctos y descartar los atípicos que no encajan en la geometría esperada. Los autores muestran que este enfoque recupera con precisión la arquitectura anular de los poros nucleares en la envoltura nuclear de la célula, la disposición tubular de los microtúbulos y las conchas aproximadamente esféricas de partículas semejantes al virus VIH inmaduro. En cada caso, TANGO limpia tanto las listas de partículas como restaura qué piezas pertenecen juntas, a menudo igualando o mejorando la curación manual detallada.
Detectar defectos sutiles y patrones en retículos
Muchos virus y estructuras celulares forman retículos repetitivos, como teselados moleculares en superficies curvas. TANGO usa sus descriptores de giro para medir cuán regulares son estos patrones y para detectar lugares donde se doblan o rompen. Un ingrediente clave es una «puntuación angular» que compara orientaciones respetando simetrías inherentes, como la simetría de seis veces de los hexámeros. Aplicado a cápsides maduras del VIH, TANGO detecta pentámeros —unidades de cinco necesarias para cerrar la concha cónica— ocultos entre grandes campos de hexámeros. En retículos de VIH inmaduros, separa regiones bien ordenadas de regiones distorsionadas y asocia puntuaciones angulares bajas con zonas irregulares o rotas de la concha. Análisis similares en datos sintéticos de cromatina y ribosomas revelan nucleosomas apilados, disposiciones helicoidales de ADN‑proteína y pares recurrentes de ribosomas que recuerdan estados de traducción descritos anteriormente. 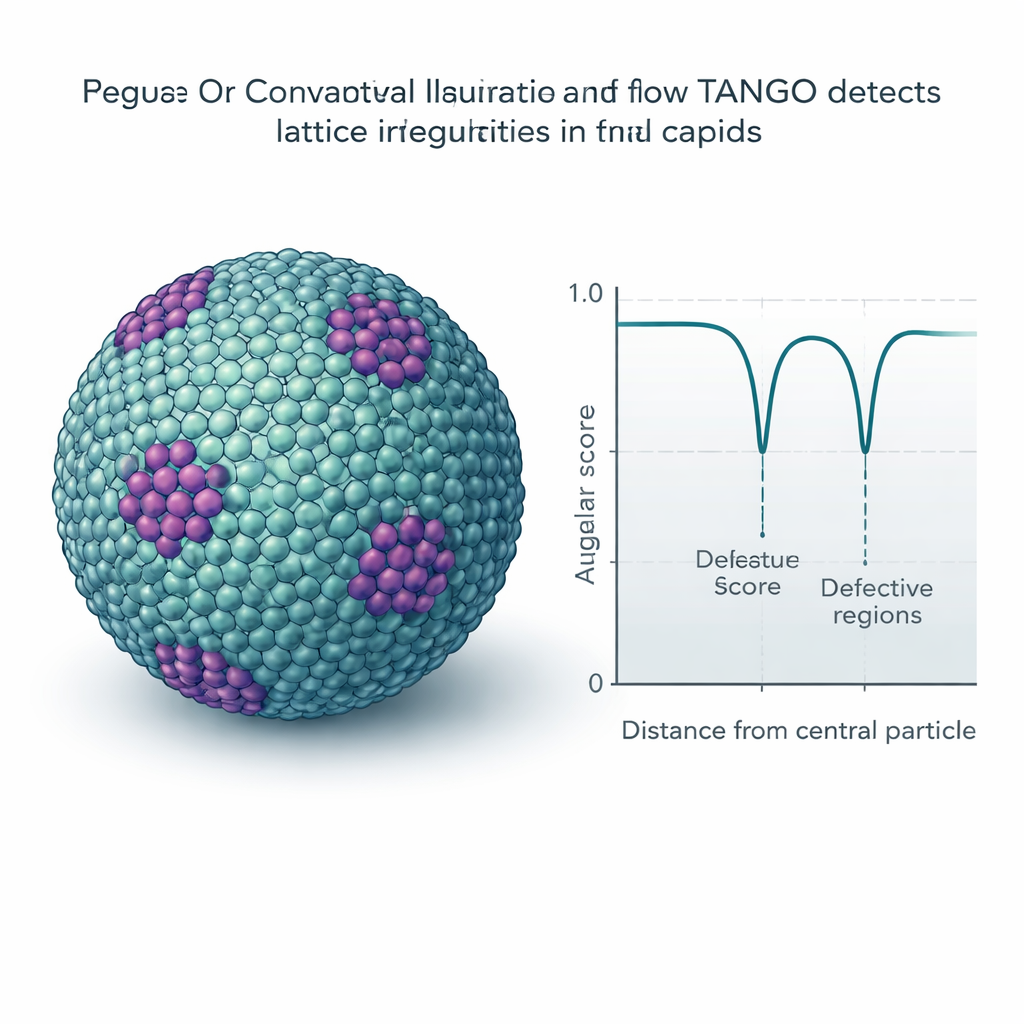
Una caja de herramientas flexible para explorar la arquitectura celular
TANGO está implementado como software Python de código abierto y cuenta con una interfaz gráfica para que los usuarios prueben distintas formas de vecindario, filtros y características sin programación intensiva. Al ser modular, los investigadores pueden incorporar sus propias medidas geométricas o descriptores de patrones y usarlos de inmediato dentro del mismo flujo de trabajo. Para los recién llegados, esto reduce la barrera para explorar la organización espacial; para los expertos, proporciona un marco que puede crecer con nuevas ideas y conjuntos de datos.
Por qué importa para entender las células vivas
En términos sencillos, este trabajo da a los biólogos una forma de pasar de imágenes estáticas de moléculas individuales a mapas dinámicos de cómo esas moléculas se organizan y cooperan dentro de las células. Al codificar las relaciones de «quién está cerca de quién» y «cómo están orientados» en características numéricas robustas, TANGO transforma datos ruidosos de microscopía 3D en patrones que se pueden agrupar, comparar y analizar estadísticamente. Esto puede revelar ensamblajes ocultos, localizar defectos en conchas virales y descubrir arreglos moleculares raros vinculados a enfermedades o a la acción de fármacos. A medida que la crio‑electrón tomografía se generalice, herramientas como TANGO ayudarán a convertir nubes densas de partículas en ideas claras sobre la coreografía interna de la vida.
Cita: Schreiber, M., Turoňová, B. TANGO: Analysis and curation of particles in cryo-electron tomography. Nat Commun 17, 1557 (2026). https://doi.org/10.1038/s41467-026-69195-5
Palabras clave: crio‑electrón tomografía, organización espacial, retículos moleculares, cápsides virales, ribosomas