Clear Sky Science · es
Ingeniería metabólica de la biosíntesis de doxorrubicina mediante optimización de P450-socios redox y análisis estructural de DoxA
Por qué importa el origen de un fármaco contra el cáncer
La doxorrubicina es uno de los fármacos fundamentales de la quimioterapia moderna, utilizada para tratar cánceres que van desde la leucemia hasta tumores de mama. Sin embargo, a pesar de décadas de uso, la forma en que producimos este medicamento es sorprendentemente indirecta: la industria suele construirlo a partir de un compuesto relacionado en lugar de permitir que su microbio nativo complete la síntesis. Este estudio descubre por qué la bacteria productora tiene dificultades para completar los pasos químicos finales y muestra cómo la reingeniería de su maquinaria interna puede aumentar de forma notable la producción de doxorrubicina completa, abriendo la puerta a suministros más fiables y potencialmente más baratos.
De bacterias del suelo a un medicamento que salva vidas
La doxorrubicina pertenece a las antraciclinas, una familia de moléculas naturales construidas por bacterias del suelo del género Streptomyces. Estos compuestos comparten un marco carbonado rígido y plano que se desliza entre las bases del ADN, además de una unidad de azúcar que se acopla en las ranuras del ADN. En conjunto, estas características bloquean la maquinaria de manejo del ADN de la célula y, en última instancia, desencadenan la muerte celular, lo que resulta útil contra las células cancerosas de rápido crecimiento. El productor clásico, Streptomyces peucetius, fabrica de forma natural principalmente un fármaco precursor llamado danorubicina, y solo una cantidad modesta de la más eficaz doxorrubicina, que difiere por un único grupo portador de oxígeno adicional. Ese pequeño cambio estructural mejora drásticamente la actividad, pero resulta sorprendentemente difícil de lograr de forma eficiente para el microbio.
Encontrar el cableado eléctrico correcto dentro de la célula
La enzima crucial que realiza los tres últimos pasos de oxidación sobre el andamiaje del fármaco se llama DoxA, miembro de la familia de los citocromos P450. Como una pequeña fábrica química, DoxA necesita un flujo constante de electrones para activar el oxígeno e incorporar nuevos átomos de oxígeno en la molécula del fármaco. Dentro de la bacteria, esos electrones se suministran a través de un relevo de proteínas auxiliares conocidas como socios redox. El genoma de S. peucetius contiene varios candidatos, lo que hacía incierto cuáles se emparejan realmente con DoxA. Al comparar la actividad génica y el metabolismo en una cepa normal, en un mutante rico en danorubicina y en un mutante rico en doxorrubicina, los investigadores identificaron un ferredoxina (Fdx4) y una ferredoxina reductasa (FdR3) como los socios naturales. Reconstruir este trío en reacciones de ensayo confirmó que DoxA funciona mejor cuando está conectado a esta cadena específica de transferencia de electrones, de la misma manera que adaptar el adaptador de alimentación correcto a un dispositivo.
Aliviar la ralentización autoinfligida de la enzima
Incluso con el cableado eléctrico correcto, DoxA tiende a atascarse en el paso final que convierte la danorubicina en doxorrubicina. Trabajos anteriores sugerían que el propio producto podría obstruir la enzima. El equipo se fijó en un gen vecino, dnrV, cuya función había sido misteriosa. Pruebas bioquímicas mostraron que la proteína DnrV se une fuertemente a una gama de moléculas antraciclínicas, incluida la doxorrubicina, sin alterarlas químicamente. Añadir DnrV a las reacciones con DoxA mejoró mucho el flujo de la química, permitiendo la conversión completa de precursores al fármaco final mientras se evitaban reacciones secundarias destructivas. En términos prácticos, DnrV actúa como una esponja interna que absorbe la doxorrubicina recién formada, impidiendo que obstruya la enzima o dañe el ADN dentro de la célula productora.
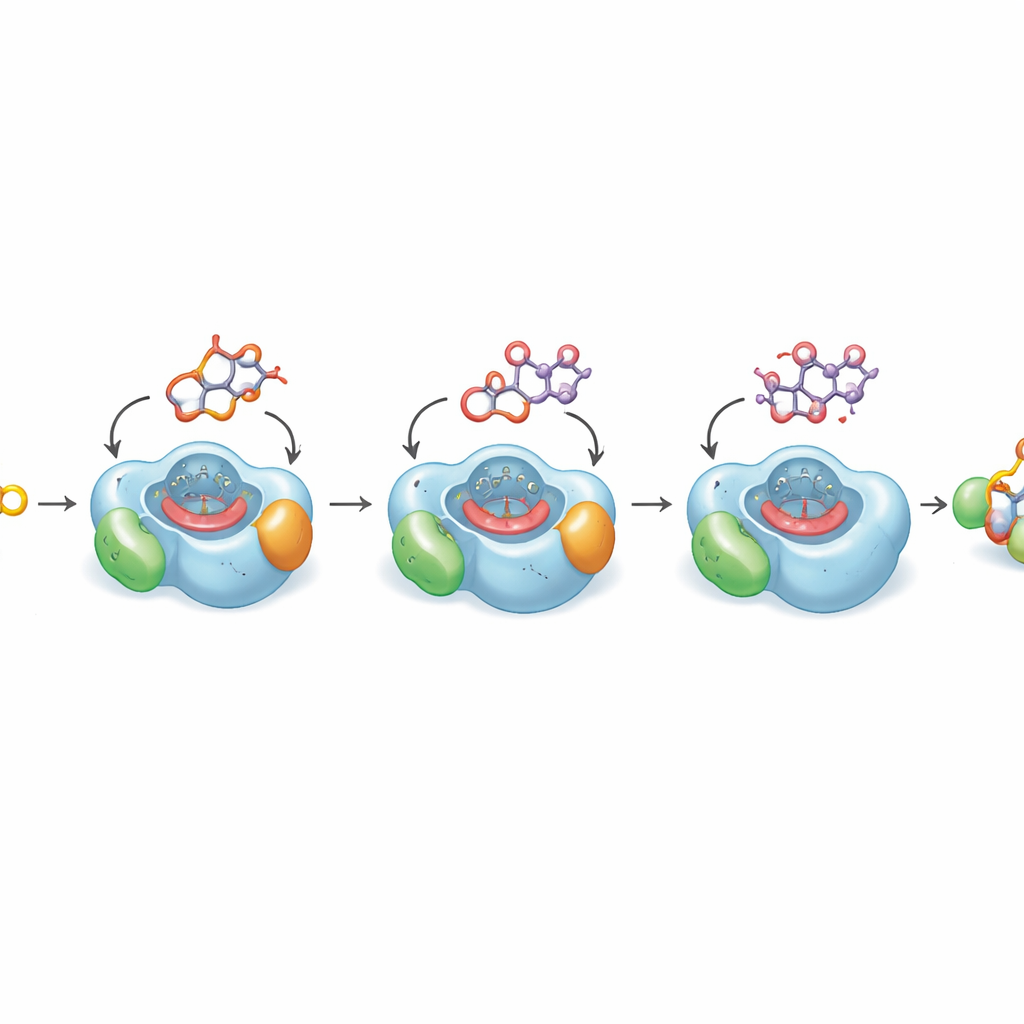
Ver por qué el último paso es tan lento
Para entender por qué la oxidación final clave es intrínsecamente lenta, los autores resolvieron estructuras cristalinas de alta resolución de DoxA unida a tres intermediarios sucesivos. Estas estructuras revelan cómo el núcleo plano del fármaco y su azúcar adjunta encajan en un bolsillo ceñido sobre el grupo hemo de la enzima, el centro metálico reactivo que realiza la oxidación. Para los pasos anteriores, el átomo de carbono que debe modificarse se sitúa cerca del hemo en una posición ideal para la reacción. Pero en el sustrato final, la danorubicina, la porción de la molécula que necesita ser hidroxilada se inclina alejándose del hemo hacia una pequeña cavidad oleosa, una disposición que cálculos cuánticos muestran que es energéticamente favorecida. Simulaciones por ordenador en escalas temporales de microsegundos confirman que la molécula solo visita ocasionalmente una pose productiva para esa última inserción de oxígeno. Este sesgo estructural explica por qué la conversión a doxorrubicina es naturalmente ineficiente.
Construir una cepa mejor para fabricar doxorrubicina
Armados con estos conocimientos, los investigadores rediseñaron racionalmente la bacteria en lugar de confiar en la mutagénesis aleatoria. Introdujeron un gen de reparación del ADN para estabilizar la producción, luego añadieron copias extra de doxA, de los socios redox óptimos fdx4 y fdr3, y del ligando útil dnrV bajo promotores cuidadosamente elegidos para equilibrar sus cantidades. También ajustaron las condiciones de cultivo y usaron resinas especiales para absorber intermedios tóxicos y pegajosos. En matraces de laboratorio y en un biorreactor de 20 litros, la mejor cepa diseñada produjo 336 miligramos de doxorrubicina por litro de cultivo con una relación 81:19 de doxorrubicina a danorubicina—un aumento de alrededor del 180% respecto a la cepa inicial y una mezcla de producto mucho más limpia.
Qué significa esto para el suministro futuro de fármacos contra el cáncer
Al diseccionar tanto el sistema de soporte eléctrico como la estructura 3D de una enzima clave, este trabajo explica por qué un microbio médicamente vital rinde por debajo de su capacidad al fabricar nuestra antraciclina más preciada. Emparejar DoxA con sus socios redox naturales, añadir una proteína auxiliar que se une al fármaco y reequilibrar la expresión génica convirtieron a un productor renuente en uno robusto. Aunque un ajuste adicional de la enzima podría acelerar aún más el paso químico final, el estudio ya acerca mucho la fabricación totalmente biológica de doxorrubicina a la realidad industrial. Para pacientes y sistemas sanitarios, estos avances podrían traducirse en un acceso más seguro, escalable y rentable a un fármaco de quimioterapia básico.
Cita: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
Palabras clave: producción de doxorrubicina, biosíntesis de antraciclinas, ingeniería de enzimas, fabricación microbiana de fármacos, citocromo P450