Clear Sky Science · es
La activación de la proteína quinasa C atípica impulsa la excreción intestinal de glucosa en la diabetes mellitus
Convertir el intestino en una válvula de azúcar
Las personas con diabetes conviven con un exceso de azúcar circulando en la sangre. Cirugías bariátricas como el bypass gástrico pueden normalizar la glucemia de forma sorprendentemente rápida, incluso antes de que se pierda mucho peso, pero cómo sucede esto ha sido un misterio. Este estudio revela una “válvula de azúcar” localizada en el intestino: un mecanismo por el que el intestino puede extraer glucosa de la sangre y expulsar parte de ella de nuevo al lumen intestinal, lo que sugiere un nuevo blanco farmacológico que podría imitar los beneficios de la cirugía sin necesidad de operarse.
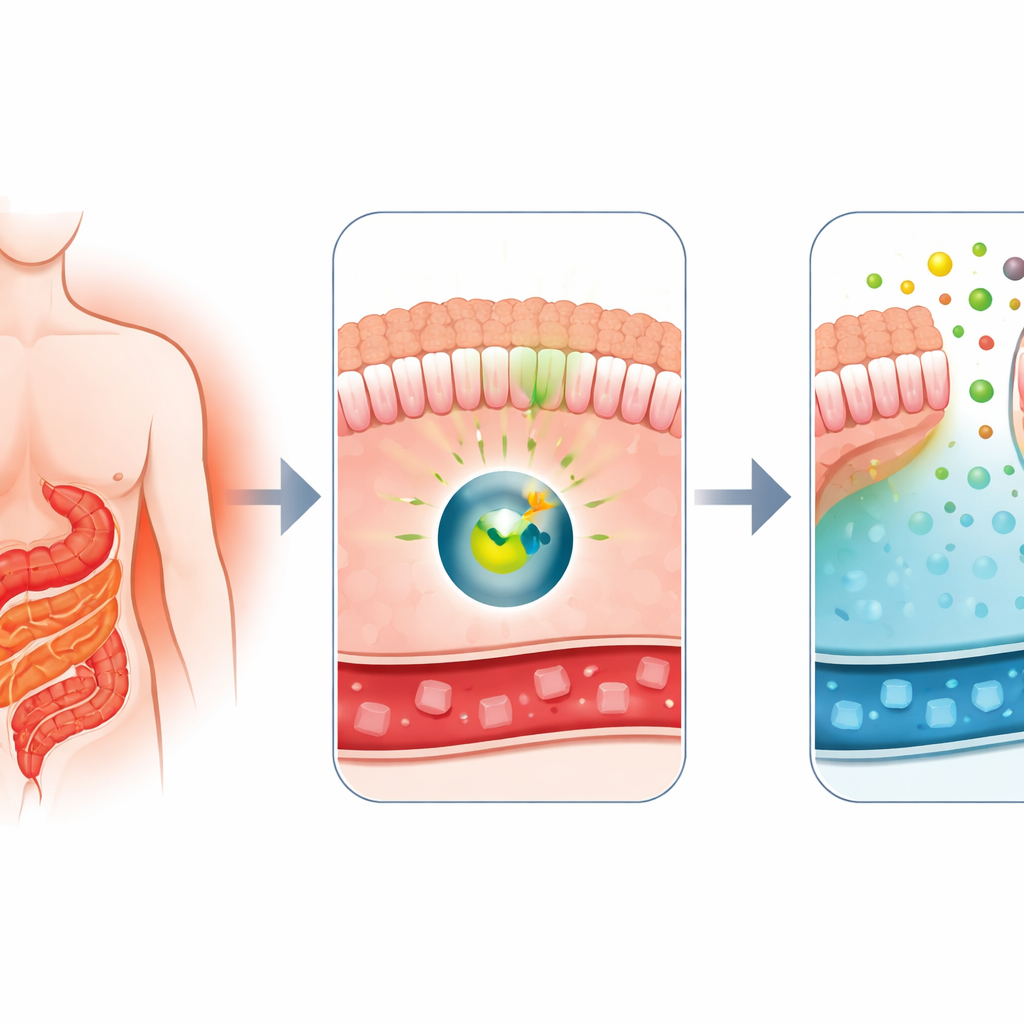
Por qué la cirugía cambia la glucosa en sangre tan deprisa
Los médicos saben desde hace tiempo que el bypass gástrico en Y de Roux, una cirugía común para perder peso, es también uno de los tratamientos más eficaces para la diabetes tipo 2. Poco después de la intervención, la glucemia de los pacientes suele mejorar de forma notable, incluso antes de una pérdida de peso apreciable. Trabajos previos de este grupo mostraron que, tras el bypass, partes del intestino delgado empiezan a comportarse como una esponja: absorben glucosa de la circulación y liberan parte de ella al interior del intestino. Ese comportamiento inusual, llamado excreción intestinal de glucosa, parecía depender de una proteína transportadora llamada GLUT1. La gran pregunta era: ¿qué interruptor molecular indica al intestino que se active en este modo de eliminación de azúcar?
Usar macrodatos para encontrar un interruptor molecular
Para buscar ese interruptor, los investigadores emplearon un sistema computacional de descubrimiento de fármacos basado en la base de datos Connectivity Map, que recoge cómo miles de compuestos alteran la actividad génica en células. Compararon los patrones de expresión génica de cinco situaciones en las que la excreción intestinal de glucosa es alta —incluyendo tejido de ratas operadas con bypass y células tratadas con una señal de crecimiento intestinal— con los patrones inducidos por fármacos conocidos. Una clase de compuestos destacó de forma consistente: activadores de la proteína quinasa C (PKC), una familia de enzimas que transmiten señales dentro de las células. Al profundizar, el equipo se centró en el subgrupo “atípico” de las PKC, en especial en una denominada PKCζ, cuya actividad en células intestinales coincidía más estrechamente con el estado tipo bypass que excreta glucosa.
La bomba de azúcar de las células intestinales en acción
Al estudiar células intestinales individuales mediante secuenciación de ARN unicelular, los autores hallaron que la cirugía de bypass incrementa tanto PKCζ como GLUT1 en células absorbentes específicas que recubren la porción distal del intestino delgado. En cultivos celulares y organoides intestinales humanos, aumentar artificialmente PKCζ o tratar con prostratina —un compuesto de origen vegetal que activa de forma segura estas PKC atípicas— promovió la translocación de GLUT1 a la superficie celular. Allí, GLUT1 actuó como una bomba bidireccional: extraía más glucosa del lado de la célula que mira a la sangre y permitió que el exceso de glucosa saliera hacia la luz intestinal. Es importante que este desvío de la glucosa no aceleró de forma significativa la propia combustión de azúcar de las células (glucólisis), lo que indica que el efecto principal fue la eliminación de glucosa, no una mayor producción de energía.
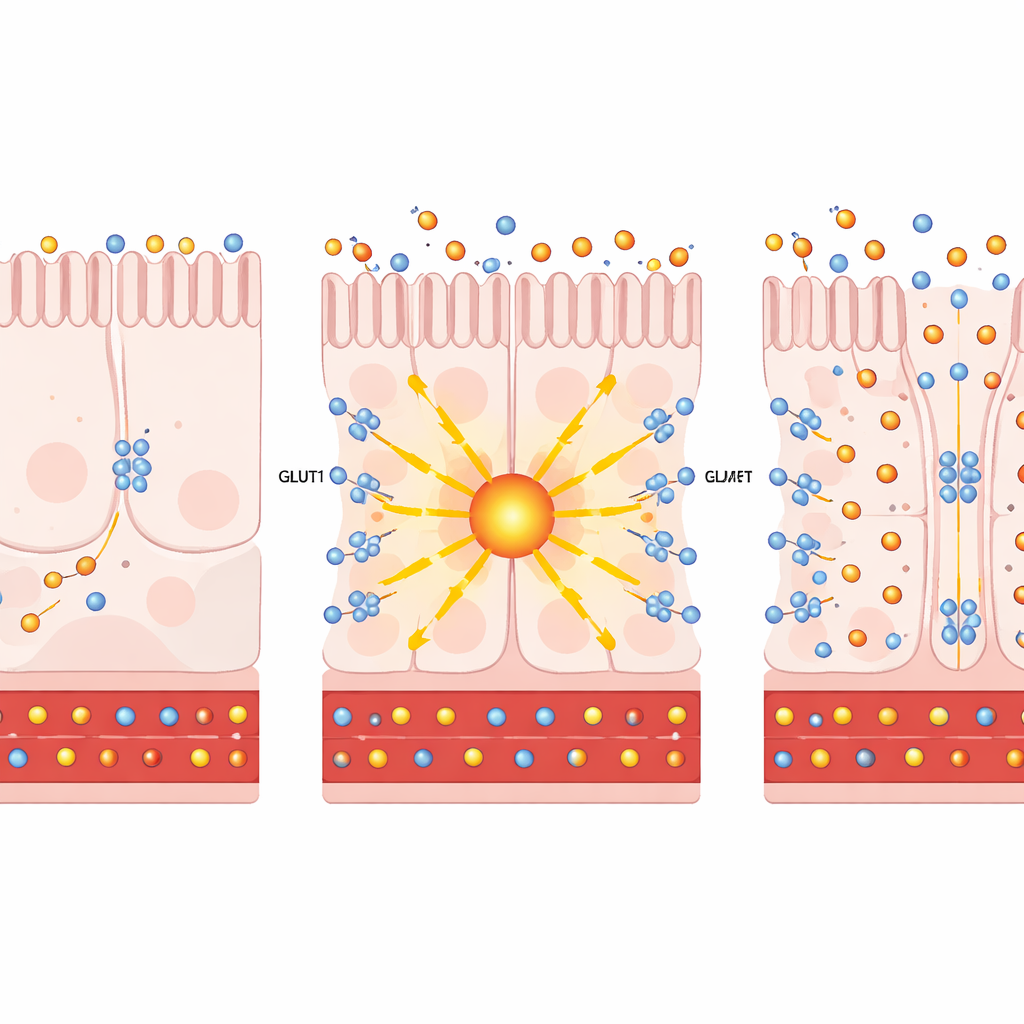
De las células a los ratones: imitar la cirugía sin bisturí
El equipo comprobó después si activar esta vía en animales vivos podía mejorar la diabetes. En ratones obesos e insulinorresistentes, la expresión adicional de PKCζ específicamente en el intestino condujo a una ganancia de peso más lenta, menor glucosa en ayunas y mejor tolerancia a la glucosa. Trazadores de azúcar radiactivos mostraron más captación de glucosa por el intestino distal y su paso al lumen intestinal. Un panorama similar apareció en modelos murinos diabéticos tratados con prostratina: ganaron menos peso, manejaron mejor las cargas de glucosa y desviaron más glucosa al tracto intestinal, todo ello sin cambios en los niveles de insulina, la ingesta de alimentos o la integridad de la barrera intestinal. En cortes de tejido, GLUT1 se observó tanto en el lado que mira a la sangre como en el que mira al lumen, perfectamente situado para extraer glucosa de la circulación y empujarla hacia el intestino.
Qué podría significar esto para la atención futura de la diabetes
Para un público general, el mensaje clave es que el intestino puede convertirse en una vía controlada de escape para el exceso de glucosa en sangre. Al activar una enzima específica dentro de las células intestinales —la PKC atípica— los investigadores lograron inducir que las células trasladen más transportadores GLUT1 a su superficie y se comporten como un desagüe reversible, extrayendo glucosa de la sangre y vertiendo parte de ella de nuevo al intestino. En ratones, esta eliminación de glucosa dirigida por el intestino mejoró la glucemia y limitó la ganancia de peso sin sobreestimular la insulina, modificar el apetito ni dañar el intestino. Aunque la prostratina y compuestos relacionados aún no están aprobados como fármacos para la diabetes, este trabajo apunta a la vía aPKC–GLUT1 como un objetivo prometedor para futuros medicamentos que podrían reproducir en parte los beneficios metabólicos del bypass gástrico sin necesidad de cirugía.
Cita: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
Palabras clave: excreción intestinal de glucosa, diabetes tipo 2, transportador GLUT1, proteína quinasa C atípica, prostratina