Clear Sky Science · es
Señal autocrina activada por MerTK y TGFβ1 regula la respuesta microglial a la neurodegeneración
Cómo el equipo de limpieza del cerebro moldea la enfermedad
Cuando las neuronas del cerebro y del nervio óptico mueren, dejan tras de sí un rastro de desechos. Células inmunitarias especializadas llamadas microglía actúan como el equipo de limpieza del cerebro, engullendo estos residuos. Pero las microglías hacen más que ordenar: su reacción puede proteger los circuitos nerviosos o agravar enfermedades como el Alzheimer. Este estudio desvela un circuito de auto‑comunicación oculto dentro de las microglías que se activa por los restos de fibras nerviosas moribundas y ayuda a determinar con qué intensidad estas células responden al daño.
Un disparador oculto en las fibras nerviosas moribundas
Para investigar este proceso, los investigadores utilizaron un modelo de ratón en el que se aplasta el nervio óptico, provocando la degeneración de las largas proyecciones de las neuronas oculares sin matar los cuerpos celulares. Esto aisla de forma limpia las consecuencias de la rotura de los axones. En la superficie de estas fibras en degeneración, una molécula grasa se gira hacia fuera, actuando como una señal de “cómeme” para las microglías cercanas. Esas señales son detectadas por un receptor en las microglías llamado MerTK, uno de una pequeña familia de proteínas que reconocen desechos. Al eliminar selectivamente MerTK en microglías, el equipo mostró que sin este receptor las microglías no montaban su respuesta habitual a la lesión: se dividían menos, se desplazaban menos y activaban menos genes vinculados al control del daño y a la inflamación.
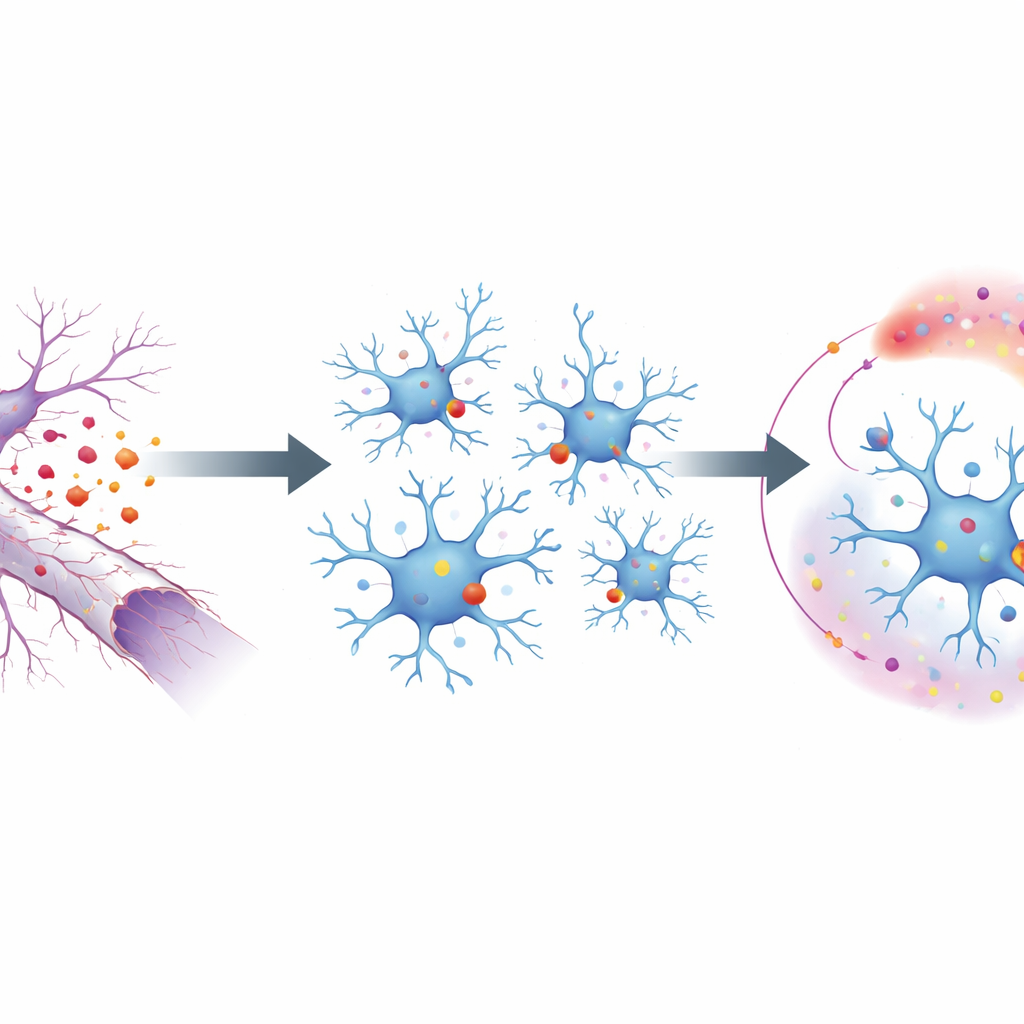
De la señal en la superficie a la reprogramación genética
Al observar el interior de las microglías, los científicos trazaron cómo la señal de MerTK en la membrana se convierte en cambios en la actividad génica. Encontraron que MerTK activa un relevo molecular llamado fosfolipasa C, que a su vez aumenta dos proteínas maestras en el núcleo, PU.1 e IRF8. Estos factores actúan como capataces en la línea de montaje microglial, encendiendo muchos genes necesarios para un estado activado. Mediante mapas de unión al ADN, el equipo descubrió que PU.1 e IRF8 se unen directamente a un sitio específico en el gen que codifica TGFβ1, una potente proteína señalizadora. Cuando ese sitio de unión se mutó de modo que los capataces ya no pudieran anclarse, las microglías en nervios lesionados dejaron de aumentar la producción de TGFβ1, aunque otras funciones basales permanecieron intactas.
Un circuito de retroalimentación en las microglías
La siguiente pregunta fue qué hace realmente TGFβ1 en este contexto. El estudio muestra que las microglías producen TGFβ1 y luego responden a él ellas mismas, formando un circuito autocrino, o de retroalimentación propia. Cuando TGFβ1 o sus receptores se eliminaron genéticamente solo en microglías, la lesión aún provocó la degeneración de los axones, pero las microglías dejaron de mostrar su programa completo de activación. Se proliferaron menos y expresaron menos genes de respuesta al daño y de inflamación, aunque muchos marcadores identitarios homeostáticos seguían suprimidos por otras señales. Una molécula clave aguas abajo de la señalización TGFβ, llamada SMAD2 fosforilada, apareció específicamente en los núcleos microgliales tras la lesión y desapareció en gran medida cuando TGFβ1 o sus receptores fueron eliminados, confirmando que el circuito de retroalimentación se rompió.
Del nervio óptico de ratón a cerebros con Alzheimer
Para evaluar si esta vía importa más allá de un modelo de lesión artificial, los autores examinaron un modelo de ratón ampliamente usado de la enfermedad de Alzheimer. En estos animales, las microglías agrupadas alrededor de las placas amiloides mostraron altos niveles de PU.1, IRF8, TGFβ1 y señalización TGFβ activada, eco de los hallazgos en el nervio óptico. El equipo recurrió luego a datos humanos de secuenciación de ARN de núcleos individuales de tejido cerebral de pacientes con Alzheimer. Allí, las microglías destacaban como las principales células que expresaban las contrapartes humanas de MerTK, PU.1, IRF8 y TGFB1. En secciones cerebrales postmortem de pacientes, las microglías también mostraron fuertes signos de señalización TGFβ activa, en contraste con tejido de donantes controles. En conjunto, estas observaciones sostienen que el mismo circuito de auto‑comunicación opera en la enfermedad humana.
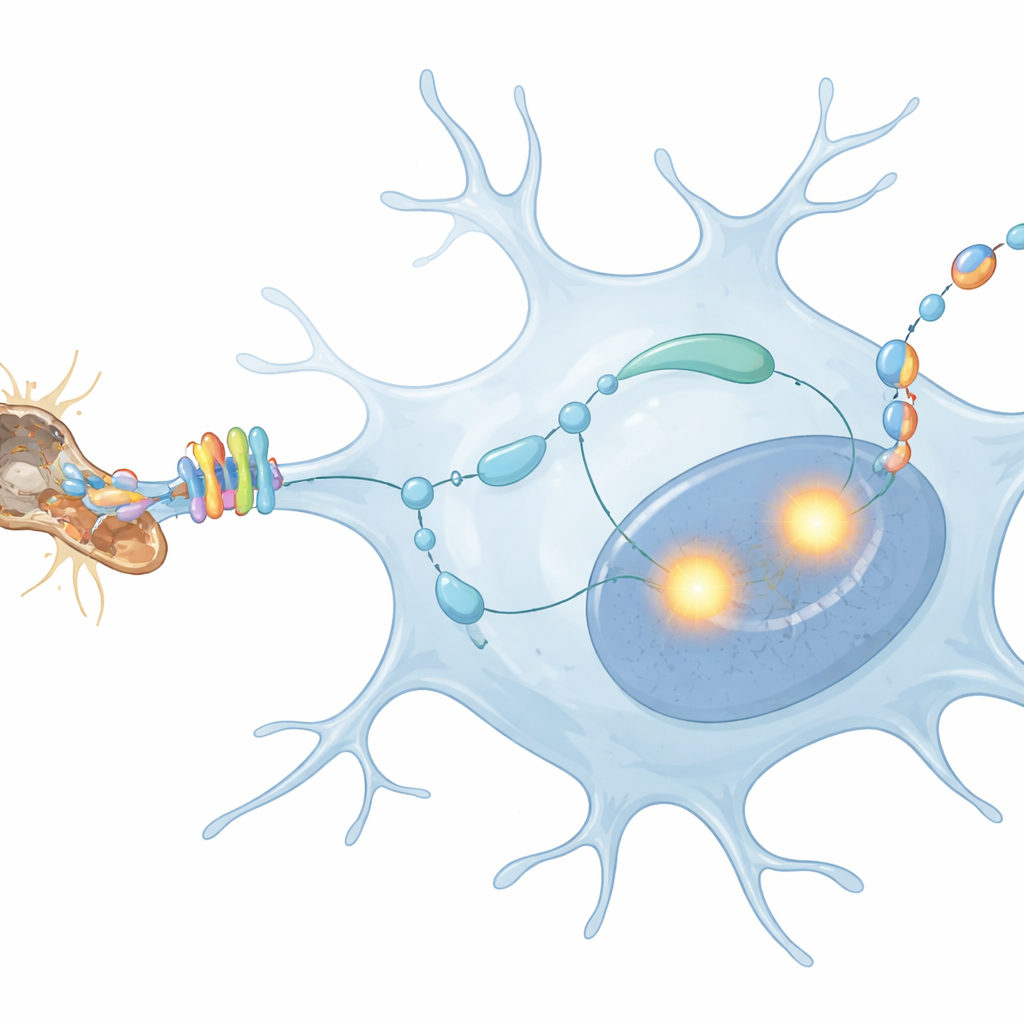
Por qué esta auto‑conversación importa para la salud cerebral
Este trabajo revela una cadena de eventos en la que los desechos de fibras nerviosas degeneradas activan MerTK en las microglías, que a su vez aumentan PU.1 e IRF8, los cuales impulsan a las microglías a producir TGFβ1 que se retroalimenta sobre ellas mismas. Esta auto‑conversación afina y sostiene su respuesta a la neurodegeneración. Para el lector general, el mensaje clave es que las células limpiadoras del cerebro no son meros operarios pasivos; escuchan activamente sus propias señales, y este ciclo de retroalimentación puede influir en si sus acciones protegen a las neuronas o aceleran enfermedades como el Alzheimer. Comprender y, posiblemente, ajustar este circuito podría abrir nuevas vías para moderar la inflamación nociva a la vez que se preserva la limpieza beneficiosa que realizan las microglías.
Cita: Huang, Y., Deng, Z., Zhou, Z. et al. MerTK-triggered TGFβ1 autocrine signal regulates microglial response to neurodegeneration. Nat Commun 17, 2312 (2026). https://doi.org/10.1038/s41467-026-69189-3
Palabras clave: microglía, neurodegeneración, enfermedad de Alzheimer, inflamación cerebral, señalización TGF-beta