Clear Sky Science · es
Determinante molecular de la dependencia a bajo voltaje de la inactivación de Nav1.7 humana revelado por un inhibidor selectivo de Nav1.7 basado en eficacia
Bajando el volumen de las señales de dolor
¿Por qué algunas personas sienten un dolor insoportable ante un toque ligero, mientras que otras apenas sienten dolor? Gran parte de la respuesta reside en diminutas puertas proteicas en nuestras neuronas que controlan las señales eléctricas. Este estudio desvela cómo una sutileza estructural en una de esas puertas, llamada Nav1.7, la hace especialmente importante para desencadenar el dolor —y cómo un compuesto natural, Uvarigranol D, puede cerrarla selectivamente. El trabajo señala una nueva estrategia para diseñar analgésicos que silencien nervios de dolor hiperactivos sin frenar el corazón ni nublar el cerebro. 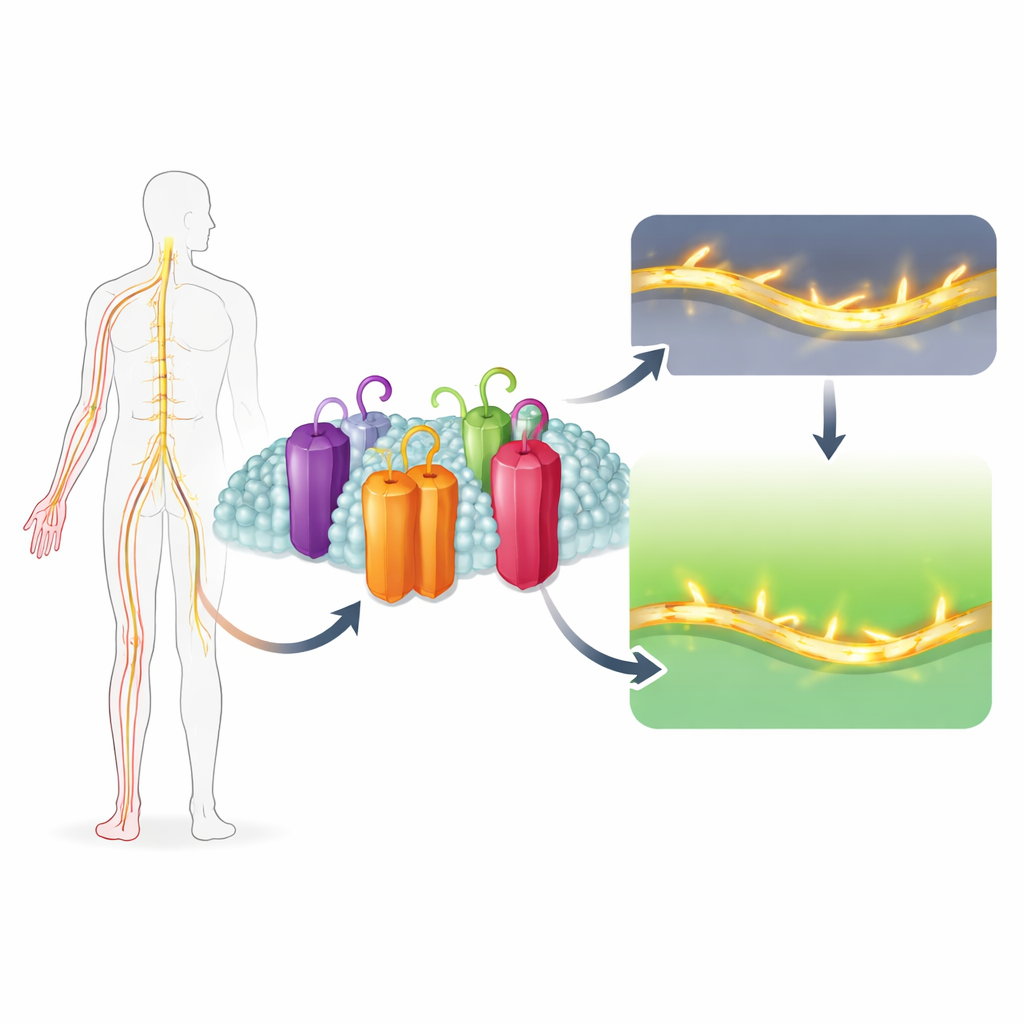
Un guardián especial del dolor
Nuestras neuronas generan impulsos eléctricos usando canales de sodio, poros microscópicos que se abren brevemente para dejar entrar iones de sodio con carga positiva. Hay nueve versiones principales de estos canales en humanos, cada una ajustada a tejidos distintos como el cerebro, el músculo, el corazón o las fibras que detectan dolor. Nav1.7 es la versión abundante en las fibras periféricas del dolor. Es inusual porque puede activarse y desactivarse a voltajes más bajos que sus parientes, lo que le permite responder incluso a pequeños empujones en el voltaje. Esto convierte a Nav1.7 en un potente amplificador de señales débiles que provocan dolor. Estudios genéticos muestran que la hiperactividad de Nav1.7 causa síndromes de dolor hereditario severo, mientras que la ausencia total de función de Nav1.7 impide sentir dolor por completo.
Encontrando un bloqueador selectivo para el dolor
Los desarrolladores de fármacos hace tiempo que intentan dirigir tratamientos al Nav1.7 para tratar el dolor crónico, pero se parece mucho a otros canales de sodio vitales para el latido cardiaco y la función cerebral. La mayoría de los fármacos experimentales se unen a varios tipos de canales, provocando efectos secundarios o fracasando en ensayos clínicos. Los investigadores examinaron más de 1.500 compuestos naturales usando un ensayo celular que detecta cambios en el voltaje de la membrana. Identificaron una familia de moléculas de la planta Uvaria grandiflora, centrando la atención en una llamada Uvarigranol D (UGD). UGD atenuó las corrientes de sodio en varios tipos de canal, pero silenció casi por completo a Nav1.7 mientras que solo bloqueó en torno a la mitad a otros canales de sodio incluso a dosis altas. Esto indica que su selectividad no proviene de una unión más fuerte, sino de un efecto mucho más potente una vez ligada. 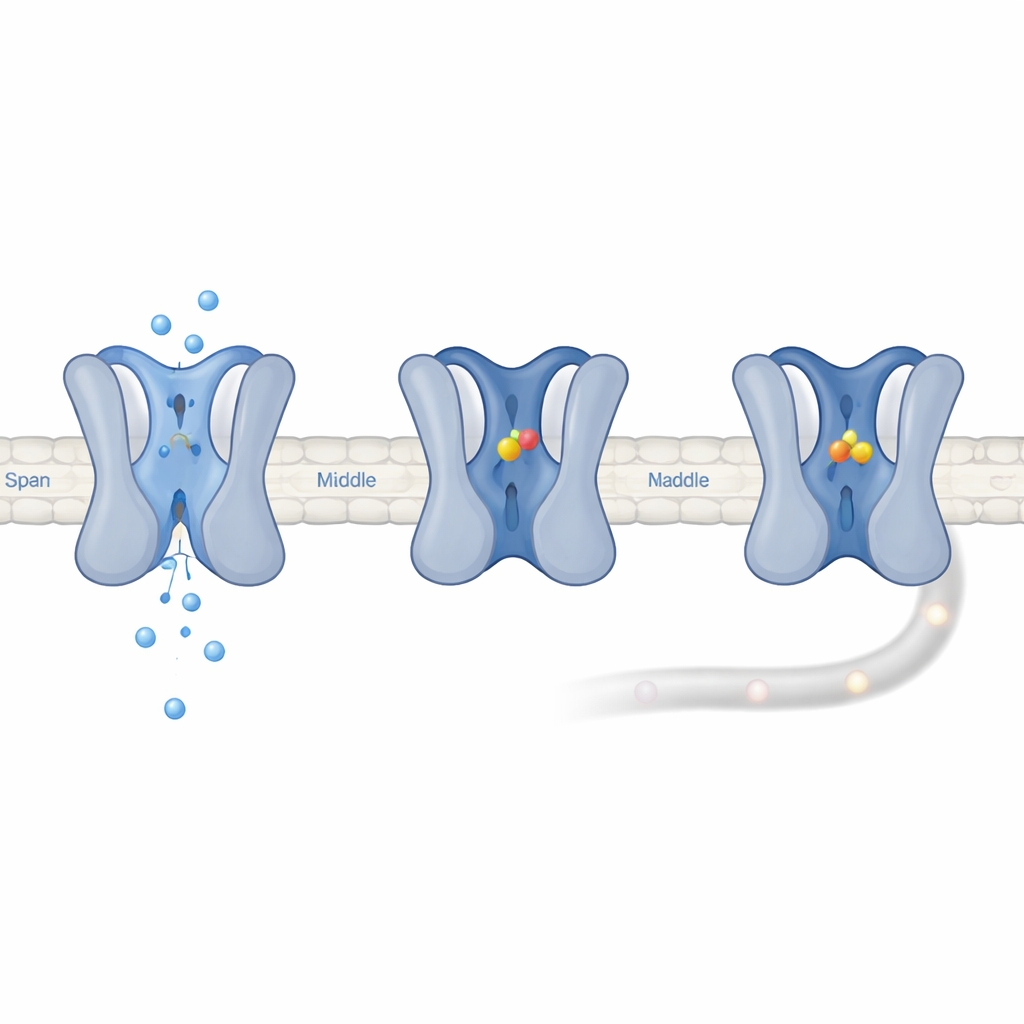
Un cambio del tamaño de un átomo hace única a Nav1.7
Para entender por qué UGD es tan efectivo sobre Nav1.7, el equipo construyó canales quiméricos que intercambiaban fragmentos entre Nav1.7 y un canal cerebral estrechamente relacionado, Nav1.2. Esto señaló una pequeña región cerca de la boca externa del poro, entre dos segmentos estructurales llamados S5 y S6 en el dominio III, como el determinante clave del poder bloqueador completo de UGD. La comparación de secuencias de aminoácidos reveló que solo Nav1.7 tiene una treonina en la posición 1398, mientras que todos los demás canales de sodio humanos llevan allí una metionina más voluminosa. Cuando los investigadores reemplazaron la treonina de Nav1.7 por metionina, UGD ya no pudo cerrar completamente el canal; sustituir la metionina por treonina en Nav1.2 hizo que ese canal se comportara como Nav1.7. Esta única sustitución también desplazó los voltajes a los que los canales se activan y se inactivan: la treonina hace que el canal se abra e inactive a voltajes más negativos y lo haga más rápidamente, propiedades que favorecen que Nav1.7 esté en un estado no reposado incluso cerca del voltaje de reposo normal de las neuronas del dolor.
Bloqueando el canal en un modo inactivo
Registros eléctricos mostraron que UGD no se une a Nav1.7 cuando está cerrada o brevemente abierta. En cambio, prefiere canales que han entrado en un estado de “inactivación lenta” de larga duración, en el que el poro está cerrado y tarda cientos de milisegundos o más en recuperarse. Cuando UGD está presente, los canales tardan alrededor de diez veces más en escapar de ese estado, lo que significa que UGD lo estabiliza. Simulaciones por ordenador sugirieron que UGD se aloja en un bolsillo formado donde un lazo del dominio III se encuentra con una hélice del dominio IV, estableciendo contactos clave con cinco aminoácidos. Mutar cualquiera de estos residuos debilitó el efecto de UGD, confirmando la importancia del bolsillo. Debido a que la estructura rica en treonina de Nav1.7 la hace entrar en estados inactivados a voltajes más bajos, más canales de Nav1.7 están en el estado que UGD prefiere unir, lo que explica por qué Nav1.7 queda funcionalmente mucho más suprimida que sus parientes aunque la afinidad de unión sea similar.
De los poros iónicos al alivio del dolor
En última instancia, lo que importa es cómo estos eventos moleculares influyen en células reales. En neuronas sensibles al dolor de la raíz dorsal de rata, UGD redujo drásticamente el número de potenciales de acción —los picos rápidos de voltaje que transmiten información de dolor— y finalmente los detuvo por completo a concentraciones micromolares bajas y submicromolares. En contraste, las células similares a cardiomiocitos humanas derivadas de células madre, que usan principalmente otro canal de sodio (Nav1.5) y tienen un potencial de reposo algo más bajo, fueron unas 60 veces menos sensibles. Esto sugiere que un bloqueador “selectivo por eficacia” como UGD puede atenuar las vías del dolor mucho más que los tejidos excitables cardíacos u otros simplemente por la frecuencia con la que Nav1.7 permanece en su estado inactivado favorecido por el fármaco.
Qué significa esto para futuros tratamientos del dolor
El estudio revela que un pequeño detalle estructural —una única treonina— subyace al comportamiento de bajo voltaje especial de Nav1.7 y a su capacidad para generar “corrientes umbral”, las señales diminutas que deciden si una neurona del dolor disparará. Al unirse y estabilizar la forma inactivada de este canal, UGD explota esa tendencia intrínseca y suprime Nav1.7 mucho más fuertemente que otros canales de sodio. Para un público general, la conclusión es que los autores han cartografiado un punto débil preciso en el guardián del dolor del cuerpo y han mostrado una forma de presionarlo sin perturbar en gran medida los canales del corazón o del cerebro. Este hallazgo abre una vía para diseñar nuevos analgésicos que calmen nervios de dolor hiperactivos apuntando al comportamiento voltaje-dependiente y al estado del canal, en lugar de perseguir únicamente una unión más fuerte a Nav1.7.
Cita: Zhao, F., Xi, C., Li, J. et al. Molecular determinant of low-voltage dependence of human Nav1.7 inactivation revealed by efficacy-based Nav1.7 selective inhibitor. Nat Commun 17, 2559 (2026). https://doi.org/10.1038/s41467-026-69184-8
Palabras clave: canal de sodio Nav1.7, dolor crónico, Uvarigranol D, inhibición dependiente del estado, canales de sodio dependientes de voltaje