Clear Sky Science · es
El mecanismo de bombeo de Na+ impulsado por redox en la NADH-quinona oxidoreductasa de Vibrio cholerae depende de cambios conformacionales dinámicos
Cómo la central energética del cólera se convirtió en un objetivo farmacológico
La bacteria que causa el cólera, Vibrio cholerae, sobrevive y se reproduce gracias al funcionamiento de una pequeña central molecular en su membrana celular. Este estudio revela, con un detalle sin precedentes, cómo uno de sus motores clave—una enzima llamada Na⁺-NQR—cambia de forma mientras bombea iones sodio fuera de la célula. Comprender esta maquinaria molecular no solo satisface la curiosidad básica sobre cómo la vida convierte los alimentos en energía utilizable, sino que también señala nuevas formas de diseñar antibióticos que inhabiliten bacterias dañinas sin afectar a las células humanas.
Un motor bacteriano impulsado por sodio
Muchas bacterias marinas y patógenas dependen de Na⁺-NQR como el primer paso en su cadena respiratoria, la serie de reacciones que extrae energía de los nutrientes. Na⁺-NQR se ubica en la membrana interna y toma electrones de una molécula combustible llamada NADH, transfiriéndolos a lo largo de una cadena de moléculas “auxiliares” coloreadas (llamadas cofactores) hasta la quinona, otra pequeña molécula integrada en la membrana. A medida que fluyen los electrones, la enzima utiliza esa energía para empujar iones sodio (Na⁺) desde el interior de la célula hacia el exterior, creando un gradiente de sodio. Este gradiente es como una batería cargada: impulsa el motor flagelar bacteriano para nadar, ayuda a sintetizar ATP (la moneda energética de la célula) y promueve la captación de nutrientes y la expulsión de fármacos. Dado que Na⁺-NQR existe solo en bacterias y difiere mucho de la enzima relacionada en nuestras mitocondrias, constituye un objetivo atractivo para antibióticos altamente selectivos.
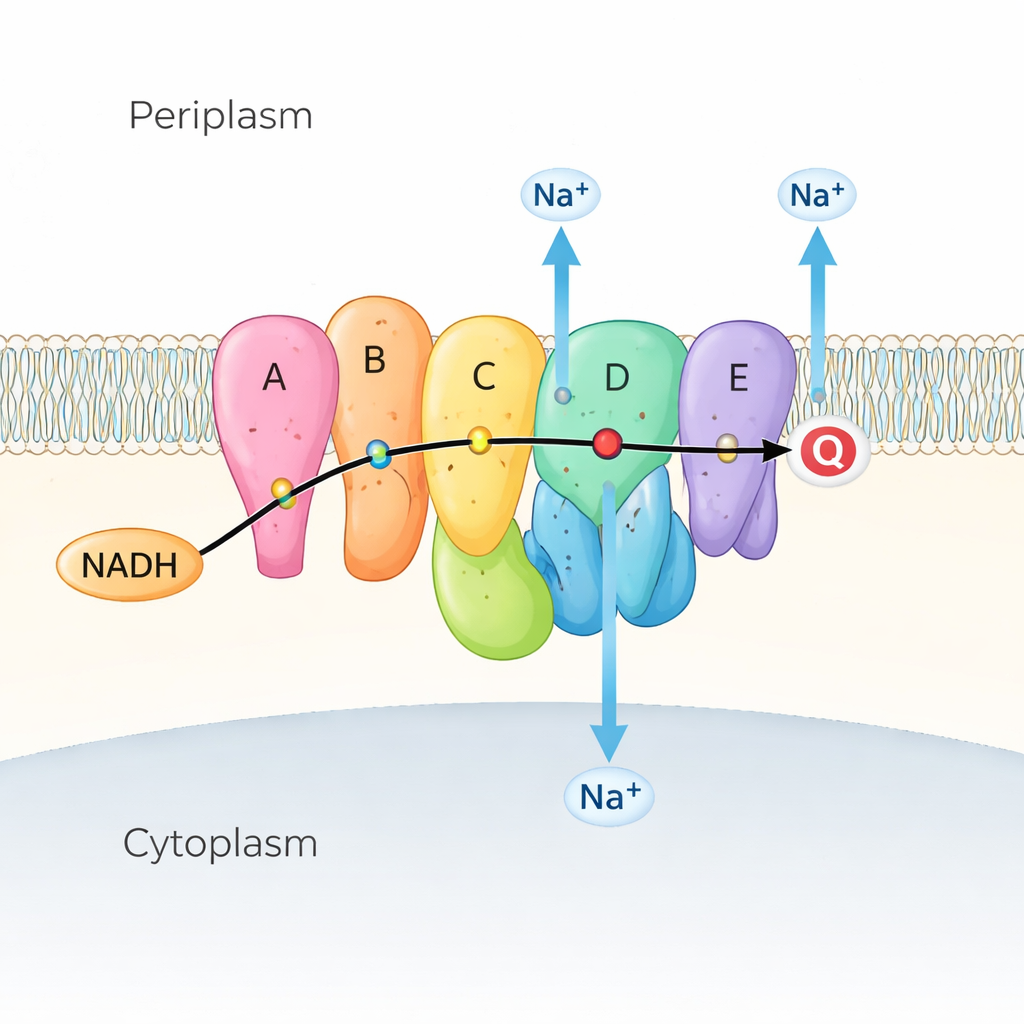
Observando la máquina en movimiento
Las instantáneas anteriores obtenidas por rayos X y crio-microscopía electrónica mostraban dónde se sitúan las subunidades y los cofactores de Na⁺-NQR, pero también revelaron un rompecabezas: algunos saltos críticos de electrones estaban demasiado separados para que los electrones se movieran eficientemente a menos que la proteína cambiara de forma. Los autores abordaron esto capturando Na⁺-NQR en muchas condiciones ligeramente distintas. Usaron mutantes que eliminan cofactores específicos, fármacos que estancan la reacción en etapas particulares y soluciones con y sin sodio. Con crio-EM de alta resolución y análisis de imagen avanzado, pudieron separar y reconstruir múltiples conformaciones de la misma enzima, transformando efectivamente instantáneas estáticas en una película de su ciclo de trabajo.
Un brazo flexible y una pinza móvil
Un hallazgo clave involucra una subunidad citoplasmática flexible, NqrF, que porta dos cofactores transportadores de electrones. El equipo identificó tres posiciones para su dominio “tipo ferredoxina”, apodadas los estados “arriba”, “medio” y “abajo”. En el raro pero crucial estado “abajo”, este pequeño dominio oscila hacia un bolsillo formado por dos subunidades de membrana, NqrD y NqrE, acercando su clúster hierro-azufre lo suficiente como para transferir un electrón. Mientras tanto, una subunidad periplásmica (externa) llamada NqrC se comporta como una pinza móvil. En una conformación (“estable”), se acopla contra otra subunidad de membrana, NqrB, posicionada para transferir electrones hacia el aceptor quinona final. En una segunda conformación (“desplazada”), NqrC se mueve hacia NqrD/E, acercando su cofactor flavínico para aceptar un electrón del centro hierro-azufre. Estos movimientos muestran que NqrF y NqrC actúan como mensajeros dinámicos, salvando grandes distancias en la cadena de cofactores.
Cómo los cambios de forma bombean sodio
El corazón de la bomba de sodio reside en las subunidades emparejadas NqrD y NqrE, que forman un haz central de hélices transmembrana. Usando tanto estructuras como simulaciones de dinámica molecular a nivel atómico, los autores muestran que cuando el clúster hierro-azufre en NqrD/E se reduce (gana un electrón), crea un sitio cargado negativamente que atrae un ion Na⁺ y algunas moléculas de agua desde el citoplasma, formando un bolsillo de unión transitorio. Aminoácidos hidrófobos por encima y por debajo de este bolsillo actúan como compuertas internas y externas, controlando el acceso al ion. Cuando NqrD/E cambian de una forma “abierta hacia dentro” a una “abierta hacia fuera”, el Na⁺ se desplaza hacia el lado periplásmico y finalmente se libera a medida que el clúster hierro-azufre se reoxida. Las simulaciones muestran al Na⁺ permaneciendo parcialmente hidratado pero sin encontrar nunca un túnel continuo lleno de agua, lo que sugiere que la enzima está sellada de forma hermética contra fugas indeseadas de protones.
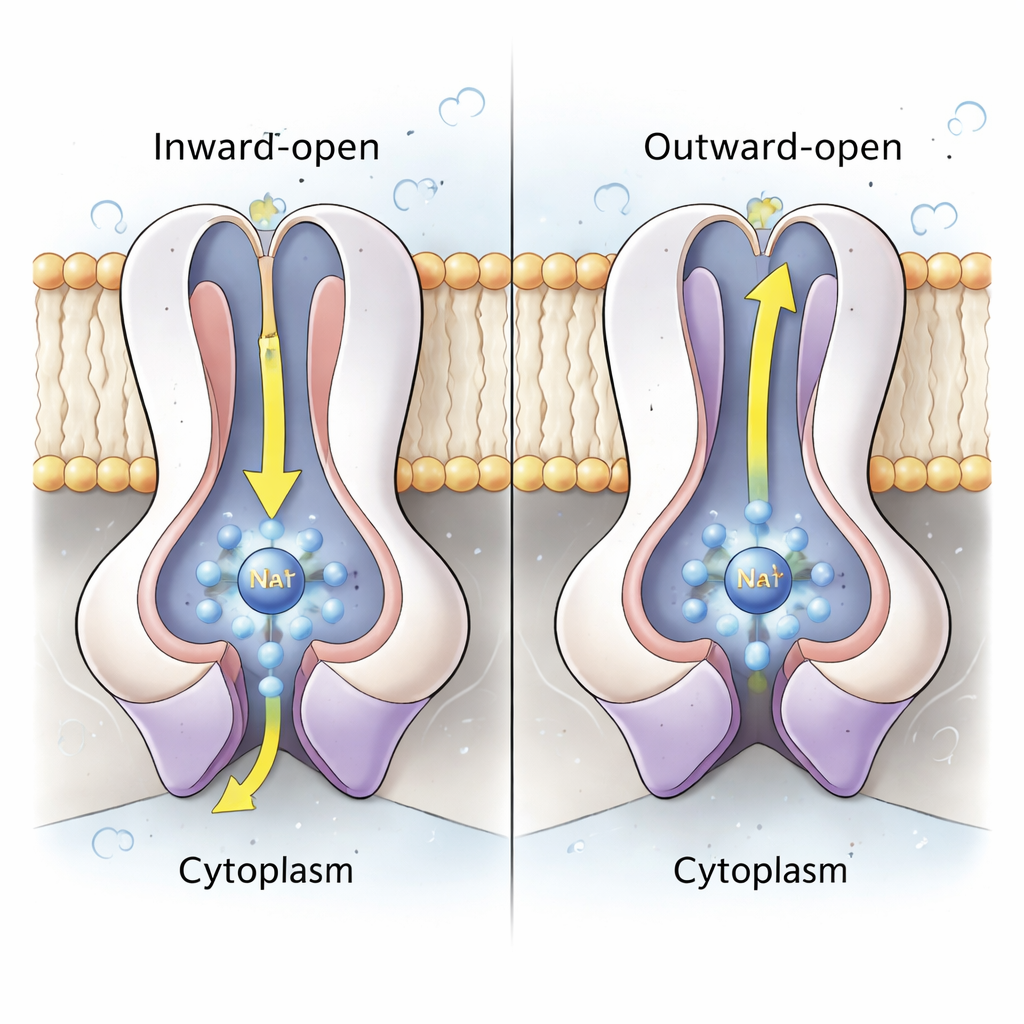
Un ciclo coordinado que asegura la dirección
Al combinar todos sus estados estructurales y las simulaciones, los investigadores proponen un ciclo de seis pasos. Primero, NADH se une y dona electrones a NqrF, que a su vez entrega un electrón a NqrD/E, desencadenando la captación de Na⁺ desde el citoplasma y cargando el bolsillo central. El conmutador conformacional resultante de NqrD/E a la forma abierta hacia fuera expulsa el Na⁺ hacia la periplasma y favorece que NqrC se coloque para aceptar el electrón. Los pasos subsiguientes transfieren electrones hacia los cofactores flavina y riboflavina y, finalmente, a la quinona, que debe recibir dos electrones para convertirse en quinol. Es importante que los mismos cambios de forma que desplazan el Na⁺ también aflojan y tensan alternativamente a NqrF y NqrC, haciendo probable el flujo electrónico hacia adelante solo cuando el Na⁺ se está bombeando hacia afuera y desalentando el retroceso. Este acoplamiento ayuda a la enzima a bombear Na⁺ en contra de un gradiente existente, manteniendo la “batería” bacteriana cargada.
Por qué esto importa para la medicina y la biología
Para un no especialista, este trabajo muestra cómo la vida construye máquinas exquisitamente coreografiadas a partir de proteínas, donde pequeños cambios en la carga desencadenan grandes movimientos útiles. Para la investigación en enfermedades infecciosas, aclara que la translocación de Na⁺ en Na⁺-NQR ocurre principalmente a través del núcleo NqrD/E, no por la subunidad NqrB sospechada anteriormente. Esa visión refina dónde deberían unirse futuros fármacos para interrumpir mejor el motor que alimenta a Vibrio cholerae y a otros patógenos, preservando las enzimas humanas. Más ampliamente, el estudio proporciona un plano estructural de cómo las reacciones redox pueden estar conectadas al bombeo de iones—un principio de diseño que la naturaleza reutiliza en muchas formas de maquinaria bioenergética.
Cita: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
Palabras clave: bomba de sodio, respiración bacteriana, Na+-NQR, crio-EM, blancos antibióticos