Clear Sky Science · es
Un sistema sintético para piroptosis sensible al ARN basado en la nucleasa-proteasa CRISPR tipo III-E
Convertir explosiones letales de células en herramientas dirigidas
Nuestros cuerpos a veces se defienden haciendo que células infectadas o dañadas exploten en una especie de autodestrucción inflamatoria. Esta explosión no solo elimina células peligrosas, sino que además convoca al sistema inmunitario. El nuevo estudio presenta un circuito génico sintético, llamado DAMAGE, que puede leer los mensajeros de ARN dentro de una célula y decidir si esa célula debe ser destruida. Al conectar un sistema de defensa microbiano con la propia maquinaria de muerte celular humana, los autores muestran una forma de eliminar selectivamente células infectadas por virus, cancerosas o envejecidas, mientras se preservan las vecinas sanas. 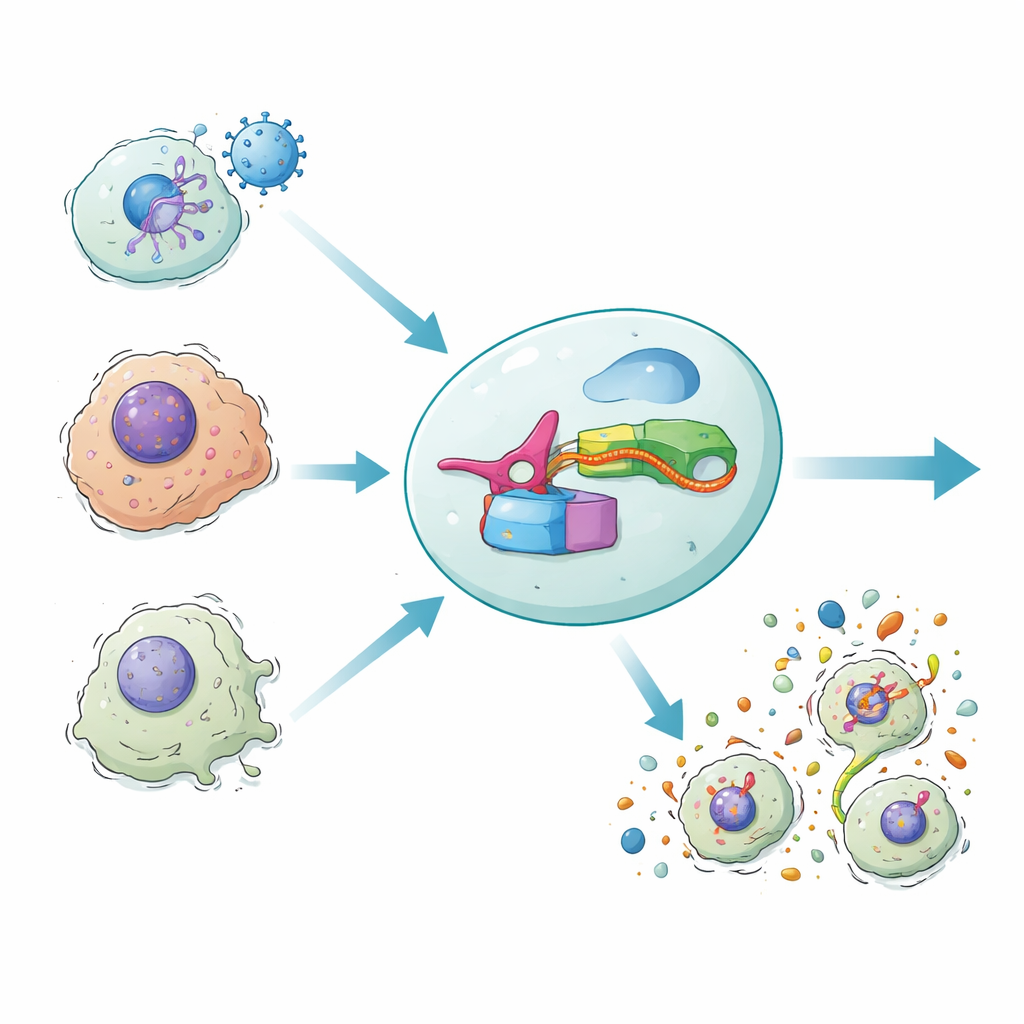
Cómo las células normalmente se hacen estallar
En la muerte celular inflamatoria, una familia de proteínas conocidas como gasderminas permanece dentro de las células como cargas preparadas. Cada gasdermina tiene una mitad delantera “asesina” que puede perforar membranas celulares y una mitad trasera que actúa como “tapón de seguridad” para mantener a raya al asesino. Cuando los sensores inmunitarios detectan peligro, enzimas cortan las gasderminas en dos, liberando la mitad delantera para ensamblar poros en la membrana. La célula se hincha, estalla y expulsa señales de alarma que reclutan células inmunes. Esta respuesta potente ayuda a combatir infecciones y tumores, pero su red de control natural es intrincada y difícil de reconfigurar para terapias.
Tomando prestadas defensas bacterianas para leer ARN
Las bacterias han desarrollado módulos de defensa compactos conocidos hoy gracias a la tecnología CRISPR. Uno de ellos, el sistema tipo III-E, utiliza una proteína llamada Cas7‑11 que puede unirse a secuencias específicas de ARN con la ayuda de un ARN guía corto. Cuando Cas7‑11 encuentra un ARN objetivo coincidente, activa una enzima compañera, Csx29, que corta una proteína asociada, Csx30. Los autores se dieron cuenta de que Csx30 podría actuar como una “bisagra” personalizable entre dos partes proteicas. Fusionaron esta bisagra entre las mitades asesina y de seguridad de gasderminas humanas, creando ejecutores artificiales que solo se separan cuando el sensor tipo CRISPR detecta su ARN elegido dentro de la célula.
Un interruptor de muerte programable para células enfermas
Este diseño, denominado DAMAGE (por Death Manipulation Gene), se construye a partir de cinco piezas: el sensor Cas7‑11, el cortador Csx29, una fusión gasdermina–Csx30, un ARN guía y el ARN objetivo dentro de la célula. Cuando aparece el mensaje de ARN correcto, Cas7‑11 se une a él, activa a Csx29 y Csx29 corta la bisagra Csx30 en la proteína de fusión. La mitad asesina de la gasdermina se libera, perfora la membrana y la célula muere en una explosión inflamatoria. Simplemente cambiando el ARN guía, el equipo redirigió DAMAGE a distintos blancos celulares. Demostraron que podía reconocer ARN de virus respiratorio sincitial, ARN de papilomavirus humano de alto riesgo en células de cáncer cervical y varias mutaciones oncogénicas de KRAS que difieren del ARN normal en una sola letra. En cada caso, las células que portaban el ARN sospechoso fueron eliminadas selectivamente, mientras las células control cercanas permanecieron intactas. 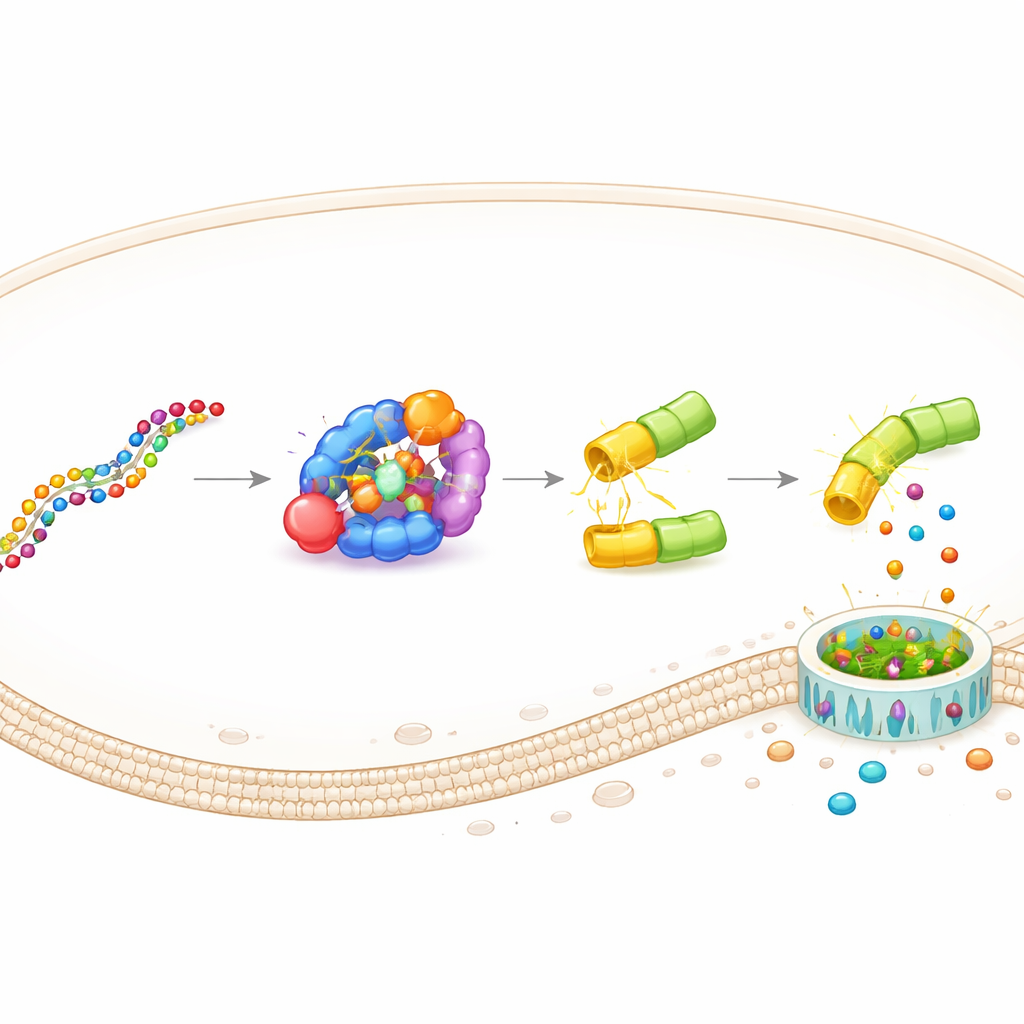
Apuntando a células envejecidas
Los investigadores también preguntaron si DAMAGE podría localizar células senescentes—células envejecidas o estresadas que dejan de dividirse pero se acumulan en los tejidos y contribuyen a la fragilidad y a enfermedades crónicas. Esas células suelen aumentar la producción de dos proteínas reguladoras, p16 y p21. Programando guías contra los ARN de p16 y p21, el equipo creó una versión llamada DAMAGE‑Aging. Este circuito mató células con niveles altos de estos mensajeros mientras perdonaba a células en las que p16 había sido eliminado genéticamente, confirmando que el sistema lee la abundancia de ARN en tiempo real y no cambios fijos en el ADN. Tratamientos farmacológicos que elevaron p16 o p21 hicieron a las células más vulnerables a este autodestrucción dirigida.
Empaquetando el sistema para futuras terapias
Para avanzar hacia un uso práctico, los autores comprimieron las numerosas partes de ADN de DAMAGE en un constructo simplificado, DAMAGE‑Plus, y demostraron que seguía funcionando de forma fiable. Luego transcribieron este constructo en ARNm sintético, lo empaquetaron en nanopartículas lipídicas similares a las usadas en las vacunas contra la COVID-19 y lo administraron a células en cultivo. La versión en ARNm ensambló con éxito el circuito y desencadenó la muerte inflamatoria dirigida en células que portaban ARN viral o relacionado con cáncer. Aunque el sistema global sigue siendo voluminoso y solo se ha probado en líneas celulares, estos resultados sugieren que la eliminación celular programable guiada por ARN podría algún día desplegarse mediante formulaciones inyectables de ARNm.
Una nueva forma de leer y reaccionar ante los mensajes celulares
En términos sencillos, DAMAGE es un portero molecular que revisa la “identificación” de ARN interna de cada célula y expulsa solo aquellas que parecen peligrosas—infectadas por virus, con mutaciones o senescentes—forzándolas a una forma explosiva de autodestrucción. El trabajo demuestra que sensores bacterianos de ARN pueden acoplarse a la maquinaria humana de muerte celular con alta precisión, incluso distinguiendo diferencias de una sola letra en los mensajes genéticos. Si bien queda mucha ingeniería por delante antes de que un sistema así pueda usarse con seguridad en animales o personas, traza una estrategia potente: leer el bullicio de ARN en vivo dentro de las células y traducirlo directamente en decisiones de vida o muerte.
Cita: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
Palabras clave: piroptosis, CRISPR, terapia dirigida al ARN, inmunoterapia contra el cáncer, senescencia celular