Clear Sky Science · es
hnRNPM coopera con BCAS2 para modular el empalme alternativo durante el desarrollo del ovocito
Por qué importa la calidad del ovocito
Cada vida humana comienza con una única célula ovoide, y sin embargo los científicos siguen descubriendo cómo estas células inusualmente grandes se preparan para el momento de la fertilización. Mucho antes de que lleguen los espermatozoides, los ovocitos en crecimiento acumulan miles de mensajeros de ARN que guiarán su maduración y los primeros días del desarrollo embrionario. Este estudio revela cómo una proteína poco conocida, que actúa junto a una socia, edita con precisión esos mensajeros en los óvulos de ratón —y qué ocurre cuando ese sistema de edición falla.
Guardianes de los mensajes genéticos
Los ovocitos crecen en el ovario durante semanas mientras su ADN permanece en gran medida silencioso. Durante ese tiempo, acumulan una vasta biblioteca de mensajes maternales de ARN copiados del genoma con anterioridad. Estos mensajes deben recortarse y ensamblarse de distintas maneras, un proceso llamado empalme alternativo, para producir la combinación adecuada de variantes proteicas en los momentos precisos. Los autores se centraron en una proteína denominada hnRNPM, parte de una gran familia que se une al ARN, y en su socia BCAS2, ambas abundantes en el sistema reproductor femenino. Trabajos previos sugerían que estas proteínas se unen a muchos ARN en los ovocitos, pero su papel preciso en la fertilidad seguía sin aclararse.
Qué sale mal sin este editor
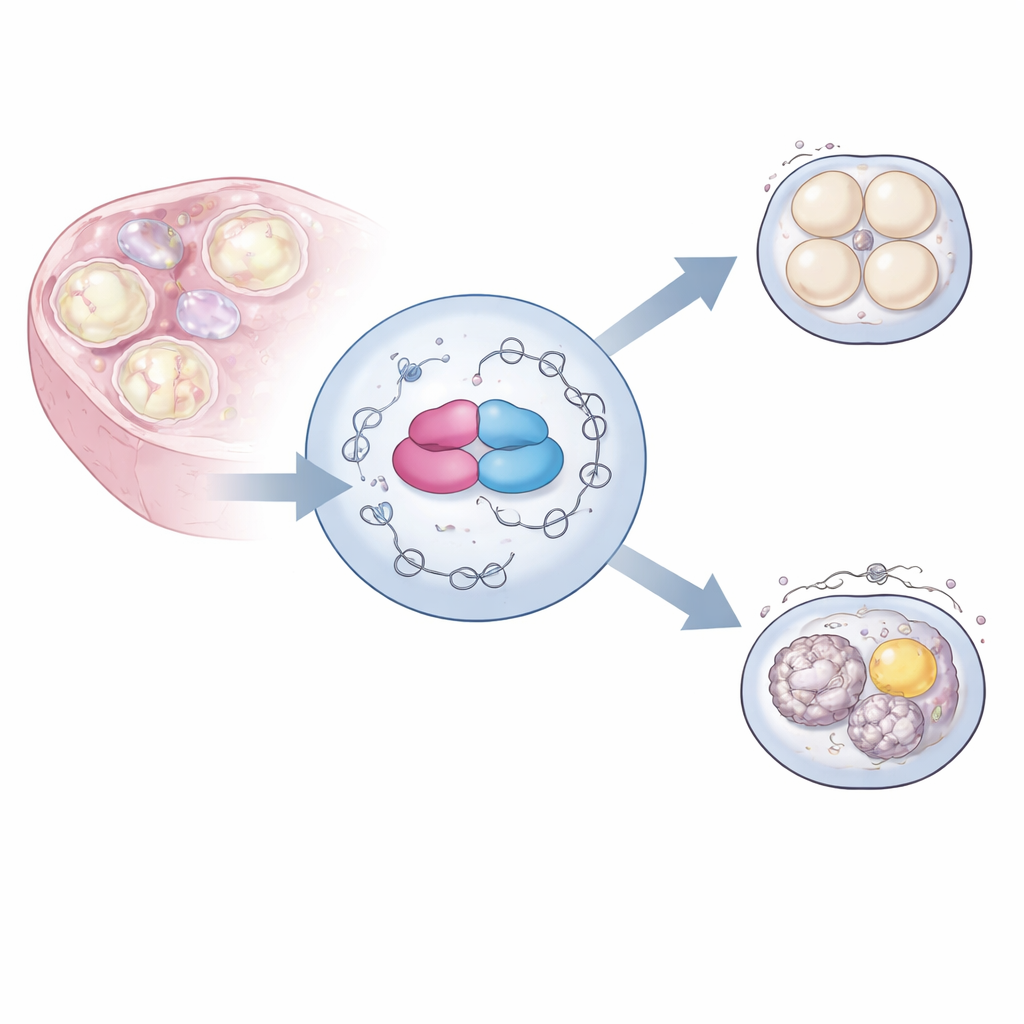
Para explorar la función de hnRNPM, el equipo empleó ingeniería genética para eliminar el gen Hnrnpm específicamente en los precursores de los ovocitos de ratón. Los ovarios de estas hembras parecían normales y producían un número de ovocitos similar al de los controles. Sin embargo, cuando estos ovocitos se fertilizaron en el laboratorio, casi ninguno se desarrolló más allá de las primeras divisiones, dejando a las hembras completamente estériles. Una inspección más detallada de los ovocitos inmaduros reveló agregados oscuros en el citoplasma, que normalmente es claro. La microscopía electrónica mostró que un fino andamiaje interno llamado andamiaje citoplasmático estaba en gran parte ausente, y orgánulos clave como las mitocondrias y las gotas lipídicas se agrupaban de forma anómala en lugar de distribuirse homogéneamente. Estos cambios indicaban un problema profundo en la organización interna del ovocito.
Maquinaria de división celular dañada
Los mismos ovocitos mutantes también tuvieron dificultades para completar la meiosis, la división celular especial que reduce a la mitad el número de cromosomas. Cuando los investigadores maduraron los ovocitos en cultivo, podían iniciar la meiosis pero por lo general se detenían antes de completarla. Al microscopio, las estructuras que separan los cromosomas —los husos— estaban retorcidos, tenían múltiples polos o estaban mal anclados. Una proteína llamada pericentrina, que ayuda a organizar los polos del huso, aparecía tarde y en lugares incorrectos. En conjunto, estos defectos impedían que los ovocitos alinearan y separaran los cromosomas de manera fiable, lo que probablemente explica el fallo completo en el desarrollo tras la fertilización.
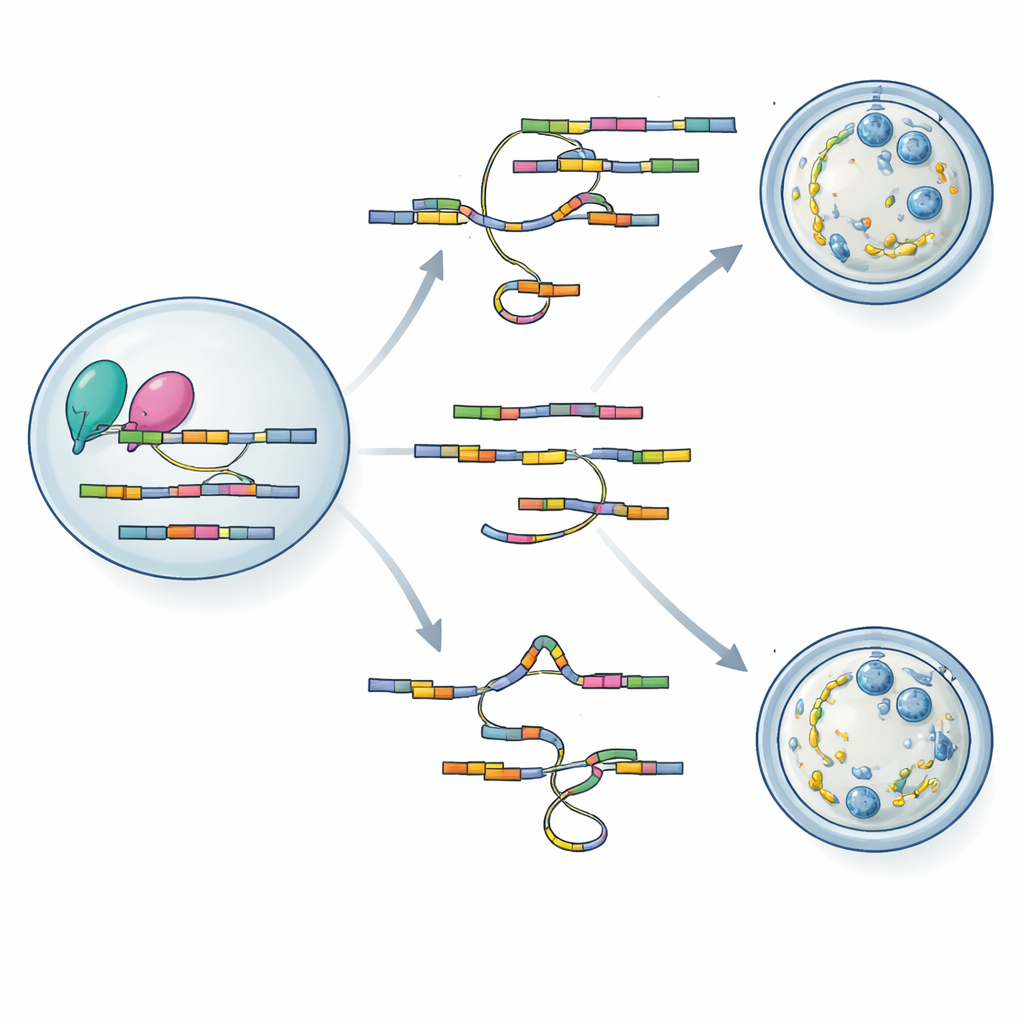
Leer y reescribir las instrucciones del ARN
Para entender cómo la pérdida de hnRNPM provoca defectos tan extendidos, el equipo recurrió a dos potentes herramientas de secuenciación adaptadas a muestras diminutas de ovocitos. Usando SCAN-seq, que lee moléculas de ARN de longitud completa en ovocitos individuales, descubrieron más de mil cambios de empalme en los ovocitos mutantes, incluidos muchos variantes de ARN previamente desconocidos. Los genes implicados en la construcción del andamiaje citoplasmático, el control del comportamiento del huso y la regulación del ciclo meiótico resultaron especialmente afectados. Un segundo método, LACE-seq, mapeó exactamente dónde se une hnRNPM en los ARN, revelando una preferencia por tramos ricos en GU dentro de los exones. Superponiendo ambos conjuntos de datos, los autores mostraron que hnRNPM se sitúa directamente sobre muchos de los mensajeros cuyo empalme cambia cuando falta la proteína, vinculando su actividad de unión con la precisión del empalme.
Un modelo cooperativo para el control del ovocito
Estudios de interacción proteica demostraron que hnRNPM se asocia físicamente con BCAS2 y con componentes centrales de la maquinaria de empalme. Las dos proteínas se unen a muchos de los mismos objetivos de ARN y a menudo los alteran de la misma manera cuando cualquiera de ellas se ve perturbada. De forma intrigante, la pérdida de hnRNPM redujo los niveles de proteína BCAS2 y debilitó la afinidad de BCAS2 por los objetivos de ARN compartidos, lo que sugiere que hnRNPM no solo edita los mensajeros sino que también ayuda a estabilizar a su socia sobre esos mensajeros. Los autores proponen un modelo en el que hnRNPM y BCAS2 forman un complejo cooperativo que ajusta ARN maternales clave durante el crecimiento del ovocito, asegurando la correcta formación del andamiaje citoplasmático y una división meiótica fiable.
Qué significa esto para la fertilidad
En términos sencillos, este trabajo demuestra que un equipo molecular de edición —hnRNPM y BCAS2— actúa detrás de escena para preparar los ovocitos para la vida tras la fertilización. Cuando este equipo falta, el andamiaje interno del ovocito colapsa, su maquinaria de clasificación cromosómica falla y, pese a que el ovocito se produce en número normal, no puede sustentar el desarrollo embrionario. Dado que hnRNPM es muy similar en ratones y humanos, estos hallazgos apuntan a un sistema conservado de control de calidad que podría subyacer a ciertas formas de infertilidad femenina inexplicada y ofrecer nuevas vías para el diagnóstico o el tratamiento.
Cita: Zhou, S., Liu, D., Gan, S. et al. hnRNPM cooperates with BCAS2 to modulate alternative splicing during oocyte development. Nat Commun 17, 2681 (2026). https://doi.org/10.1038/s41467-026-69176-8
Palabras clave: desarrollo del ovocito, empalme alternativo, infertilidad femenina, proteínas de unión al ARN, andamiaje citoplasmático