Clear Sky Science · es
Impacto de las fuerzas del solvente y la simetría rota en el ensamblaje de proteínas diseñadas en una interfaz líquido-sólido
Por qué importa este diminuto mundo sobre una superficie
Desde las celdas solares hasta los sensores médicos, muchas tecnologías futuras dependerán de construir estructuras precisas en la frontera donde las moléculas biológicas se encuentran con materiales sólidos. Este estudio examina cómo "varillas" proteicas diseñadas a medida se organizan sobre superficies minerales en agua salina. La lección sorprendente es que el agua justo en la superficie, y las sutiles asimetrías del cristal subyacente, pueden cambiar por completo la forma en que estas proteínas se alinean: a veces generando patrones que la teoría clásica indicaría que no deberían existir.
Diseñar proteínas para encajar con un cristal
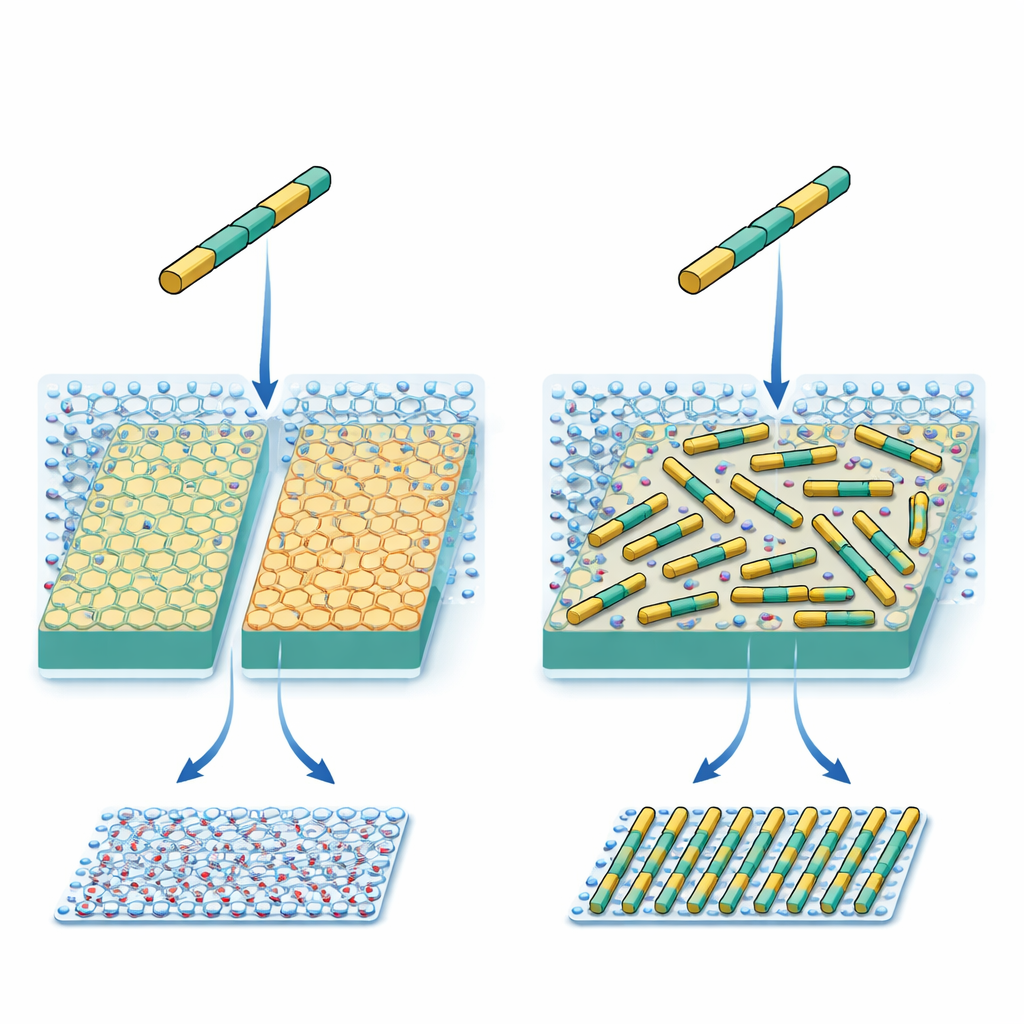
Los investigadores trabajan con una proteína artificial con forma de varilla corta y rígida. Su química superficial y la separación de grupos cargados se diseñaron cuidadosamente para coincidir con el patrón de iones potasio en un mineral común llamado mica. En principio, esto debería hacer que cada varilla proteica prefiriera tres direcciones equivalentes sobre la superficie cristalina, como alinearse a lo largo de tres radios de una rueda. Trabajos previos mostraron que, incluso con tal diseño cuidadoso, las proteínas formaron múltiples patrones inesperados en lugar de solo el que los ingenieros habían previsto. Esa inconsistencia sugirió que faltaba alguna fuerza importante en las reglas de diseño actuales.
Dos superficies casi idénticas, dos resultados muy distintos
Para seguir lo que ocurría, el equipo utilizó microscopía de fuerza atómica de alta velocidad, que puede observar varillas proteicas individuales moverse y ensamblarse sobre una superficie en tiempo real. Compararon dos formas estrechamente relacionadas de mica. Ambas tienen la misma red expuesta de potasio, pero sus estructuras atómicas internas difieren ligeramente, lo que a su vez cambia cómo se organiza el agua en capas justo por encima de la superficie. A concentraciones moderadas de sal, las varillas formaron una alfombra densa pero localmente desordenada en ambas superficies, con solo pequeños parches de alineamiento. Sin embargo, cuando la concentración de sal se aumentó mucho, el comportamiento se bifurcó: en un tipo de mica, las varillas siguieron desordenadas a lo largo de tres direcciones, mientras que en la otra formaron espontáneamente largas filas paralelas y equiespaciadas a lo largo de toda la superficie.
Capas de agua y simetría rota
El modelado por computadora de los minerales y el agua circundante ayudó a explicar esta doble personalidad. En la forma de mica más simétrica, la primera y la segunda capa de moléculas de agua conservan un patrón hexagonal regular. En la forma menos simétrica, los átomos internos y grupos enterrados dentro del cristal rompen esa simetría triple, y este patrón roto se transmite a las capas de agua cercanas, que desarrollan regiones con aspecto de franjas. Las proteínas no contactan el cristal desnudo por sí solo; interactúan también con esta agua estructurada. Como resultado, una orientación de las varillas se vuelve ligeramente más favorable que las otras dos, aun cuando la coincidencia diseñada entre proteína y cristal sugeriría que las tres deberían ser iguales.
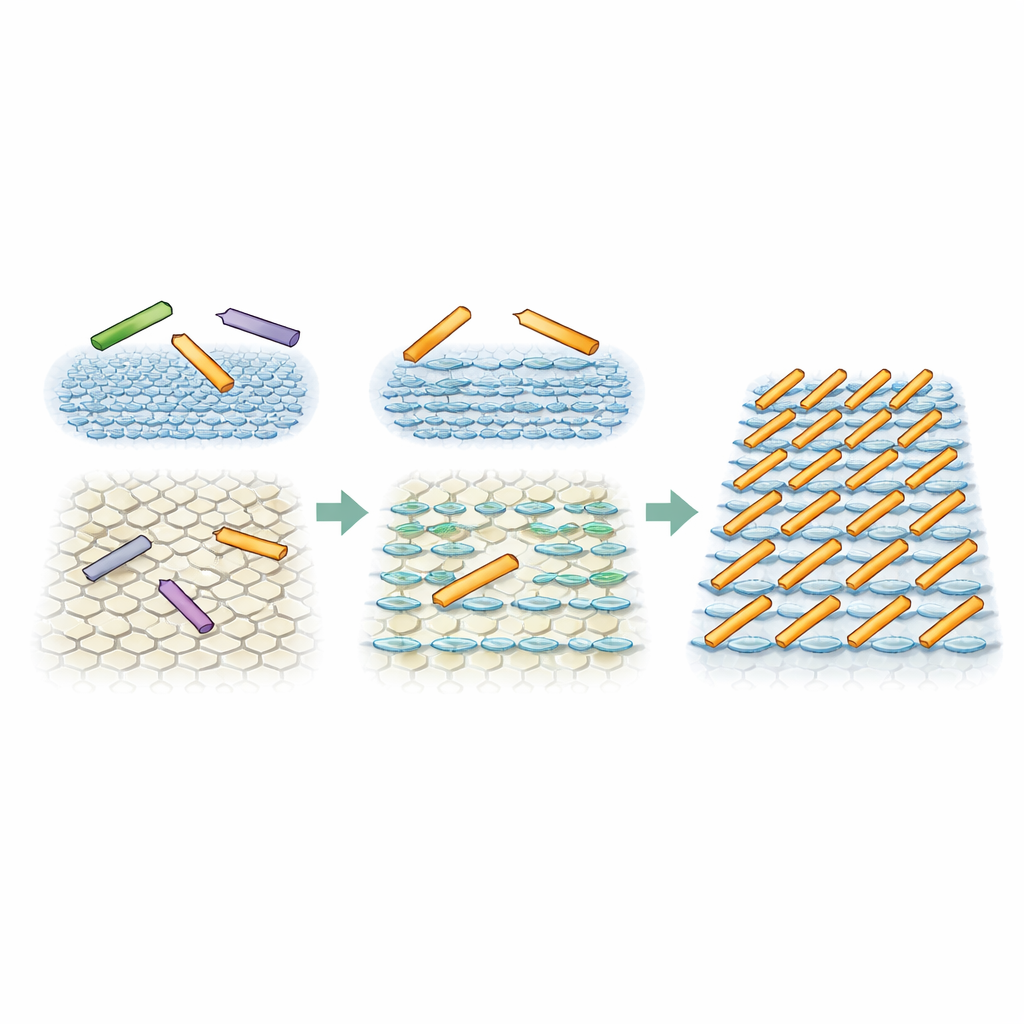
Las simulaciones revelan una fase inesperada
Para comprobar si un sesgo direccional sutil del entorno superficial podía realmente explicar los patrones observados, los investigadores realizaron simulaciones Monte Carlo de rectángulos rígidos simples que representan las varillas proteicas. En un conjunto de simulaciones, las tres orientaciones eran igualmente probables, imitando la superficie totalmente simétrica. En ese caso, las varillas permanecieron en un estado de alta densidad pero desordenado, con solo alineamientos temporales o limitados, tal como se vio en un tipo de mica. En un segundo conjunto, una dirección se hizo solo modestamente más favorable —aproximadamente el doble de probable que las otras dos— representando la influencia de las capas de agua en franjas. Bajo estas condiciones, y cuando las varillas podían moverse lo suficiente, el sistema evolucionó de forma natural hacia un estado con filas paralelas y equiespaciadas. Esta es la llamada fase smectica, que la teoría de larga data dice que no debería aparecer para varillas no interactuantes en dos dimensiones, sin embargo el pequeño empuje direccional de la interfaz la estabilizó.
Repensar cómo diseñamos materiales bioinspirados
En resumen, este trabajo muestra que una química proteína-superficie finamente ajustada no es suficiente para predecir cómo se dispondrán las proteínas diseñadas sobre materiales reales. El agua situada entre la proteína y el sólido, y la forma en que el cristal rompe sutilmente la simetría, pueden dirigir el ensamblaje hacia patrones que los modelos de libro de texto jamás anticiparían. Combinando microscopía de alta velocidad, aprendizaje automático para cuantificar el orden y simulaciones basadas en la física, el estudio traza una vía para incorporar estos efectos ocultos del solvente y la simetría en futuras herramientas de diseño de proteínas. Para cualquiera que espere diseñar materiales híbridos bio-inorgánicos fiables, el mensaje es claro: debe diseñar no solo para la proteína y la superficie, sino también para la capa estructurada de agua que los conecta.
Cita: Yadav Schmid, S., Helfrecht, B., Stegmann, A. et al. Impact of solvent forces and broken symmetry on the assembly of designed proteins at a liquid-solid interface. Nat Commun 17, 2446 (2026). https://doi.org/10.1038/s41467-026-69170-0
Palabras clave: autoensamblaje de proteínas, interfases líquido-sólido, estructura del agua interfacial, ordenamiento smectico, materiales bioinspirados