Clear Sky Science · es
Un enfoque integrador de biología estructural revela la organización dinámica del complejo chaperón cuaternario R2SP
Cómo las células construyen máquinas moleculares complejas
Dentro de cada célula, muchas proteínas no actúan solas: deben ensamblarse en máquinas elaboradas antes de poder desempeñar sus funciones. Hacer bien este paso de ensamblaje es vital para una respiración sana, el movimiento e incluso la fertilidad. Este trabajo explora a uno de esos ayudantes de ensamblaje, una "tripulación de construcción" molecular llamada complejo R2SP, y muestra cómo está organizada y cómo funciona. Entender R2SP es importante porque cuando sus componentes fallan, unas pequeñas estructuras semejantes a pelos en la superficie celular llamadas cilios no se mueven correctamente, lo que conduce a problemas respiratorios crónicos y otras enfermedades.
Las cuadrillas de construcción celular R2TP y R2SP
Las células dependen de equipos de proteínas auxiliares, conocidos como complejos chaperones, para guiar a otras proteínas hacia las formas multipartitas correctas. Un equipo estudiado durante mucho tiempo, llamado R2TP, se encuentra en muchos tejidos y ayuda a ensamblar grandes máquinas como las fábricas de ARN y los sensores de daño en el ADN. R2SP es un primo cercano de R2TP: ambos se construyen alrededor del mismo motor en forma de anillo formado por dos proteínas asociadas, RUVBL1 y RUVBL2, que consumen la molécula energética ATP. Lo que difiere son los adaptadores accesorios que conectan a los clientes con este motor. R2TP emplea adaptadores llamados RPAP3 y PIH1D1, mientras que R2SP utiliza SPAG1 y PIH1D2. Estas pequeñas diferencias en las piezas confieren a los dos complejos listas de clientes distintas y vinculan en particular a R2SP con la construcción de los cilios móviles que barren el moco y los fluidos sobre los tejidos.
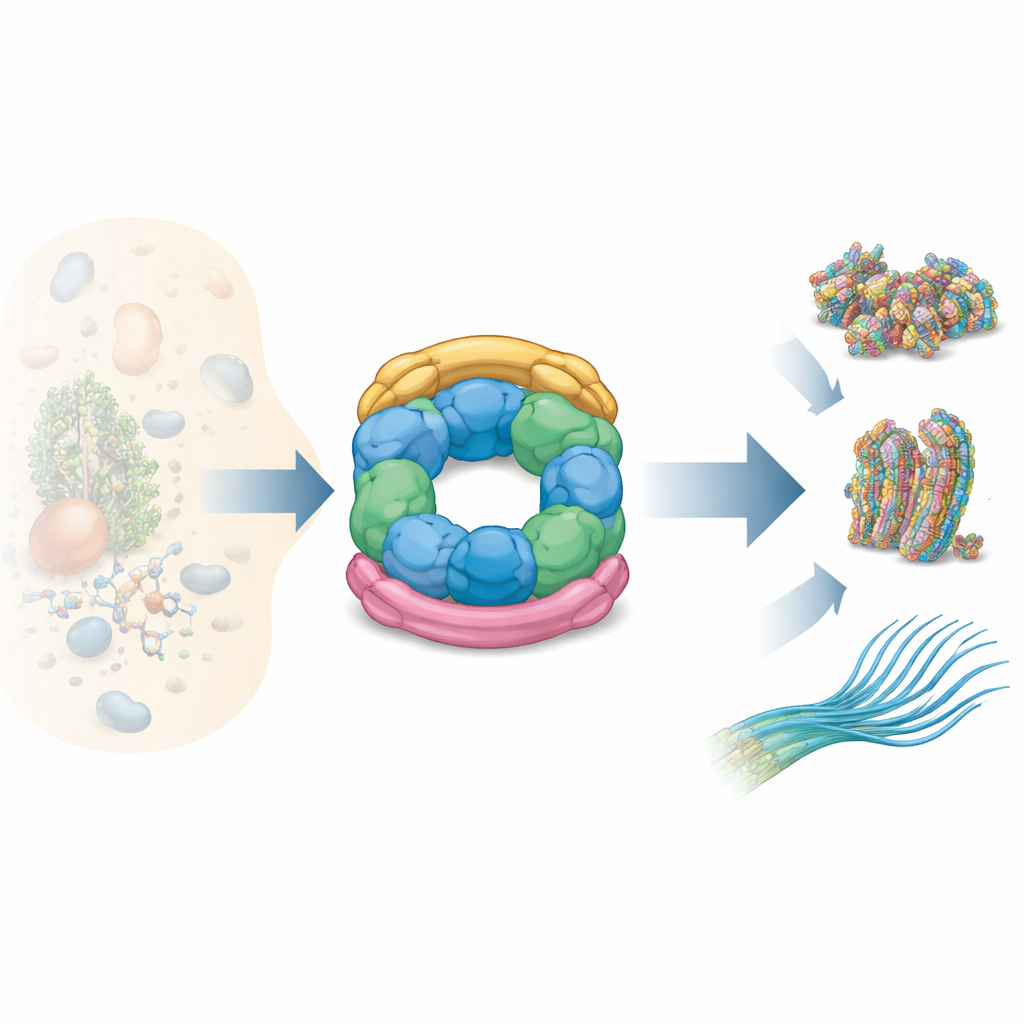
Cómo encajan las piezas de R2SP
Los autores combinaron varias técnicas estructurales —resonancia magnética nuclear, criomicroscopía electrónica y espectrometría de masas con entrecruzamiento— con ensayos bioquímicos para mapear cómo se construye R2SP. Mostraron que el extremo en cola de SPAG1 se agarra al anillo RUVBL1/RUVBL2 de una forma que recuerda a cómo se une RPAP3 en R2TP, pero con ajustes clave en la forma y los puntos de contacto. Un segundo adaptador, PIH1D2, se asienta bajo el anillo y también alcanza a tocar dominios laterales flexibles del motor. Estos dominios laterales actúan como brazos con bisagra que ayudan a transmitir movimientos desde el núcleo que consume ATP hacia los clientes unidos. Los datos revelan que SPAG1 y PIH1D2 no se acoplan de forma independiente: cooperan, formando una unidad acoplada que sujeta el anillo desde arriba y desde abajo, estabilizando una arquitectura tridimensional distintiva.
Un anillo dinámico que cambia de marcha
Más allá de imágenes estáticas, el equipo investigó cómo se comporta R2SP. Mediante medidas de interacción, encontraron que el motor RUVBL1/RUVBL2 puede existir tanto como un anillo simple como en una pila de anillos dobles. Cuando SPAG1 y PIH1D2 se unen, desplazan fuertemente este equilibrio hacia la forma de anillo simple y pueden decorar dicho anillo con hasta tres pares de adaptadores. Al mismo tiempo, los adaptadores aumentan notablemente la actividad consumidora de ATP del motor y cambian la velocidad con que moléculas semejantes al ATP se unen y se desprenden de los sitios activos. En comparación con el sistema R2TP, SPAG1 y PIH1D2 favorecen pasos distintos en la liberación de nucleótidos, lo que sugiere que R2SP ajusta el ciclo energético del motor central a su manera. Se piensa que este uso de energía finamente controlado impulsa el ensamblaje por etapas de los complejos clientes necesarios para los cilios móviles.
Una plataforma flexible para construir componentes ciliares
Al integrar todas sus restricciones estructurales en un único modelo, los autores proponen que R2SP actúa como una plataforma flexible y de múltiples brazos. La cola de SPAG1 se ancla firmemente en la parte superior del anillo, mientras que sus otras regiones y los dos dominios de PIH1D2 se extienden hacia el lado más abierto, en forma de brazo, del motor. Este lado es donde es más probable que se acoplen las proteínas clientes y chaperonas auxiliares como HSP70 y HSP90. Debido a que hasta tres unidades SPAG1–PIH1D2 pueden unirse a un mismo anillo y los brazos flexibles se mueven constantemente, el complejo se asemeja a un pulpo cuyos tentáculos pueden agarrar varias piezas cliente a la vez, coordinaras y entregarlas para su ensamblaje en estructuras ciliares más grandes.
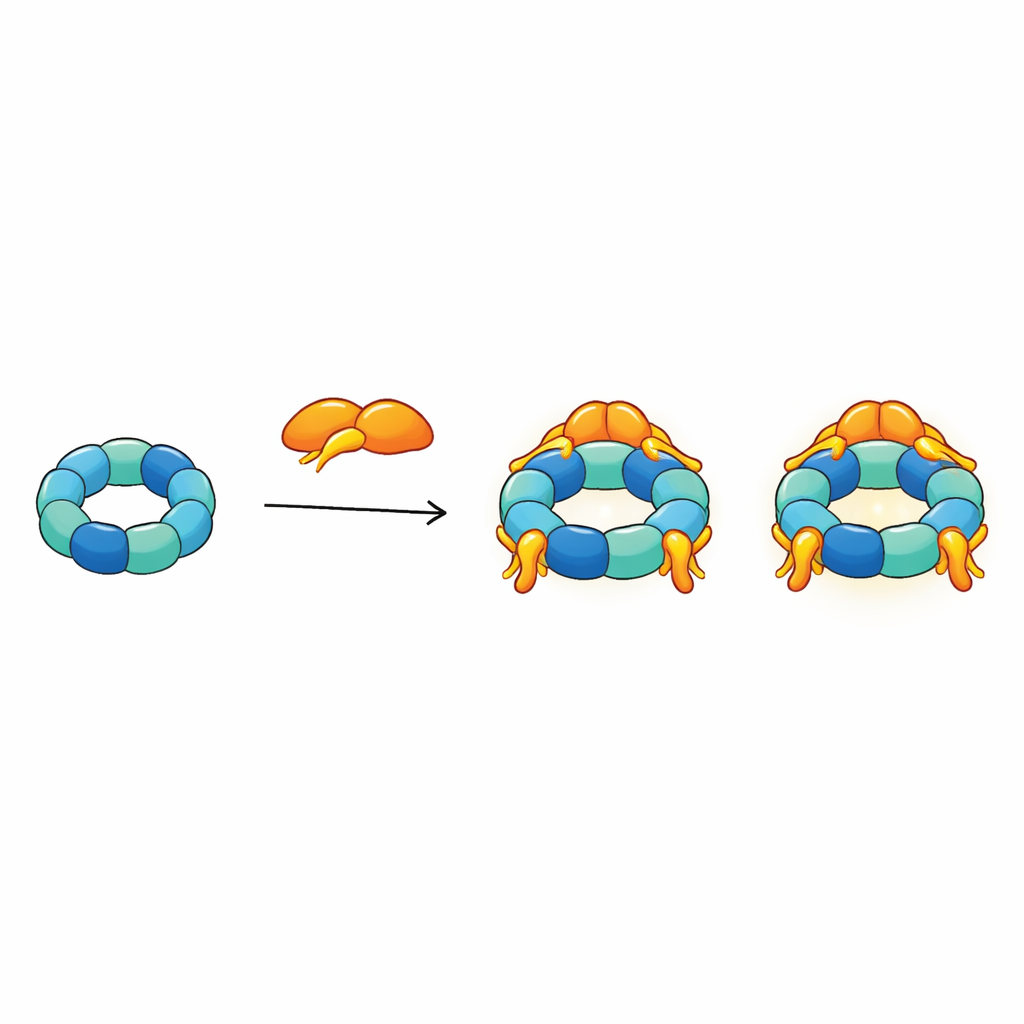
Qué significa esto para la salud y la enfermedad
Para el público no especializado, el mensaje principal es que R2SP es una versión especializada de una máquina general de construcción celular, reconectada mediante el intercambio de apenas dos proteínas adaptadoras. Este intercambio cambia tanto cómo se controla el motor central como cómo se posicionan los clientes, lo que explica por qué R2SP se centra en construir piezas para cilios móviles mientras que R2TP sirve a otras fábricas celulares. Ya se sabe que fallos en SPAG1 causan discinesia ciliar primaria, un trastorno caracterizado por infecciones crónicas y problemas de fertilidad. Al revelar la disposición detallada y los principios de funcionamiento de R2SP, este estudio sienta las bases para entender cómo mutaciones concretas interrumpen el ensamblaje de cilios y podría, eventualmente, guiar tratamientos dirigidos que restauren o modulen esta crucial tripulación molecular de construcción.
Cita: Santo, P.E., Chagot, ME., Gizardin-Fredon, H. et al. An integrative structural biology approach reveals the dynamic organization of the R2SP quaternary chaperone complex. Nat Commun 17, 2605 (2026). https://doi.org/10.1038/s41467-026-69157-x
Palabras clave: chaperonas moleculares, ensamblaje de complejos proteicos, cilios móviles, biología estructural, RUVBL1 RUVBL2