Clear Sky Science · es
Mecanismo molecular de importación de fosfato por el transportador bacteriano PstSCAB
Por qué nos importan los nutrientes minúsculos
Cada célula viva, desde las neuronas humanas hasta las bacterias del suelo, funciona gracias al fósforo. Este elemento ayuda a almacenar energía, construir el ADN y mantener la integridad de las membranas celulares. Sin embargo, en el entorno, el fosfato utilizable —la forma de fósforo que las células pueden importar— suele ser escaso. Muchas bacterias patógenas dependen de una máquina molecular ultrafuerte, llamada transportador PstSCAB, para recolectar fosfato cuando hay poca disponibilidad. Entender exactamente cómo funciona esta máquina no es solo una cuestión básica de ciencia; podría abrir vías nuevas para desarmar infecciones privando a las bacterias de este nutriente vital.
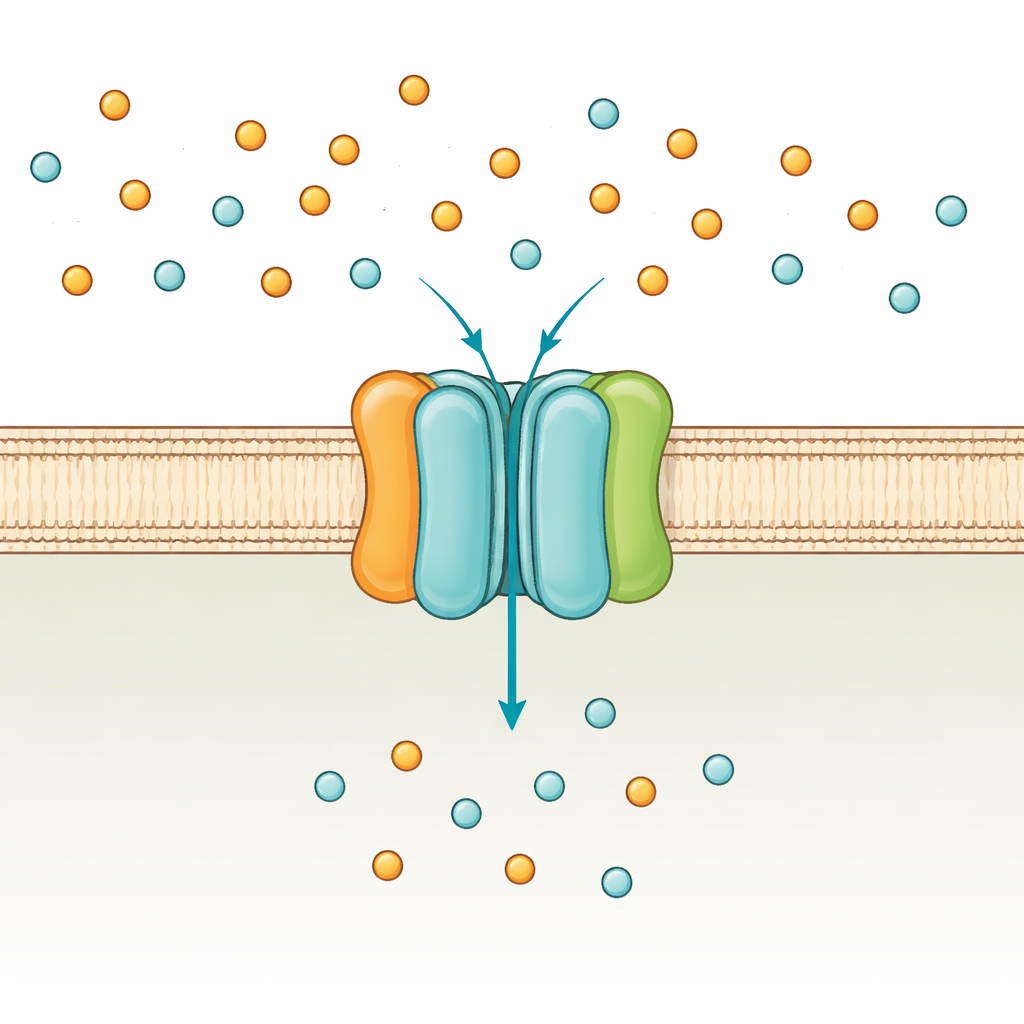
El guardián del fosfato de la célula
Bacterias como Escherichia coli usan dos rutas principales para captar fosfato: un sistema de baja afinidad que funciona cuando el fosfato es abundante, y el sistema de alta afinidad PstSCAB que se activa en condiciones de escasez. PstSCAB se sitúa en la membrana celular y se alimenta de ATP, la moneda energética universal de la célula. Está compuesto por cinco partes: dos subunidades integrales de membrana (PstA y PstC) que forman el pasaje, una proteína soluble “capturadora” fuera de la membrana (PstS) que atrapa el fosfato, y un par de subunidades internas (PstB) que consumen ATP para impulsar el transporte. Dado que este sistema también contribuye al control de muchos genes asociados a la virulencia bacteriana, mutaciones en PstSCAB pueden debilitar patógenos responsables de infecciones del tracto urinario, septicemia en animales de granja y tuberculosis.
Capturando la máquina en acción
Hasta ahora, los científicos solo tenían vistas parciales de PstSCAB, principalmente de la proteína capturadora PstS en solitario. En este estudio, los investigadores emplearon criomicroscopía electrónica de alta resolución para visualizar el transportador completo en varios pasos clave de su ciclo de trabajo. Reconstituyeron las proteínas bacterianas en “nanodiscos” de membrana artificial y las congelaron tan rápido que las moléculas quedaron atrapadas en movimiento. Ajustando con cuidado las proteínas y añadiendo o suprimiendo ATP, obtuvieron estructuras de tres estados principales: una forma de reposo orientada hacia el interior sin la capturadora unida, un estado pretranslocación en el que PstS cargado de fosfato se acopla al complejo de membrana, y un intermedio catalítico ligado a ATP en el que el fosfato queda retenido dentro del transportador.
Cómo los cambios de forma mueven el fosfato
Las imágenes revelan cómo los cambios de forma coordinados trasladan el fosfato del exterior al interior de la célula. En el estado de reposo, el pasaje formado por PstA y PstC se abre solo hacia el interior celular; el lado exterior está sellado por un conjunto de residuos que actúan como “puerta”, de modo que el fosfato aún no puede entrar desde fuera. Cuando PstS, cargado de fosfato, se acopla en el estado pretranslocación, se acomoda entre bucles flexibles de PstA y PstC pero, de forma sorprendente, las subunidades de membrana apenas cambian de forma. El cambio real ocurre cuando PstS comienza a abrir sus dos lóbulos para liberar el fosfato y, a la vez, las dos subunidades PstB se aproximan para unirse al ATP. Esta unión al ATP estabiliza a PstB en dímero y tira de las hélices conectantes en PstA y PstC, invirtiendo todo el poro a una conformación orientada hacia el exterior que expone un bolsillo específico de unión al fosfato hacia afuera.
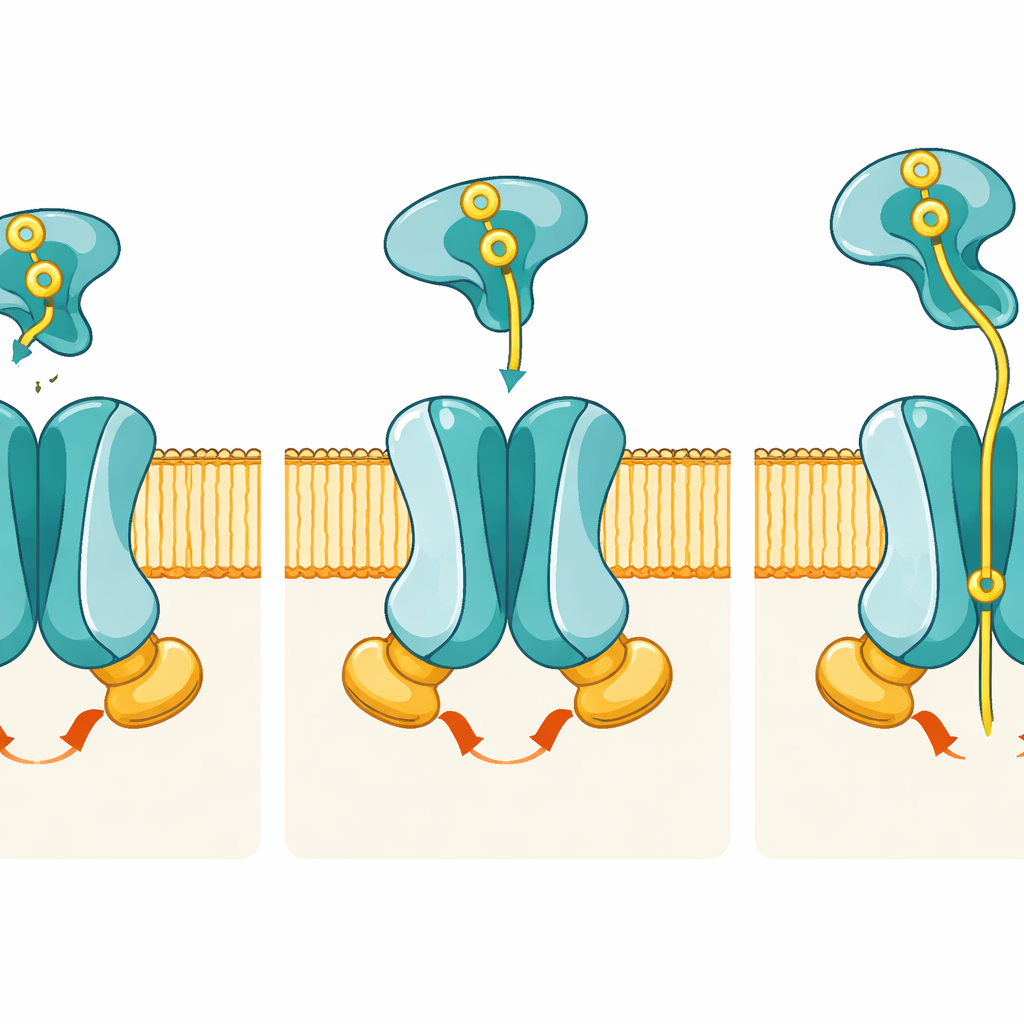
Un bolsillo a medida para el fosfato
En la estructura orientada hacia el exterior y ligada a ATP, los autores encuentran una densidad en el centro de la región de membrana que coincide con un ion fosfato. Este ion está acunado por aminoácidos cargados positivamente —en particular dos argininas, una de PstA y otra de PstC— que actúan como puntas moleculares que sujetan el fosfato cargado negativamente. Simulaciones por ordenador muestran que el fosfato permanece unido de forma estable en este bolsillo durante microsegundos, y experimentos genéticos confirman su importancia: cuando estos residuos clave se mutan, el transportador sigue hidrolizando ATP pero importa fosfato muy mal. Esta separación entre “dónde se gasta la energía” y “dónde se reconoce la carga” subraya lo finamente afinada que está la máquina para el fosfato.
De instantáneas estructurales a promesas médicas
En conjunto, las estructuras y las pruebas bioquímicas de apoyo delinean un ciclo completo: PstS captura fosfato en el exterior, se acopla al transportador orientado hacia el interior y luego —acoplado a la unión y al corte de ATP por parte de PstB— provoca un volteo que traslada el fosfato al bolsillo en la membrana y finalmente al interior celular. Tras la hidrólisis del ATP, la máquina vuelve a relajarse a su estado de reposo, lista para otra ronda. Para un lector general, el mensaje clave es que ahora disponemos de un plano a nivel atómico de cómo muchas bacterias sobreviven en ambientes pobres en fosfato y regulan su virulencia. Este mapa detallado puede guiar el diseño de fármacos, anticuerpos o péptidos que bloqueen el transportador o su proteína capturadora, convirtiendo potencialmente esta puerta de un nutriente esencial en un blanco terapéutico vulnerable.
Cita: Xiao, H., Li, S., Qi, R. et al. Molecular mechanism of phosphate import by the bacterial PstSCAB transporter. Nat Commun 17, 2294 (2026). https://doi.org/10.1038/s41467-026-69153-1
Palabras clave: transporte de fosfato, captación de nutrientes en bacterias, transportador ABC, PstSCAB, blancos antibacterianos