Clear Sky Science · es
Alquilenilación y alquinilación selectiva en N-Me en fase tardía de fármacos y aminas terciarias no activadas mediante catálisis fotoredox
Por qué sigue importando cambiar medicamentos antiguos
Muchos de los medicamentos actuales funcionan bien, pero todavía hay margen de mejora en su seguridad, efectos secundarios o en la precisión con la que alcanzan sus dianas en el organismo. Los químicos se interesan cada vez más en «ajustar» con suavidad fármacos ya existentes en etapas avanzadas del desarrollo, en lugar de inventar moléculas completamente nuevas desde cero. Este estudio muestra cómo haces de luz visible pueden usarse para añadir nuevas piezas a un tipo común de bloque de construcción farmacéutico, creando candidatas antidepresivas mejoradas y abriendo una vía más rápida hacia tratamientos refinados.
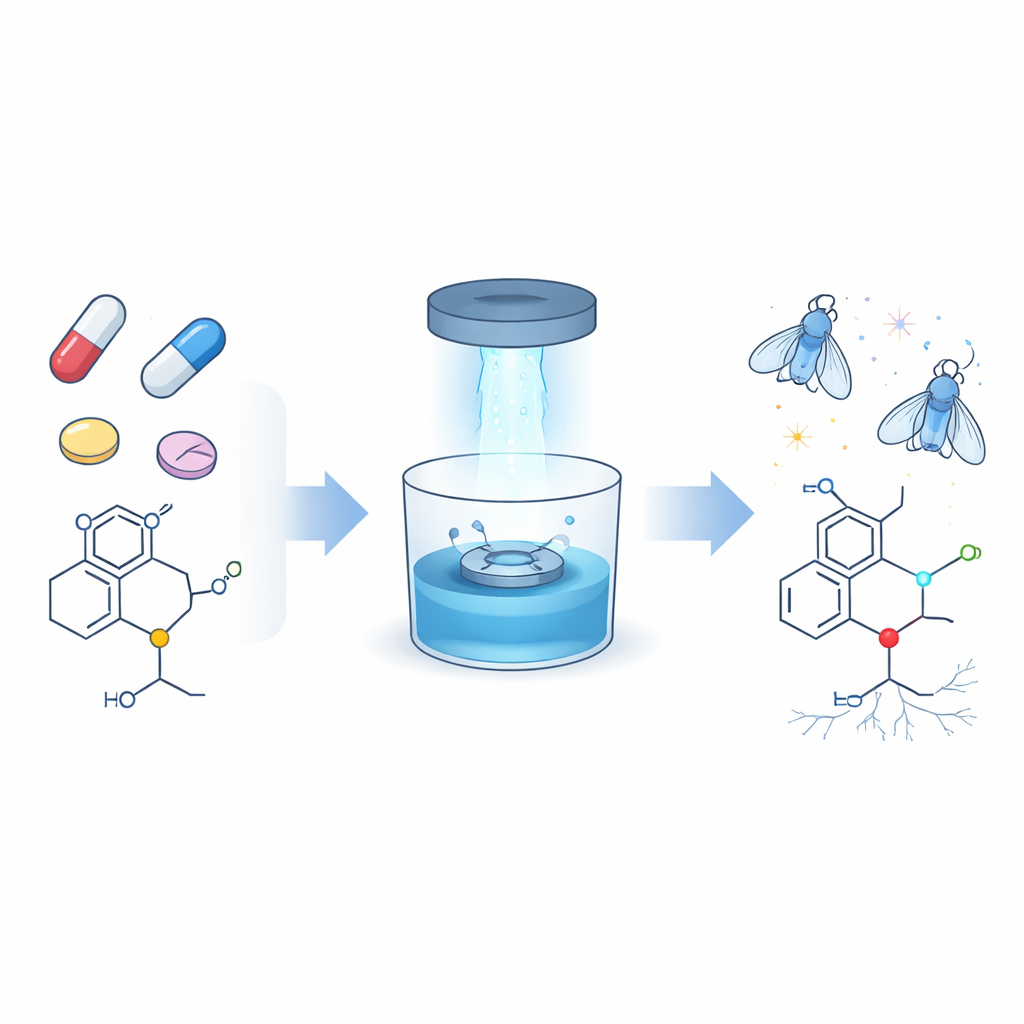
Mejorando un rasgo común en muchos fármacos
Una proporción sorprendentemente alta de los medicamentos modernos—más de dos de cada cinco—contiene fragmentos ricos en nitrógeno llamados aminas, y la mayor parte de estas son de un subtipo conocido como aminas terciarias. Aparecen en antibióticos, fármacos contra el cáncer, antialérgicos, analgésicos y antidepresivos. Hasta ahora, los químicos han tenido dificultades para modificar selectivamente una parte muy pequeña de estos grupos, la unidad N-metilo, cuando está rodeada de varios enlaces carbono–hidrógeno casi idénticos. Los autores se propusieron desarrollar una forma suave y fiable de unir nuevas “asas”, concretamente enlaces carbono–carbono dobles (alquenos) y triples (alquinos), en esa posición N-metilo sin alterar el resto de la molécula del fármaco.
Usar la luz para reconfigurar un enlace a la vez
El equipo recurrió a la catálisis fotoredox, una tecnología que emplea luz visible y un catalizador fotosensible para mover electrones individuales y desencadenar reacciones en condiciones suaves. En su sistema, la luz azul excita un catalizador orgánico, que extrae temporalmente un electrón de la amina terciaria. Este paso crea un radical de vida corta en la posición N-metilo que puede unirse a moléculas compañeras cuidadosamente elegidas que llevan grupos vinilo o alquinilo. Al ajustar las condiciones de reacción—elección de disolvente, base y aditivos—los investigadores lograron altos rendimientos y un control excelente, de modo que el nuevo grupo se incorpora casi exclusivamente en la posición N-metilo, incluso cuando hay varios sitios similares presentes. Demostraron esto en un amplio panel de aminas simples y después en fármacos reales, incluidos antihistamínicos, medicamentos cardiacos, antiinfecciosos y varios antidepresivos.
Del ajuste químico a una mejor acción antidepresiva
Para evaluar si estos ajustes estructurales podían tener relevancia médica, los autores se centraron en la imipramina, un antidepresivo tricíclico de uso prolongado. Diseñaron y modelaron más de veinte variantes de imipramina en las que la nueva extensión vinílica o alquinílica portaba anillos aromáticos que podrían encajar en un bolsillo hidrofóbico del transportador humano de serotonina, una proteína que regula los niveles del mensajero relacionado con el estado de ánimo, la serotonina. El acoplamiento por ordenador sugirió que muchas de estas moléculas modificadas deberían unirse tan bien como, o mejor que, el fármaco original. Los candidatos más prometedores se sintetizaron luego usando el nuevo método activado por luz y se probaron en sistemas vivos: un modelo de depresión en la mosca de la fruta basado en el aislamiento social y, para los dos compuestos mejores, en neuronas de ratón que transportan activamente serotonina.
Cómo moscas y células revelaron fármacos más potentes
En moscas de la fruta macho aisladas, el comportamiento tipo depresión se manifiesta como un aumento de la agresión. Alimentar con imipramina reduce esta agresión, reflejando su acción antidepresiva en humanos. De forma notable, varias de las derivadas de imipramina producidas por el nuevo método redujeron la agresión igual de bien, y cuatro candidatas funcionaron incluso mejor que la propia imipramina. En cultivos de células hipocampales de ratón, dos compuestos líderes bloquearon la recaptación de serotonina con más fuerza que la imipramina, según se confirmó tanto por mediciones químicas directas de serotonina como por un tinte fluorescente que se ilumina al ser captado por las células. Estas pruebas indican que cambios sutiles en fase tardía en el sitio N-metilo pueden mejorar genuinamente la potencia antidepresiva, y no limitarse a modificar la molécula sobre el papel.
Por qué la reacción es tan selectiva
Una cuestión científica clave era por qué la reacción modifica el grupo N-metilo con tanta limpieza cuando otras posiciones cercanas parecen igualmente reactivas. A través de experimentos de control, mediciones de spin electrónico y cálculos computacionales detallados, los autores mostraron que el punto decisivo crucial no es cuando el radical se forma por primera vez, sino cuando ese radical se adiciona al compañero vinílico o alquinílico. La vía que conduce desde el radical N-metilo hasta el producto final es tanto energéticamente más favorable como mucho más rápida que las rutas competidoras, orientando efectivamente la reacción hacia un único resultado. Esta idea ayuda a explicar la alta selectividad y podría guiar estrategias similares en otras moléculas complejas.
Qué significa este trabajo para futuros medicamentos
En conjunto, el estudio introduce una forma práctica de mejorar quirúrgicamente fármacos existentes que contienen aminas terciarias, añadiendo asas químicas compactas que pueden ajustar cómo interactúan con dianas biológicas o unirse a otros componentes. Al mostrar que dichas modificaciones en fase tardía pueden convertir un antidepresivo bien establecido en variantes aún más eficaces en modelos sencillos de animal y célula, el trabajo apunta a una poderosa combinación de química sintética moderna, computación y biología. A medida que el enfoque se extienda a otros medicamentos, podría acelerar la refinación de candidatos farmacológicos y ayudar a actualizar terapias antiguas con un rendimiento y una seguridad mejorados.
Cita: Paul, S., Mahato, S., Mahapatra, S.K. et al. Late-stage N-Me selective alkenylation and alkynylation of drugs and unactivated tertiary amines using photoredox catalysis. Nat Commun 17, 2695 (2026). https://doi.org/10.1038/s41467-026-69131-7
Palabras clave: catálisis fotoredox, funcionalización en fase tardía, aminas terciarias, diseño de fármacos antidepresivos, transportador de serotonina