Clear Sky Science · es
Terapia bacteriana diseñada suprime Escherichia coli enterohemorrágica mediante competencia metabólica y silenciamiento de la virulencia
Bacterias amigas como medicina viva
El envenenamiento alimentario por ciertas cepas de Escherichia coli puede provocar mucho más que un malestar estomacal. Algunas de las llamadas E. coli enterohemorrágicas (EHEC) liberan potentes toxinas que pueden desencadenar insuficiencia renal, especialmente en niños, y los antibióticos estándar pueden empeorar la situación. Este estudio explora otro tipo de tratamiento: usar un probiótico diseñado y un azúcar presente en la leche materna, encapsulados en microcápsulas inteligentes, para competir con las bacterias peligrosas y silenciar su comportamiento dañino sin perturbar el resto del ecosistema intestinal.
Por qué algunas E. coli son tan peligrosas
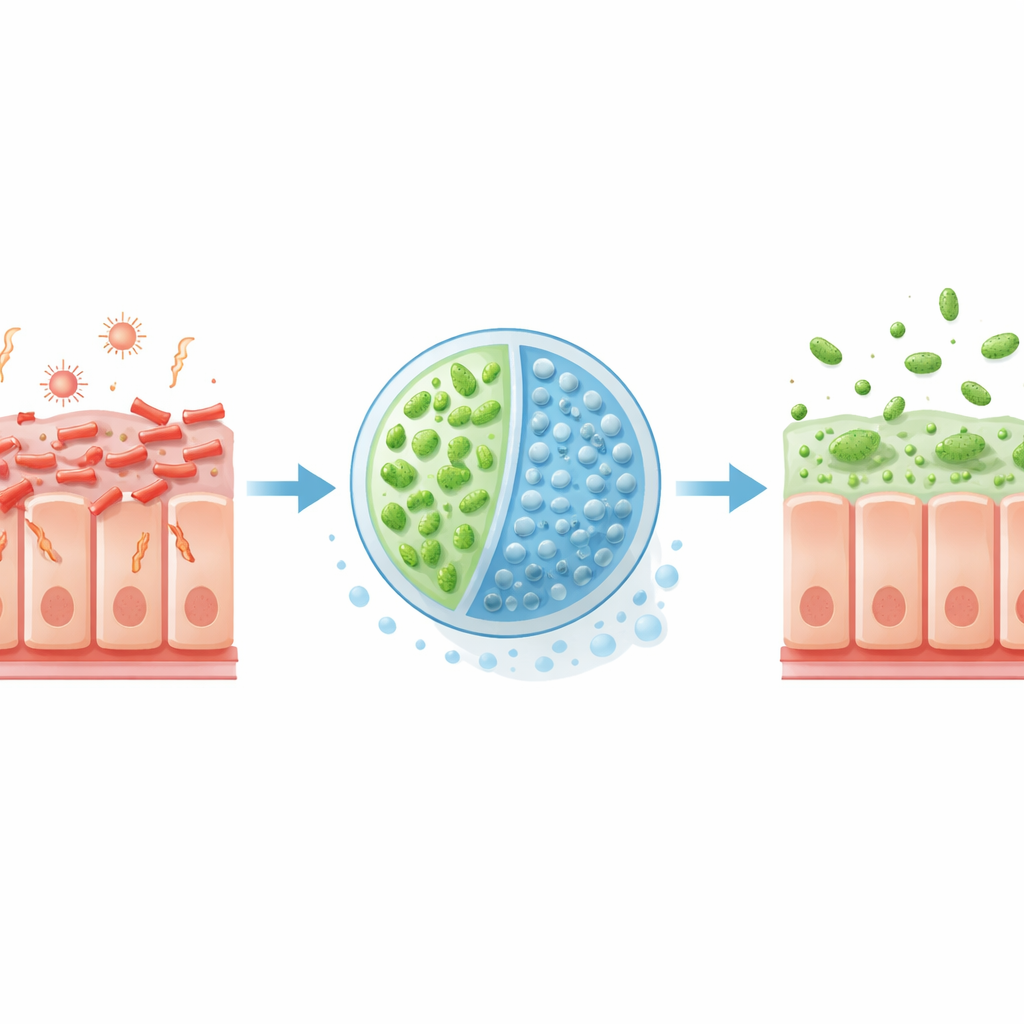
La EHEC es un germen transmitido por alimentos que a menudo se adquiere por carne poco cocinada o productos contaminados. Una vez en el intestino, se adhiere firmemente a las células intestinales e inyecta proteínas que remodelan la superficie celular, creando puntos de apoyo que ayudan a la bacteria a aferrarse y propagarse. Al mismo tiempo, la EHEC produce toxinas Shiga, que pueden entrar en el torrente sanguíneo y dañar los vasos sanguíneos, a veces conduciendo a una condición potencialmente letal llamada síndrome urémico hemolítico. Dado que muchos antibióticos estresan a estas bacterias y desencadenan aún más liberación de toxinas, los médicos disponen de pocas opciones seguras más allá de la atención de soporte, lo que hace deseables enfoques nuevos y dirigidos.
Reprogramar un probiótico para desarmar y privar de alimento a la EHEC
Los investigadores recurrieron a Escherichia coli Nissle 1917, una cepa probiótica de larga data, y la reconfiguraron en un microbio terapéutico llamado EcN3. Dotaron a EcN3 con genes adicionales que le permiten descomponer con mayor eficiencia un ácido azucarado, el ácido glucurónico, que la EHEC prefiere como fuente de alimento en el intestino grueso. También proporcionaron a EcN3 una enzima que divide el azúcar de la leche materna 2′‑fucosilactosa en dos partes: lactosa y fucosa. La lactosa actúa como un "interruptor" interno que activa el sistema mejorado de utilización de nutrientes en EcN3, ayudándole a absorber el ácido glucurónico y privar a la EHEC de este combustible. La fucosa, por su parte, sirve como señal que indica a la EHEC que reduzca la expresión de genes de virulencia clave, disminuyendo su capacidad para formar unas adherencias firmes y causar daño.
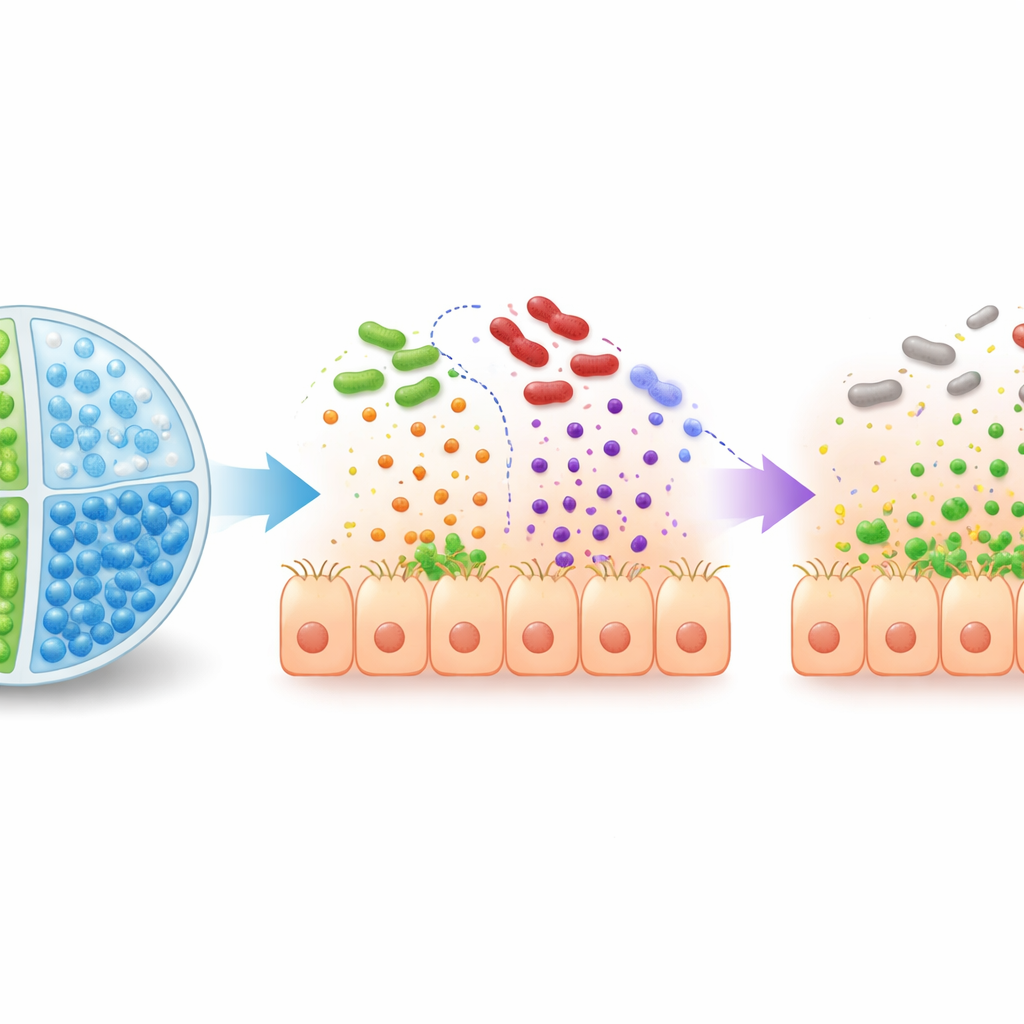
Cápsulas inteligentes que liberan la terapia en el lugar adecuado
Simplemente administrar bacterias diseñadas y azúcar al intestino no es suficiente: el ácido del estómago puede matar al probiótico y otros microbios pueden consumir el azúcar antes de que llegue al colon. Para resolver esto, el equipo construyó microesferas multicompartmentales —pequeñas perlas hechas de gel de alginato con dos cámaras internas separadas. Una cámara contiene EcN3 y la otra contiene 2′‑fucosilactosa, manteniéndolos aislados hasta que las partículas llegan al intestino grueso. Estas microcápsulas resisten la degradación en fluidos simulados del estómago pero se disuelven en condiciones similares al colon, liberando tanto la bacteria diseñada como el azúcar exactamente donde se necesitan. En ratones, el sistema encapsulado condujo a una mayor supervivencia de EcN3 y a una mayor activación de sus genes diseñados que administrar los mismos componentes sin cápsulas.
Pruebas de protección en modelos animales
El equipo probó su estrategia en conejos lactantes infectados con EHEC y en ratones infectados con Citrobacter rodentium, un patógeno estrechamente relacionado que replica muchos aspectos de la enfermedad humana. Cuando se trató después de la infección con EcN3 más 2′‑fucosilactosa, los animales presentaron menos patógenos en el intestino, menor expresión de los genes de adhesión bacteriana y menos daño al tejido intestinal, todo ello sin aumentar la producción de toxina Shiga. Como medida preventiva, la combinación libre (no encapsulada) funcionó mal porque el azúcar fue rápidamente consumida por la microbiota existente. En contraste, cuando EcN3 y 2′‑fucosilactosa se administraron juntos en microesferas de doble cámara, tanto los conejos como los ratones mostraron una colonización patógena marcadamente reducida, enfermedad más leve y mejor supervivencia.
Ayudar a que los microbios beneficiosos y la barrera intestinal se recuperen
Mediante secuenciación de ADN para perfilar las bacterias intestinales, los científicos encontraron que la infección alteraba el equilibrio microbiano normal, aumentando Citrobacter dañino y debilitando grupos beneficiosos. El tratamiento con las microcápsulas diseñadas no sólo redujo los niveles del patógeno sino que también restauró la comunidad hacia un estado más saludable, aumentando especialmente especies de Lactobacillus que se sabe apoyan la salud intestinal. Las medidas de la función de la barrera intestinal contaron una historia similar: los animales que recibieron la terapia encapsulada presentaron niveles más altos de genes relacionados con el moco y las uniones estrechas, capas de moco protector más gruesas y menor filtración de trazadores fluorescentes desde el intestino hacia el torrente sanguíneo, lo que indica paredes intestinales más cerradas y menos inflamadas.
Una mirada a un futuro del tratamiento de infecciones sin antibióticos
En conjunto, este trabajo demuestra una estrategia dirigida y de doble vertiente contra una infección transmitida por alimentos que es notoriamente difícil de tratar. Al combinar un probiótico diseñado que compite por el alimento y detecta una señal de azúcar inocua con microcápsulas que entregan ambos componentes al colon, la terapia debilita a la EHEC, reduce su número y protege el intestino sin recurrir a antibióticos tradicionales. Si bien se necesitan más estudios de seguridad y ensayos clínicos, el enfoque ilustra cómo medicinas vivas y materiales inteligentes podrían algún día ofrecer formas precisas y respetuosas con el microbioma de manejar infecciones intestinales graves y reducir la dependencia de los fármacos convencionales.
Cita: Ma, G., Liu, R., Li, X. et al. Engineered bacterial therapy suppresses Enterohemorrhagic Escherichia coli through metabolic competition and virulence silencing. Nat Commun 17, 2307 (2026). https://doi.org/10.1038/s41467-026-69126-4
Palabras clave: probióticos diseñados, terapia para infecciones intestinales, EHEC, microbioma, microesferas para liberación de fármacos