Clear Sky Science · es
Un fosfaalumeno(3) aislable capaz de activar pequeñas moléculas mediante modos únicos de reactividad
Rompiendo enlaces resistentes con una nueva herramienta química
Los químicos buscan constantemente formas de convencer a moléculas reacias para que reaccionen. Muchas sustancias cotidianas, desde el hidrógeno gaseoso hasta el dióxido de carbono, son notablemente estables, lo que dificulta transformarlas en productos útiles. Este trabajo presenta una molécula recién diseñada, formada por aluminio y fósforo, que puede enganchar a esos socios reacios y abrir sus enlaces. Comprender y controlar este tipo de activación de enlaces podría, algún día, ayudar a convertir gases residuales en materias primas o proporcionar rutas más suaves y ahorradoras de metales para fabricar productos químicos finos y materiales.
Un enlace diseñado entre aluminio y fósforo
En el centro del estudio está un tipo raro de conexión entre dos elementos del grupo principal: aluminio y fósforo. Los investigadores sintetizaron una molécula, denominada «3» en el artículo, en la que estos dos átomos comparten un estrecho enlace doble. Para evitar que este par reactivo se desintegre, lo rodearon con un armazón orgánico voluminoso que lo protege de reacciones accidentales. Utilizando dos rutas sintéticas diferentes, obtuvieron este complejo en forma aislable y crecieron cristales únicos aptos para difracción de rayos X, confirmando que el fósforo está enlazado al aluminio mediante un vínculo corto, parecido a un doble enlace, mientras que cada átomo está estabilizado por ligandos circundantes que contienen nitrógeno. Cálculos mostraron que los electrones se comparten de forma desigual entre aluminio y fósforo, polarizando el enlace y dejándolo listo para ser atacado por otras moléculas.
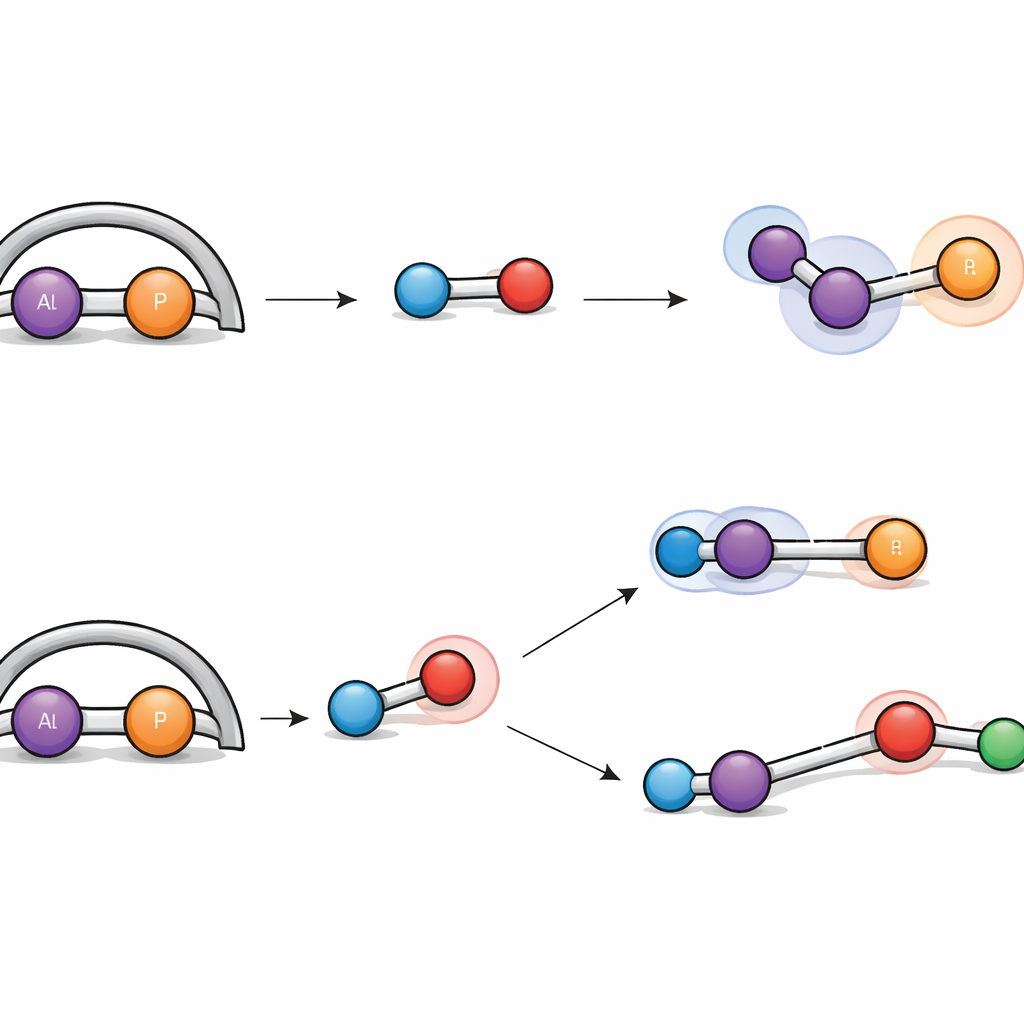
Cómo maneja la nueva molécula el gas hidrógeno
El hidrógeno gaseoso es famoso por ser difícil de dividir sin usar metales preciosos, sin embargo la nueva unidad aluminio‑fósforo consigue hacerlo. Cuando se expone a hidrógeno en condiciones suaves, el complejo reacciona de dos maneras distintas. En una vía, el enlace H–H simplemente se addiciona a través del doble enlace aluminio–fósforo, convirtiéndolo en dos enlaces sencillos y fijando un hidrógeno a cada átomo. En la otra, la molécula de hidrógeno se escinde de forma cooperativa por el aluminio y un átomo de nitrógeno vecino, un comportamiento que recuerda a los llamados «pares ácido‑base frustrados», que activan hidrógeno sin catalizadores metálicos tradicionales. Simulaciones detalladas mostraron ambas rutas y revelaron que sus barreras energéticas son similares, lo que explica por qué se forman ambos productos de forma concurrente.
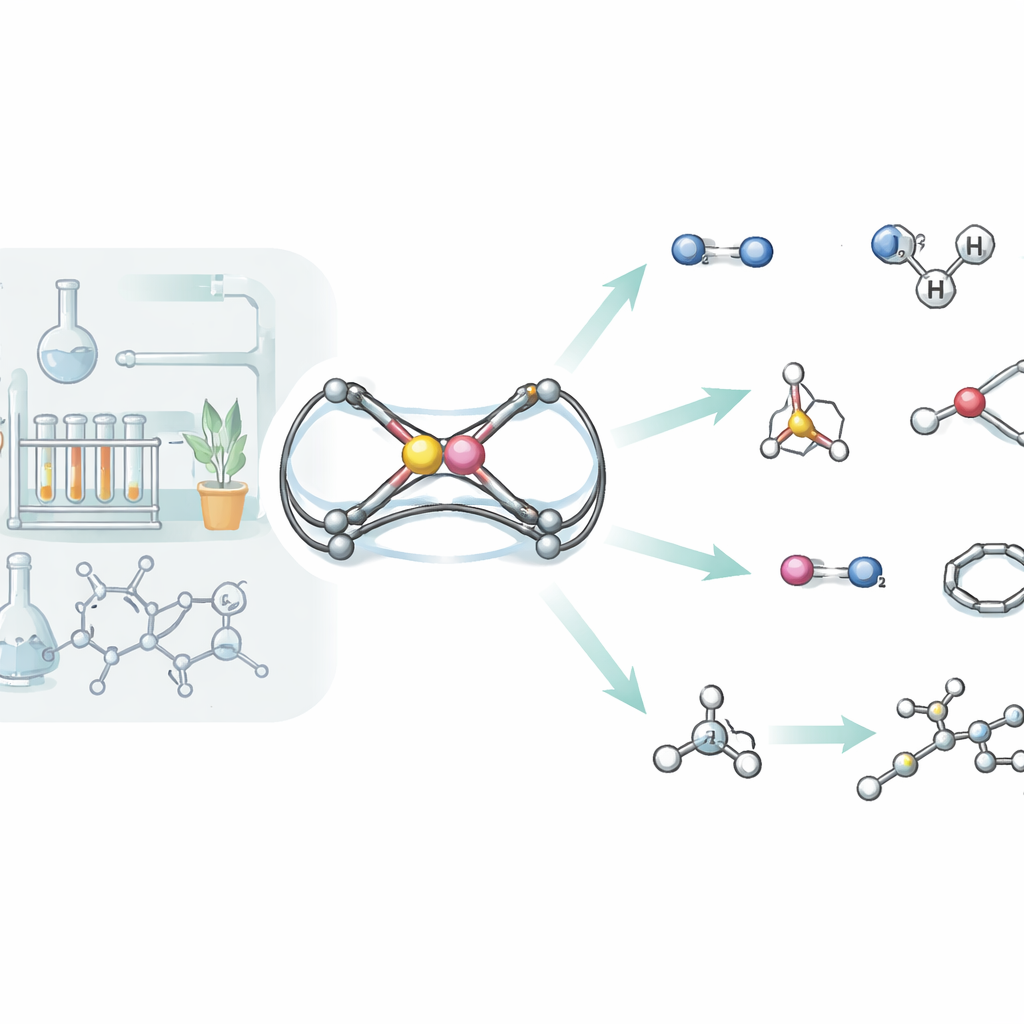
Desmontando una galería de pequeñas moléculas
El hidrógeno es solo el comienzo. El equipo probó sistemáticamente cómo reacciona su andamiaje aluminio‑fósforo con una amplia variedad de pequeñas moléculas, incluyendo fósforo blanco, isocianuros, dióxido de carbono, óxido nitroso, azida de trimetilsilio, dímeros de selenio, silanos, aminas, estireno y alquinos simples. En muchas de estas reacciones, el enlace original Al=P se rompe por completo, y los dos átomos terminan en estructuras mayores tipo jaula o anillo que incorporan fragmentos de la molécula entrante. Por ejemplo, el fósforo blanco (P4) se abre y se reconstruye en una jaula aluminio‑fósforo, mientras que el dióxido de carbono se inserta por duplicado para formar un anillo de seis miembros que une aluminio y fósforo mediante dos nuevos puentes carbono‑oxígeno. Con silanos y aminas, la molécula se comporta más bien como un doble enlace clásico: la unidad entrante Si–H o N–H se adiciona de forma ordenada sobre Al=P, demostrando de nuevo el carácter de «enlace π» de esta inusual conexión.
Por qué importa el armazón circundante
Una de las lecciones clave del trabajo es que el voluminoso y rico en nitrógeno armazón alrededor de la unidad Al=P no es solo un andamiaje; dirige cómo y dónde ocurren las reacciones. Comparando sus resultados con sistemas aluminio‑fósforo anteriores y de vida más corta, los autores muestran que pequeños cambios en los ligandos de soporte invierten el equilibrio entre distintas vías, como la adición simple sobre el doble enlace frente a la escisión de enlaces y la formación de anillos más elaborados. Análisis sofisticados de la distribución electrónica revelaron una fuerte polarización del enlace Al=P y destacaron cómo los átomos de nitrógeno vecinos pueden cooperar con el aluminio, especialmente en la activación del hidrógeno. La congestión estérica —la ocupación física por grupos voluminosos— también empuja a las moléculas entrantes hacia un sitio reactivo u otro.
Qué significa esto para la química futura
Para un no especialista, la sopa de siglas de reactivos en este estudio puede parecer remota, pero el mensaje subyacente es claro: ajustando cuidadosamente tanto el enlace como la forma alrededor de elementos del grupo principal, los químicos pueden construir herramientas ágiles que igualen o complementen a los catalizadores metálicos tradicionales. Este complejo aluminio‑fósforo aislable no solo se conserva en una botella, sino que también afronta un amplio conjunto de pequeñas moléculas resistentes en condiciones suaves, rompiendo hidrógeno, reorganizando el fósforo blanco y capturando dióxido de carbono. El trabajo muestra que cambios sutiles en el «asa» de una molécula pueden redirigir profundamente su reactividad, ofreciendo un plan para diseñar futuros catalizadores que ayuden a convertir moléculas simples y estables en productos más valiosos con precisión y eficiencia.
Cita: Cha, Y., Yang, Z., Zhuang, X. et al. An isolable phosphaalumene(3) capable of small molecule activation via unique modes of reactivity. Nat Commun 17, 2390 (2026). https://doi.org/10.1038/s41467-026-69118-4
Palabras clave: activación de pequeñas moléculas, química de elementos principales, enlace doble aluminio-fósforo, par ácido-base frustrado, mecanismos de activación de enlaces