Clear Sky Science · es
Mecanismo de inhibición de las glucano-sintasas fúngicas β−1,3 por fármacos antifúngicos triterpenoides
Por qué importa frenar las infecciones fúngicas
Las infecciones fúngicas silenciosamente matan a más de un millón de personas cada año y amenazan cultivos y ecosistemas en todo el mundo. Los médicos ya lidian con una lista reducida de medicamentos antifúngicos, y algunos hongos peligrosos están evolucionando para eludirlos. Este estudio revela, con detalle molecular, cómo una nueva clase de fármacos antifúngicos se adhieren y desactivan una enzima clave que los hongos necesitan para construir su pared celular protectora. Entender este proceso ofrece una hoja de ruta para diseñar tratamientos mejores que puedan superar a los hongos resistentes.
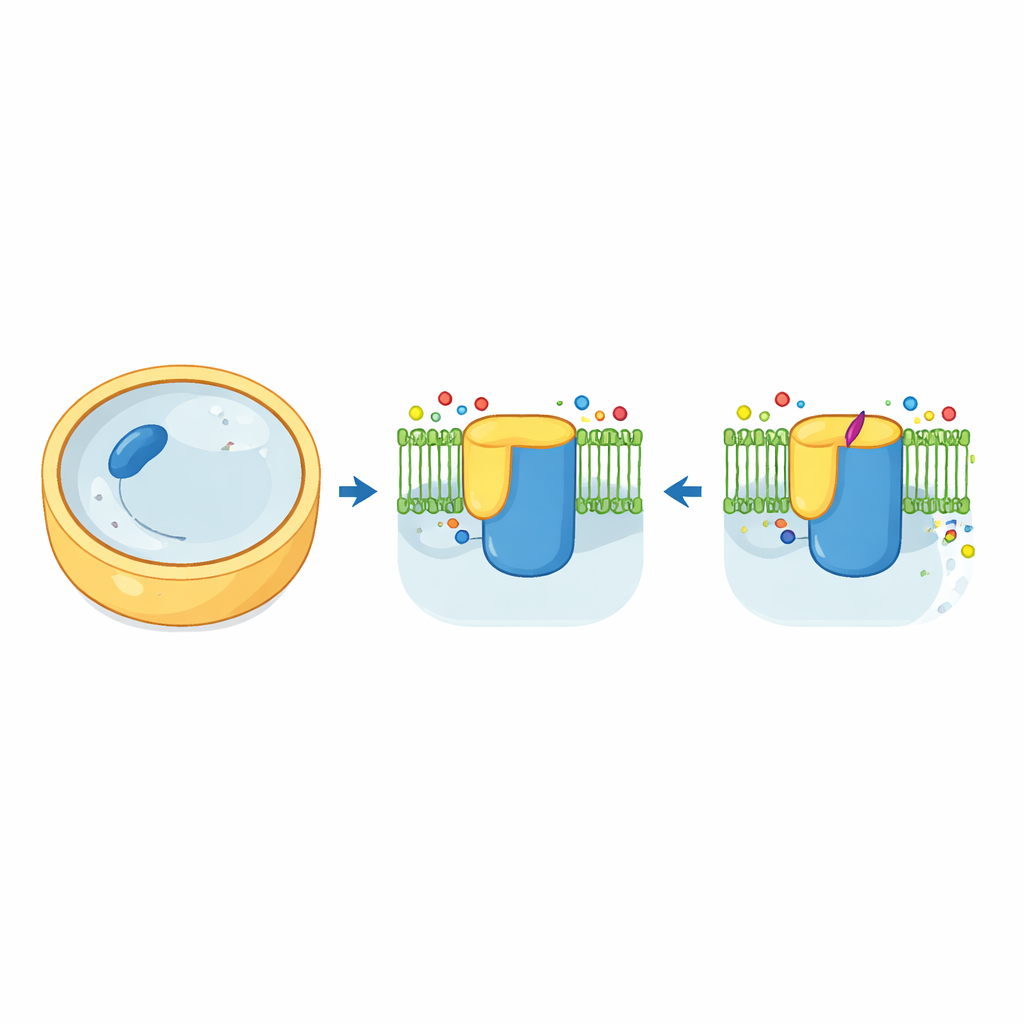
El fabricante de ‘ladrillos’ de la pared celular fúngica
Las células fúngicas están recubiertas por una pared resistente compuesta en gran parte por un polímero de azúcar llamado beta-1,3-glucano. La enzima que fabrica y exporta este polímero, conocida como beta-1,3-glucano-sintasa, actúa como una combinación de fabricante de ladrillos y cinta transportadora. En la levadura de panadería, esta máquina se construye a partir de dos versiones muy similares, Fks1 y Fks2, cada una incrustada en la membrana celular y controlada por una pequeña proteína auxiliar llamada Rho1. Usando crio-microscopía electrónica, los autores capturaron vistas tridimensionales de alta resolución de Fks1 y Fks2 en su forma natural. Las estructuras revelan un gran “banco de trabajo” citosólico unido a un bosque de hélices que atraviesan la membrana, con una cavidad central que probablemente sirve como túnel por el que la cadena de glucano en crecimiento sale de la célula.
Cómo un producto natural toma la enzima
Los fármacos triterpenoides de importancia clínica, incluido el medicamento oral ibrexafungerp, tienen su origen en un compuesto natural llamado enfumafungina. Hasta ahora, nadie sabía exactamente dónde se unen estos fármacos en la glucano-sintasa. Los investigadores resolvieron las estructuras de Fks1 y Fks2 unidas a la enfumafungina. Sorprendentemente, el fármaco no se incrusta en el sitio activo donde se unen las unidades de azúcar. En su lugar, se acopla en la porción externa de una única hélice transmembrana llamada TM5, situada en la membrana a unos tres nanómetros del centro catalítico y cerca del probable canal de salida del glucano. Aminoácidos clave en este parche acunan el núcleo hidrofóbico del fármaco y contactan su cola ácida, mientras que su apéndice de azúcar apenas toca la proteína —lo que explica por qué los químicos han podido modificar esa parte sin perder potencia.
Fármacos que congelan una máquina en movimiento
A primera vista, la forma general de la enzima con y sin enfumafungina parece casi inalterada. La diferencia crucial radica en cómo se organizan los lípidos circundantes y en la flexibilidad de ciertas hélices. Cuando el fármaco se une, una cadena lateral aromática cercana rota para sujetar la enfumafungina en su sitio y, junto con otro residuo, estabiliza un lípido ordenado junto al fármaco. Lípidos adicionales con aspecto de esteroles se disponen ordenadamente alrededor de un conjunto de hélices horizontales que ayudan a definir la ruta de exportación del glucano. Estos lípidos actúan como cuñas y soportes, bloqueando las hélices y la entrada del canal en una determinada disposición “basal”. Pruebas genéticas muestran que alterar muchos de los puntos de contacto para el fármaco o estos esteroles debilita la unión del fármaco o destruye la función enzimática, y las mutaciones en estos sitios coinciden con mutaciones de resistencia conocidas en patógenos humanos y vegetales.
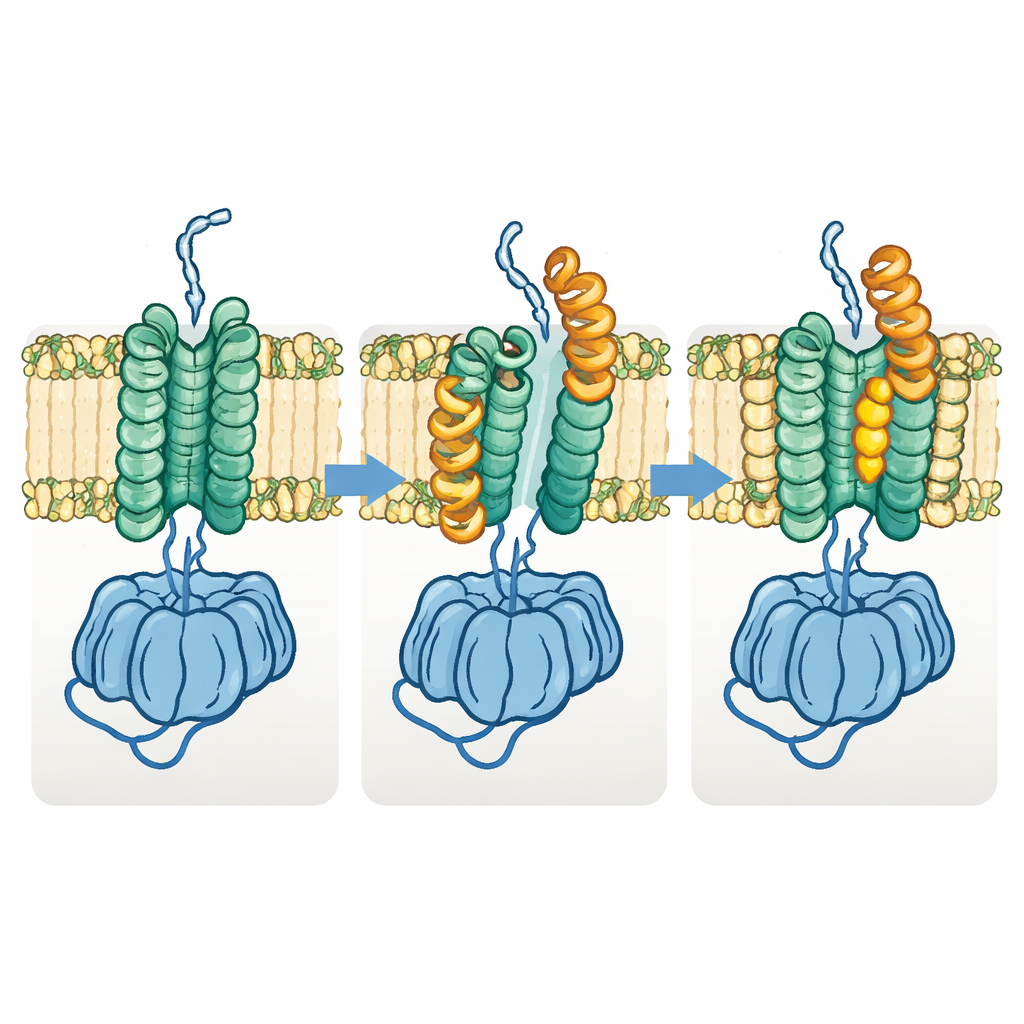
Un cambio de forma necesario para el transporte del polímero
El equipo también descubrió una forma distinta “abierta” de Fks1. En este estado, una mitad de la región de membrana se desplaza lateralmente y hélices horizontales clave se abren hacia afuera, separando el espacio entre los dos haces de membrana y ensanchando el aparente túnel del glucano. La comparación de muchas estructuras sugiere que la enzima alterna entre los estados basal y abierto durante su funcionamiento normal: el estado basal prepara e inicia la formación del polímero, mientras que el estado abierto permite que la cadena en crecimiento se desplace lateralmente a través de la membrana hacia el exterior. Cuando los autores diseñaron enlaces disulfuro destinados a bloquear permanentemente la enzima en cualquiera de los dos estados, ambas variantes perdieron en gran medida la actividad, lo que apoya la idea de que este cambio de forma es esencial para la función.
Qué significa esto para futuros fármacos antifúngicos
Al mostrar que la enfumafungina y fármacos relacionados no actúan bloqueando el bolsillo catalítico sino remodelando el entorno lipídico local y congelando la glucano-sintasa en su estado basal, este estudio revela un modo de acción de fármaco no convencional. También demuestra que Fks1 y Fks2 comparten estructuras y respuestas al fármaco casi idénticas, lo que explica por qué ambos deben considerarse al abordar la resistencia. En un sentido más amplio, el trabajo pone de manifiesto cómo pequeñas moléculas pueden controlar proteínas de membrana “difíciles de atacar” uniéndose a superficies poco profundas y reclutando lípidos, ofreciendo un plano conceptual para diseñar antifúngicos de nueva generación que sigan siendo efectivos incluso cuando los hongos evolucionan.
Cita: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
Palabras clave: fármacos antifúngicos, pared celular fúngica, glucano-sintasa, resistencia a fármacos, crio-microscopía electrónica