Clear Sky Science · es
Estructuras por crio‑EM de intermediarios del ensamblaje portal‑cuello del bacteriófago T4 revelan un mecanismo de retención del genoma viral
Cómo un virus mantiene su ADN bajo presión
El bacteriófago T4 es un virus que infecta la bacteria E. coli y empaqueta su ADN tan densamente en su cabeza que la presión interior puede ser de cinco a siete veces la de una botella de champán. Aun así, el ADN no se fuga mientras el virus completa el resto de su estructura. Este estudio revela, con detalle molecular, cómo el T4 resuelve ese problema utilizando una diminuta doble puerta que actúa como un esclusa para su material genético.
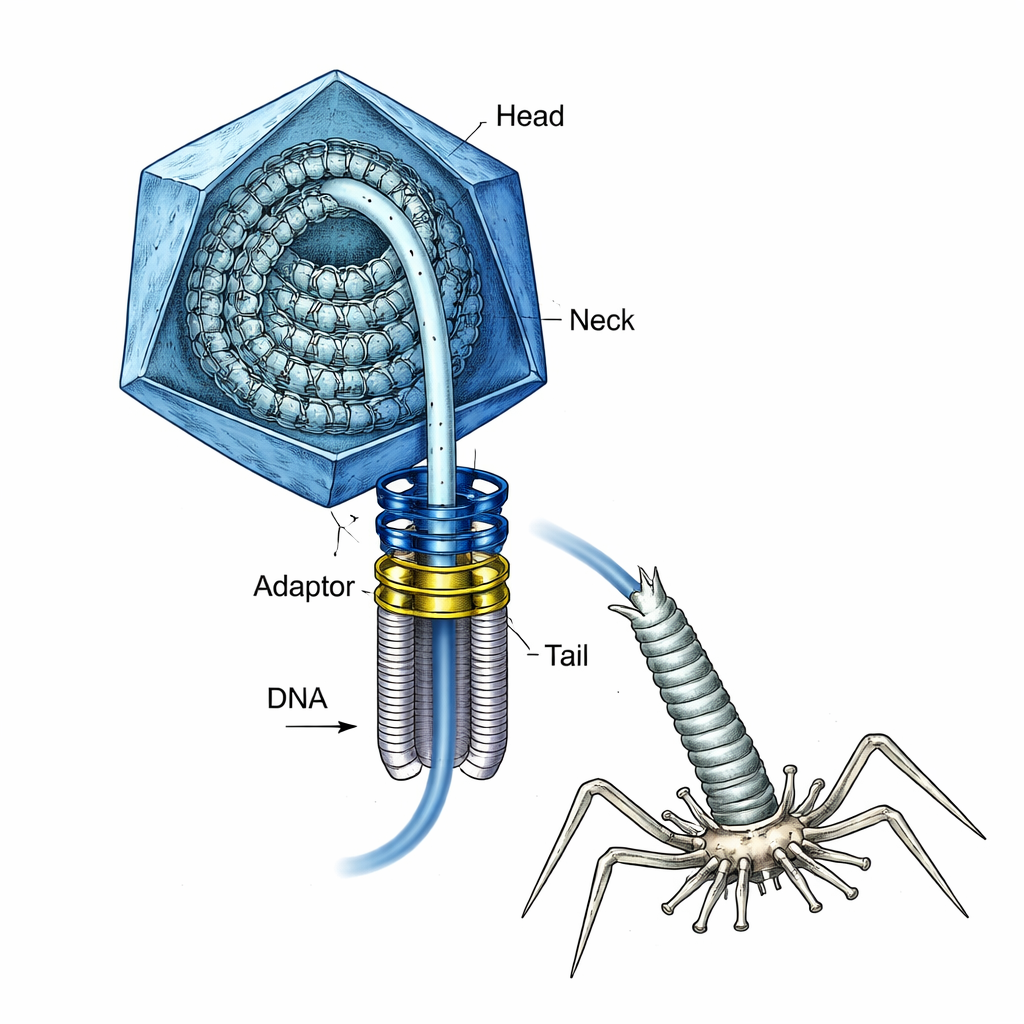
El virus con un resorte cargado en su interior
El T4 ha sido durante mucho tiempo una herramienta fundamental de la biología molecular y también es un modelo para construir futuras vacunas y vectores de entrega génica. Durante el ensamblaje, el virus primero construye una cápside proteica vacía, o cabeza, y un “portal” anular especial en un vértice. Un potente motor molecular enrolla el ADN en la cabeza a través de ese portal hasta que la cabeza está “llena”. En ese momento, el motor debe desprenderse, hay que unir un cuello y una cola, y más tarde el ADN debe inyectarse en una bacteria—todo sin permitir que el ADN presurizado salga de forma prematura. Cómo el virus mantenía este ADN tan tensionado de forma segura durante esas transiciones no se comprendía bien.
Reconstruir el cuello en el laboratorio
Los investigadores recrearon piezas clave del T4 en bacterias y las mezclaron de forma controlada para observar cómo se ensambla el cuello—el conector entre la cabeza y la cola. Dos proteínas virales, llamadas gp13 y gp14, se produjeron por separado. Por sí solas flotaban como unidades individuales, pero juntas encajaron en anillos apilados que forman un túnel central para el paso del ADN. Para sorpresa de los científicos, una tercera proteína apareció de forma recurrente en estas preparaciones: Hfq, una proteína bacteriana bien conocida que normalmente ayuda a controlar el ARN y la actividad génica en E. coli. La espectrometría de masas confirmó que Hfq se unía específicamente a gp14, lo que sugiere que el virus toma prestada esta proteína del huésped como parte de su cuello.
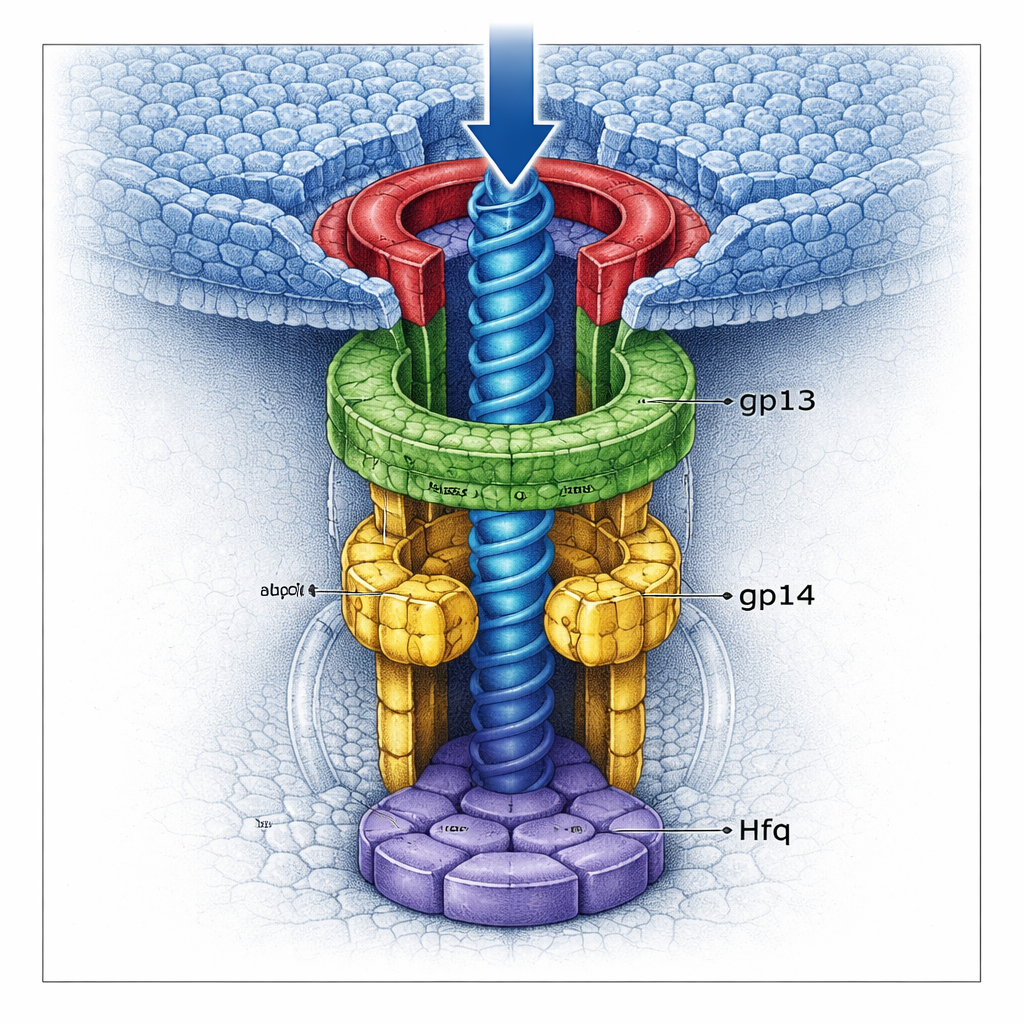
Una doble puerta que encierra el genoma
Usando crio‑microscopía electrónica de alta resolución, el equipo visualizó varias versiones del complejo del cuello con detalle casi atómico. Encontraron que gp13 forma un anillo amplio que se adapta al portal, mientras que gp14 se sitúa debajo como un hexámero, creando un canal más estrecho. Crucialmente, cada subunidad de gp14 aporta un lazo largo que se proyecta hacia el centro del túnel. Juntos, seis de esos “lazos tapones” forman una compuerta ajustada que puede atrapar el último segmento de ADN cuando intenta salir de la cabeza. Debajo de gp14, la proteína Hfq secuestrada se ensambla en su propio hexámero, taponando la base del canal como una segunda puerta. Cuando Hfq está presente, la estructura gp13–gp14 está más completa y rígida, y las compuertas combinadas constriñen aún más el túnel, haciendo mucho menos probable la fuga de ADN.
Sincronización, a prueba de errores y una ayudante prestada
El estudio también muestra que este sistema es más que un tapón estático; es una secuencia cuidadosamente coreografiada de cambios conformacionales. Una vez que la cabeza está llena, la presión interna empuja al portal hacia una nueva conformación que expone sitios de unión para gp13. Un cuello preensamblado gp13–gp14–Hfq se acopla entonces al portal. Gp13 se flexiona, se eleva y se asegura tanto al portal como a la cáscara exterior, integrando firmemente el cuello en la cabeza. A lo largo de esta fase, los lazos tapones de gp14 y el tapón Hfq mantienen el ADN en su sitio. Hfq desempeña un segundo papel como factor de control de calidad: al ocupar superficies clave en gp14, impide que gp14 se una al portal en la posición equivocada, lo que evitaría el ensamblaje defectuoso del cuello. Solo cuando llega la cola preconstruida, una proteína de la punta de la cola, gp15, forma un enlace aún más fuerte con gp14, desplazando a Hfq y abriendo el paso para la liberación controlada del ADN hacia la cola.
Por qué importa más allá de un virus
En términos sencillos, el T4 usa un cerrojo de dos puertas para contener un poderoso “resorte” de ADN mientras completa el resto del virus. La primera puerta está hecha de su propia proteína del cuello, gp14, y la segunda puerta se toma prestada de la proteína Hfq del huésped, que el virus utiliza temporalmente y luego desecha. Esta doble compuerta asegura que casi no se pierda ADN y que el virus final sea plenamente infeccioso. Dado que muchos virus grandes empaquetan sus genomas bajo presiones extremas similares y comparten arquitecturas relacionadas, este trabajo sugiere que sistemas de compuerta comparables, e incluso el secuestro temporal de proteínas del huésped, pueden ser frecuentes. Comprender estos mecanismos podría orientar el diseño de vectores virales más seguros para la medicina y señalar nuevas formas de bloquear virus dañinos apuntando a sus “cerraduras” genómicas.
Cita: Han, L., Mao, Q., Zhu, J. et al. Cryo-EM structures of bacteriophage T4 portal-neck assembly intermediates reveal a viral genome retention mechanism. Nat Commun 17, 1964 (2026). https://doi.org/10.1038/s41467-026-69107-7
Palabras clave: bacteriófago T4, ensamblaje viral, crio‑microscopía electrónica, empaque del genoma, interacción huésped–virus