Clear Sky Science · es
ILC1s CD127+ en el tejido adiposo inducidos por peritonitis aguda expresan PD-L1 y atenúan la inflamación en ratones
Por qué la grasa abdominal puede ayudar a combatir una infección mortal
Cuando las bacterias se filtran desde un intestino desgarrado hacia la cavidad abdominal, el organismo puede entrar en una condición potencialmente letal llamada sepsis. Este estudio revela un aliado inesperado en esa batalla: un conjunto especial de células inmunitarias que se ocultan en la grasa abdominal, que migran hacia la zona durante la fase temprana de la infección y actúan como un freno incorporado frente a la inflamación descontrolada. Comprender cómo funcionan estas células podría inspirar nuevos tratamientos que calmen las infecciones peligrosas sin apagar por completo el sistema inmunitario.
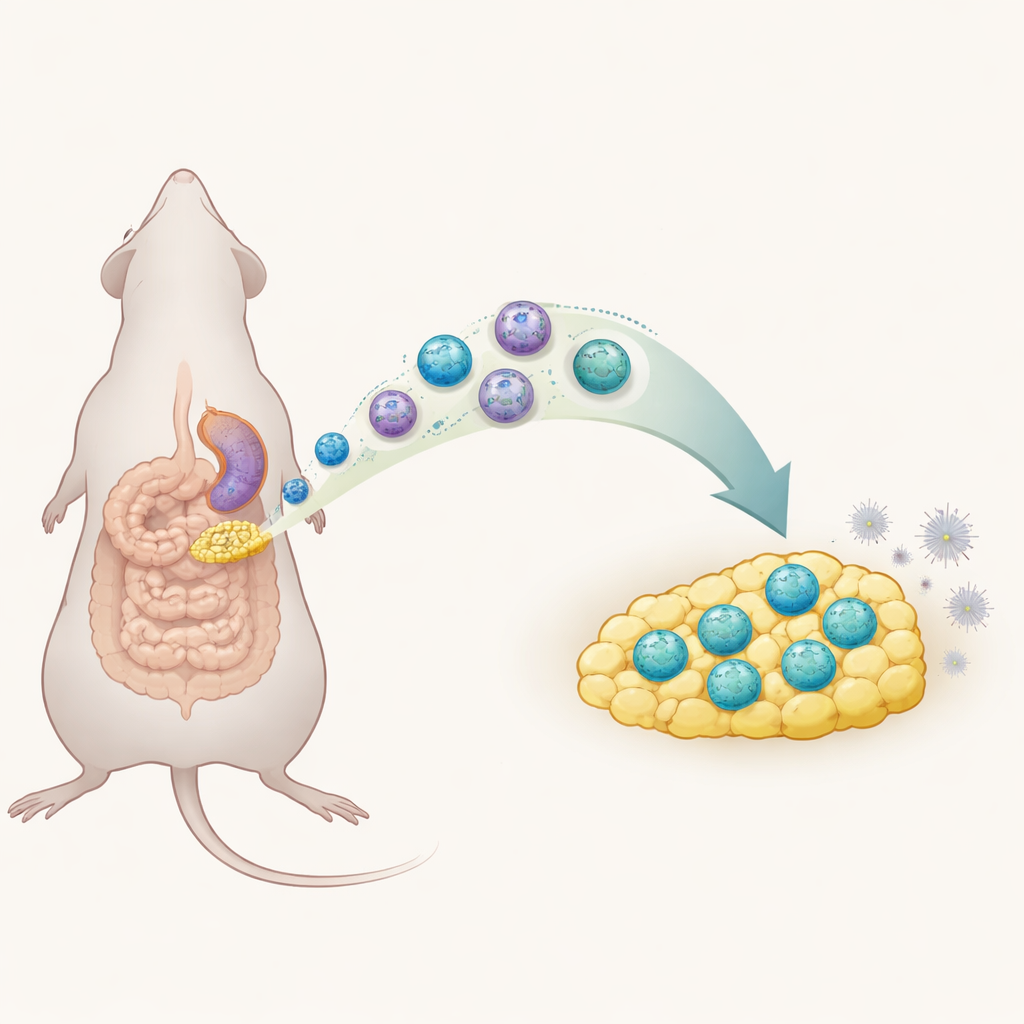
Una filtración peligrosa en el abdomen
La peritonitis ocurre cuando el revestimiento del abdomen se inflama, con mayor frecuencia porque las bacterias se derraman desde un intestino perforado. Si esta primera tormenta de inflamación no se controla, los pacientes pueden desarrollar sepsis, que aún hoy mata aproximadamente a una de cada cinco personas afectadas a pesar de los cuidados modernos. Los médicos pueden tratar la infección con cirugía y antibióticos, pero disponen de pocas herramientas para reconducir la propia reacción inmune del cuerpo y evitar que entre en sobreactivación perjudicial. La grasa que cubre los intestinos, denominada tejido adiposo mesentérico, es conocida por movilizarse hacia los sitios de daño intestinal, lo que sugiere que desempeña un papel activo en esta respuesta inmune temprana.
Guardianes ocultos en la grasa abdominal
En años recientes, los científicos han descubierto las “células linfoides innatas”, centinelas inmunitarias de acción rápida que viven en muchos tejidos. Un subtipo, llamado ILC1 de grupo 1, normalmente ayuda a desencadenar reacciones inflamatorias intensas. En este estudio con ratones, los investigadores usaron un modelo quirúrgico estándar de peritonitis para investigar cómo se comportan estas células en la grasa mesentérica. Encontraron que, seis horas después de la lesión, esta grasa se iluminó con señales inflamatorias y una oleada de células ILC1, mientras que otros tipos celulares relacionados apenas cambiaron. Este momento coincidía con el pico de enfermedad en los animales, lo que sugiere que las ILC1 estaban estrechamente ligadas a la fase inflamatoria temprana en el abdomen.
Células viajeras que cambian su naturaleza
Ahondando más, el equipo empleó perfiles avanzados de una sola célula para dividir la población de ILC1 en subgrupos. En condiciones normales, la mayoría de las ILC1 de la grasa abdominal carecían de una molécula llamada CD127 en su superficie. Sin embargo, durante la peritonitis aguda apareció y se expandió un nuevo grupo de ILC1 CD127‑positivas. Estas recién llegadas producían menos de la potente señal inflamatoria interferón‑gamma que sus homólogas CD127‑negativas, lo que las señalaba como inusualmente reprimidas. Los científicos mostraron que muchas de estas células no simplemente se dividían in situ: en cambio, ILC1 del bazo viajaban por el torrente sanguíneo hasta la grasa mesentérica, guiadas en parte por una señal química de “homing” llamada CXCL10 y su receptor asociado CXCR3. Una vez en la grasa, cambiaban sus marcadores de superficie, adquiriendo CD127 y adoptando esta personalidad más tranquila y reguladora.
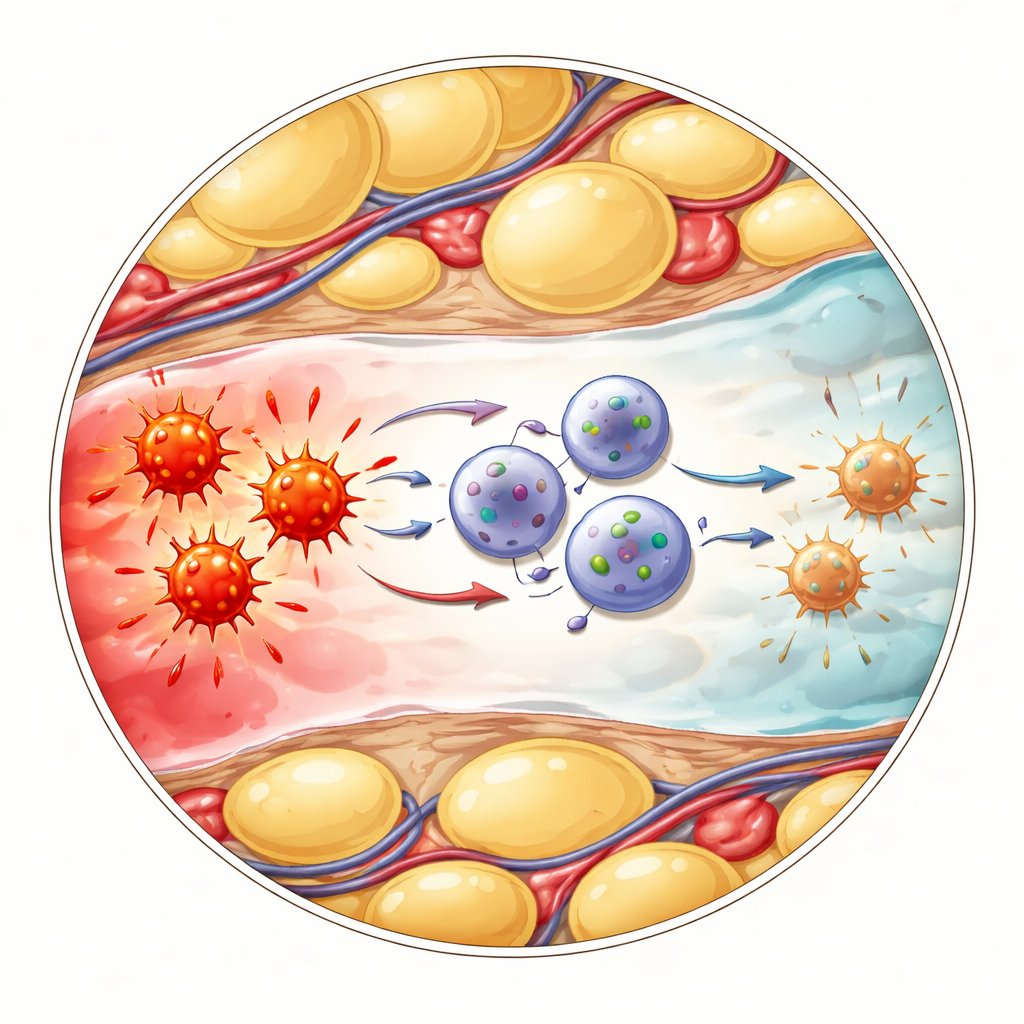
Cómo las células calmantes hablan con las células inflamatorias
La pregunta siguiente fue cómo estas ILC1 alteradas realmente mitigaban la inflamación. Los investigadores se centraron en otro grupo inmunitario llamado células T gamma‑delta, que responden rápidamente al peligro y pueden liberar grandes cantidades de la molécula de alarma TNF. Los análisis de una sola célula sugirieron que las ILC1 CD127‑positivas y las células T gamma‑delta interaccionan mediante una vía de “freno” bien conocida que implica las proteínas de superficie PD‑L1 y PD‑1. En la grasa abdominal inflamada, las ILC1 recién llegadas aumentaron fuertemente PD‑L1, mientras que las células T gamma‑delta cercanas mostraron altos niveles de PD‑1. Cuando el equipo bloqueó PD‑1 con anticuerpos, las células T gamma‑delta secretaron más TNF, confirmando que este contacto normalmente restringe su producción inflamatoria. De forma similar, los ratones genéticamente modificados para carecer de ILC1 sufrieron una enfermedad más grave, con mayores marcadores inflamatorios y más TNF procedente de las células T gamma‑delta—efectos que pudieron mitigarse bloqueando directamente el TNF.
Qué significa esto para futuros tratamientos
Conjuntando estos hallazgos, los autores proponen un eje “bazo‑a‑grasa‑abdominal”: poco después de que las bacterias se filtren en el abdomen, las ILC1 salen del bazo, se dirigen al tejido adiposo mesentérico y allí se transforman en células ricas en CD127 y PD‑L1 que atenúan la producción de TNF por parte de las células T gamma‑delta. En lugar de avivar el fuego, estas ILC1 especializadas actúan como pacificadoras locales, impidiendo que la inflamación se desborde y ayudando posiblemente a que la peritonitis no progrese hacia una sepsis mortal. A largo plazo, fármacos que refuercen o imiten este circuito regulador en la grasa abdominal podrían ofrecer una nueva forma de tratar infecciones graves: modular la respuesta inmune para que siga siendo lo bastante fuerte como para combatir los gérmenes, pero no tan intensa que ponga en peligro al paciente.
Cita: Nagata, R., Akama, Y., Goncalves, P. et al. Acute peritonitis-induced adipose CD127+ ILC1s express PD-L1 and ameliorate inflammation in mice. Nat Commun 17, 2391 (2026). https://doi.org/10.1038/s41467-026-69100-0
Palabras clave: peritonitis, células linfoides innatas, tejido adiposo mesentérico, regulación inmune, sepsis