Clear Sky Science · es
Reutilizar receptores nucleares para la formación de condensados líquidos dependientes de ligando y la regulación génica
Convertir hormonas en interruptores celulares bajo demanda
Nuestras células están constantemente atendiendo señales como hormonas y vitaminas y las traducen en acciones, por ejemplo activando o silencian genes. Este estudio muestra cómo los científicos pueden aprovechar ese lenguaje natural para construir “interruptores” sintéticos que respondan a señales reales del organismo e incluso formen diminutas gotas líquidas dentro de las células para potenciar la actividad génica. Esos interruptores controlados por hormonas podrían algún día ayudar a crear terapias génicas más inteligentes, biosensores precisos o fármacos vivos estrechamente acoplados a la fisiología del paciente.
Usar los propios lectores de señales de la célula
Las hormonas y moléculas relacionadas son detectadas por una familia de proteínas llamadas receptores nucleares, que normalmente residen en las células y controlan genes en respuesta a señales como la hormona tiroidea, la vitamina D, el estrógeno y el cortisol. Cada receptor tiene una cavidad que enlaza su hormona específica y una superficie que recluta proteínas auxiliares, llamadas coactivadores, cuando la hormona está presente. En lugar de diseñar piezas totalmente artificiales, los investigadores reutilizaron estos receptores naturales y un pequeño fragmento de una proteína coactivadora humana (un péptido corto de TIF2) como bloques modulares. Esta elección hace que sus interruptores sintéticos hablen el mismo lenguaje bioquímico del organismo, facilitando su integración en vías de señalización existentes.
Construir interruptores químicos de encendido/apagado
El equipo demostró primero que la unión de la hormona podía reunir bajo demanda dos fragmentos proteicos diseñados. Fusionaron la región de unión al ligando de varios receptores nucleares a una mitad de una enzima reportera partida y conectaron el péptido TIF2 a la otra mitad. En células humanas, añadir la hormona correspondiente hizo que las dos mitades se encontraran, restaurando el brillo del reportero, mientras que eliminar o bloquear la hormona rompía la conexión. Al emparejar receptores con sus fármacos activadores (agonistas) y bloqueantes (antagonistas), construyeron interruptores de dos entradas que podían activarse con un compuesto y desactivarse con otro, a veces de forma repetida y en minutos. También usaron esta estrategia para mover enzimas a lugares específicos dentro de las células, cambiando niveles químicos locales bajo demanda.
Controlar genes con contactos multiplicados
Para convertir estos interruptores en controladores génicos, los investigadores los conectaron a una plataforma de unión al ADN basada en CRISPR. Una proteína Cas9 “muerta” (dCas9) era dirigida a sitios de ADN escogidos, mientras el receptor nuclear llevaba un dominio fuerte activador de genes. Cuando se añadía la hormona, el receptor se unía a segmentos de TIF2 acoplados a dCas9, llevando el activador al gen objetivo. Un solo segmento de TIF2 producía efectos modestos, pero encadenar muchas copias creó una plataforma multivalente capaz de reclutar muchos receptores a la vez. Esto amplificó drásticamente la activación génica—hasta cientos de veces por encima de la línea base—y la respuesta se mantuvo sensible dentro de rangos hormonales similares a los que se encuentran en el organismo. Los antagonistas podían reducir esta actividad de forma contundente, demostrando un control reversible y preciso.
Crear gotas líquidas que turboalimentan la expresión
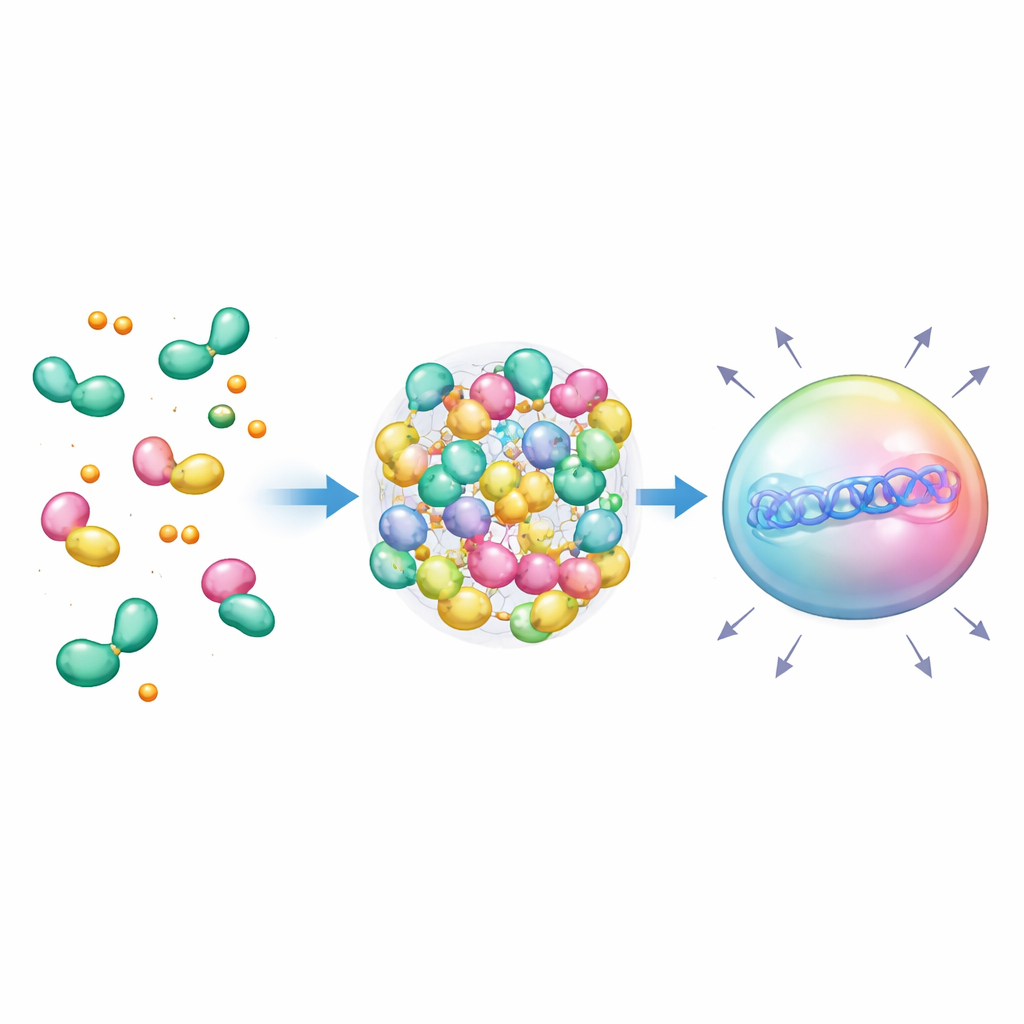
Al aumentar el número de copias de TIF2, el equipo observó un umbral marcado en el rendimiento, lo que sugería que las proteínas podrían condensarse en gotas. Muchos reguladores génicos naturales forman “condensados” de tipo líquido que concentran la maquinaria necesaria para la transcripción. Los investigadores diseñaron intencionadamente andamios que agrupan muchos motivos TIF2 mediante péptidos enrollados en hélice (coiled-coil), favoreciendo que múltiples receptores se empaqueten en el mismo lugar cuando la hormona está presente. En células vivas, esto produjo gotas brillantes y esféricas que se comportaban como líquidos: se fusionaban, recuperaban fluorescencia tras fotoblanqueo y podían disolverse con químicos que interrumpen interacciones proteicas débiles. Es importante que las gotas solo aparecían bajo las condiciones multivalentes y hormonales adecuadas, y los antagonistas podían hacerlas desaparecer, demostrando que la formación de gotas era químicamente modulable.
De gotas diseñadas a futuras terapias
Al fusionar estos condensados controlados por hormonas con herramientas CRISPR dirigidas al ADN, los autores crearon condensados nucleares que se sitúan directamente sobre genes específicos y amplifican su actividad de forma masiva—even cuando solo hay un único sitio de anclaje en el ADN. Dado que los componentes provienen de humanos y responden a señales familiares como el cortisol y el estrógeno, estos sistemas podrían en última instancia conectarse a circuitos terapéuticos que respondan automáticamente a los niveles hormonales del paciente. Aunque será necesario un ensayo cuidadoso para evitar interferencias con los propios receptores del organismo, este trabajo ilustra un concepto potente: reutilizar los lectores hormonales naturales y los condensados líquidos como interruptores programables para detectar la química interna y dirigir respuestas génicas a medida.
Cita: Rihtar, E., Fink, T., Ivanovski, F. et al. Repurposing nuclear receptors for ligand-responsive liquid condensate formation and gene regulation. Nat Commun 17, 2218 (2026). https://doi.org/10.1038/s41467-026-69099-4
Palabras clave: biología sintética, receptores nucleares, señalización hormonal, regulación génica, separación de fases