Clear Sky Science · es
Una estrategia sintética combinatoria para desarrollar agentes de transporte de proteínas de edición genómica dirigidos a la retina de ratón
Nueva esperanza para tratar la ceguera hereditaria
Muchas formas de ceguera hereditaria comienzan con un único gen defectuoso en las células sensibles a la luz en la parte posterior del ojo. Herramientas modernas de edición genética como CRISPR pueden, en principio, corregir estos errores, pero introducir de forma segura la maquinaria de edición en las células adecuadas ha sido un gran obstáculo. Este estudio describe una nueva forma de transportar potentes editores genéticos directamente a la retina de ratón usando partículas especialmente diseñadas con comportamiento similar a las grasas, lo que abre la posibilidad de tratamientos únicos que restauren la visión en personas con enfermedades oculares genéticas.
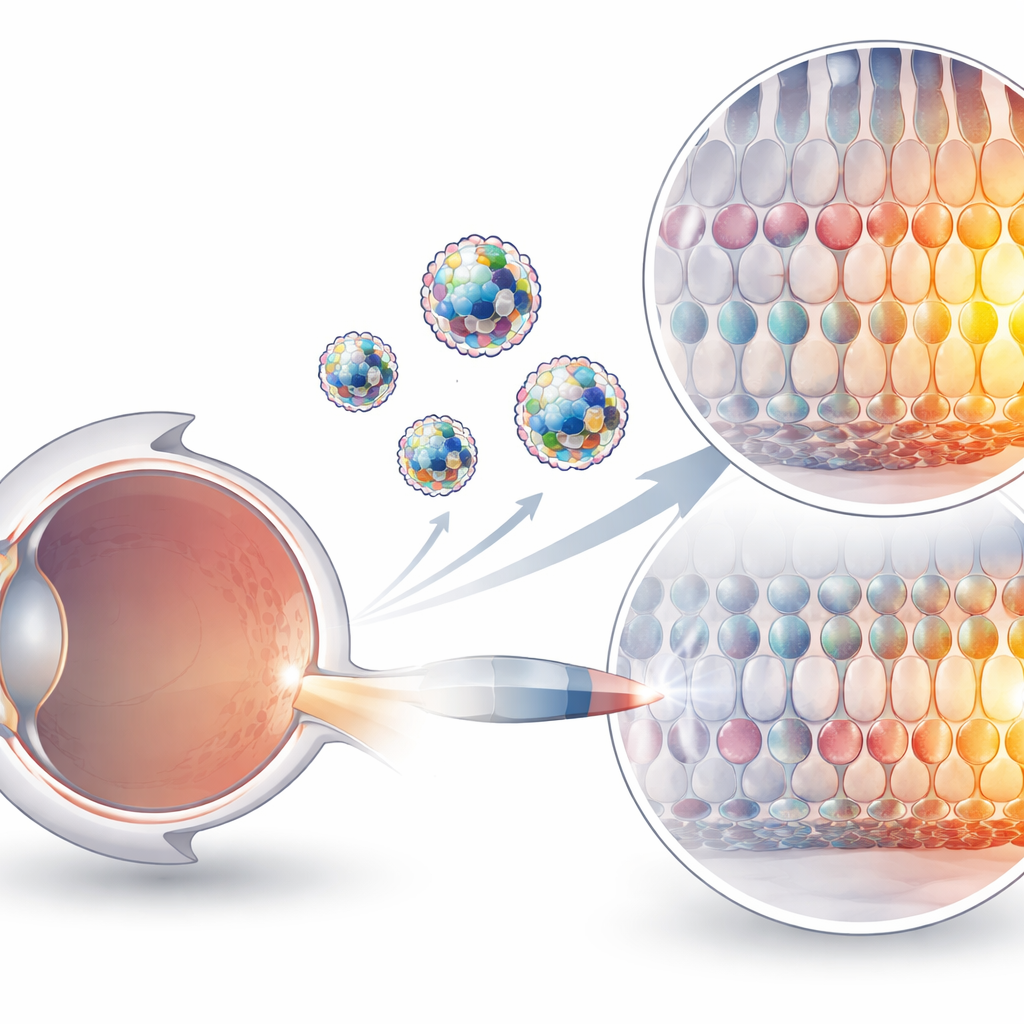
Por qué es tan difícil entregar editores genéticos
Las herramientas basadas en CRISPR pueden ahora cambiar letras individuales del ADN sin cortar ambas hebras, un avance que las hace atractivas para tratar trastornos genéticos. Pero estas herramientas son aparatosos complejos proteína–ARN, cargados eléctricamente y frágiles en el organismo. Los métodos de entrega actuales dependen en gran medida de virus modificados o de partículas que transportan los planos genéticos del editor en lugar del editor en sí. Los virus pueden provocar reacciones inmunitarias y tienen límites estrictos de tamaño, mientras que la entrega de ARNm funciona muy bien en el hígado pero sigue siendo ineficiente en muchos otros tejidos, incluido el ojo. Inyectar directamente los complejos proteína–ARN ya ensamblados es, en teoría, más limpio y seguro, pero han carecido de un vehículo adecuado que les ayude a cruzar las membranas celulares y alcanzar sus objetivos.
Un transbordador inspirado en un tinte para proteínas
Los investigadores partieron de un punto de partida inesperado: el Coomassie Brilliant Blue, un tinte azul intenso comúnmente usado en laboratorios de biología y ya aprobado para ciertas cirugías oculares. Este tinte se une fuertemente a muchas proteínas. El equipo vinculó químicamente “cabezas” de Coomassie a “colas” con comportamiento similar a lípidos para crear una familia de nuevas moléculas llamadas lipidoides. En agua, estos lipidoides tienden a agruparse en partículas, con las partes oleosas enterradas en el interior y los grupos Coomassie expuestos en el exterior, donde pueden capturar proteínas. Al variar la longitud, ramificación y carga de las colas, los científicos construyeron docenas de compuestos candidatos diseñados para unirse a proteínas de edición genética por un lado e interactuar con las membranas celulares por el otro.
Pruebas de entrega de proteínas a las células oculares
Para ver qué diseños funcionaban realmente, el grupo usó primero una proteína de prueba simple llamada Cre recombinasa que invierte un interruptor genético de verde a rojo o de rojo a verde en células y ratones diseñados. Varios lipidoides de Coomassie transportaron Cre de forma eficiente a células en cultivo, convirtiendo grandes fracciones de células de verde a rojo. Cuando se inyectaron bajo la retina de ratones reporteros, los compuestos seleccionados desencadenaron cambios de color sorprendentes tanto en la capa de pigmento que sustenta la visión como en los fotorreceptores sensibles a la luz, demostrando que las proteínas alcanzaron las propias células más afectadas en muchas enfermedades que causan ceguera. Estos experimentos iniciales también revelaron que cambios sutiles en la estructura del lipidoide podían modificar qué tipos celulares se dirigían, lo que sugiere que versiones futuras podrían ajustarse para capas retinianas particulares.
Potenciar la edición genética y rescatar la visión
A continuación, el equipo cargó su sistema con un editor de bases de adenina, una variante refinada de CRISPR que puede corregir la mutación de una sola letra específica que causa pérdida de visión en ratones rd12, un modelo de ceguera infantil grave. Por sí solo, el complejo proteína–ARN del editor penetraba mal en las células. Un lipidoide, llamado CBB11, mejoró la entrega pero tendía a agregarse en solución. Para estabilizarlo, los investigadores incorporaron CBB11 en liposomas pequeños y bien definidos—esferas huecas hechas de varios tipos de lípidos, incluidos componentes de uso clínico procedentes de vacunas de ARNm. En estas formulaciones, CBB11 en la superficie del liposoma capturaba la parte proteica del editor, mientras que otros lípidos ayudaban a unir la guía de ARN, creando una capa cooperativa que mantuvo todo el complejo en el exterior de la partícula.
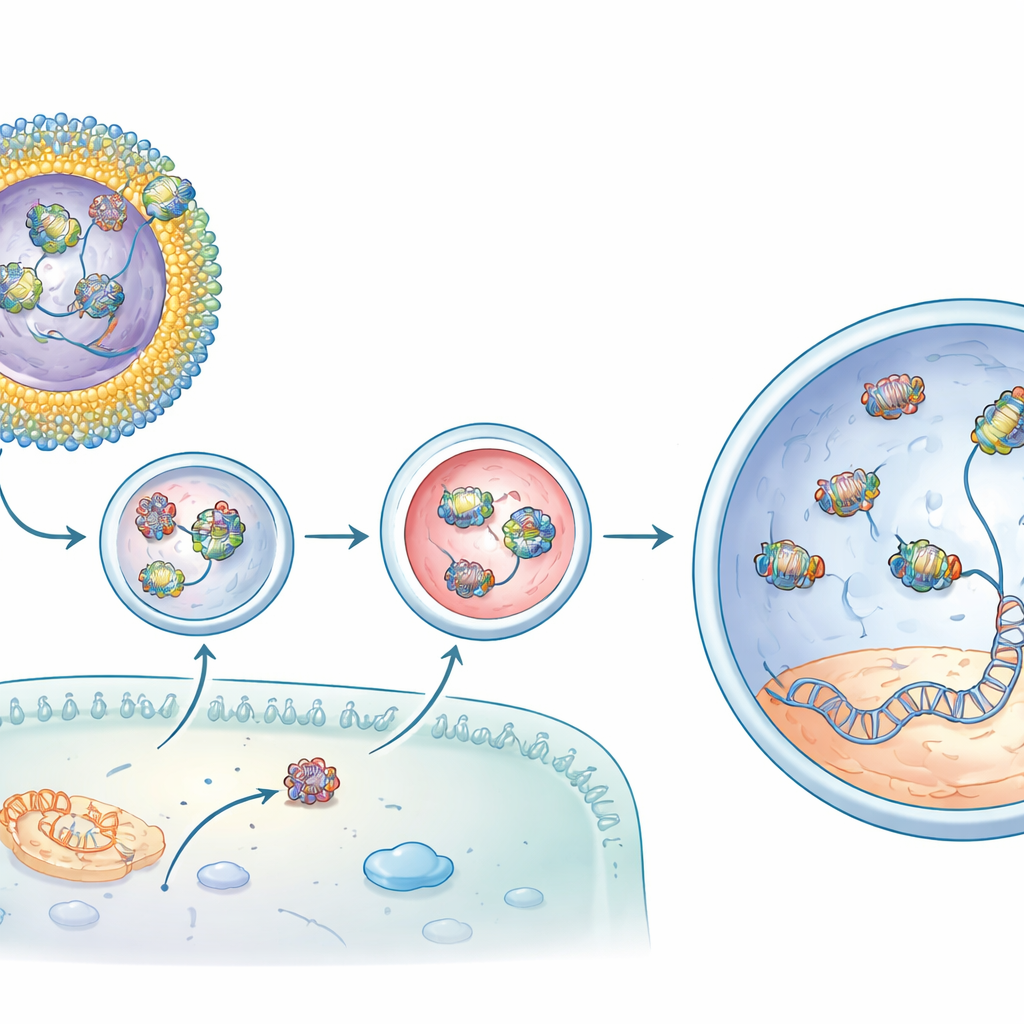
De la reparación molecular a respuestas a la luz restauradas
Cuando estos liposomas que contenían CBB11 y llevaban el editor de bases se inyectaron bajo la retina de ratones rd12, los resultados fueron contundentes. En comparación con el editor inyectado solo, la formulación optimizada aumentó la corrección de ADN deseada en el gen objetivo en más de un orden de magnitud y produjo niveles aún mayores de ARNm corregido. El análisis químico mostró la recuperación del pigmento retiniano sensible a la luz que falta en la enfermedad. Lo más convincente: las grabaciones eléctricas desde los ojos de los animales revelaron que sus células bastón recuperaron gran parte de su capacidad para responder a la luz tenue—hasta aproximadamente tres cuartas partes de la señal de un ratón normal en los mejores casos. Los cambios fuera del objetivo en otras partes del genoma se detectaron en niveles de fondo, lo que sugiere que la edición fue tanto potente como precisa.
Qué podría significar esto para futuras terapias oculares
Para un no especialista, el mensaje clave es que los autores han construido un “autobús lanzadera” reutilizable para proteínas de edición genética que funciona directamente en el ojo vivo. Al decorar partículas seguras, similares a las usadas en vacunas, con un tinte que agarra proteínas, crearon un sistema que puede capturar distintos editores en su superficie, entregarlos a células retinianas, corregir mutaciones causantes de enfermedades y restaurar de manera mensurable la visión en ratones tras un único tratamiento. Aunque es necesario más trabajo para evaluar completamente la seguridad, mejorar la orientación y adaptar el método para el uso humano, esta plataforma apunta hacia futuros medicamentos de precisión de una sola dosis para enfermedades retinianas hereditarias y, posiblemente, otras condiciones genéticas donde la reparación localizada y cuidadosa del ADN podría marcar la diferencia entre la ceguera y la vista.
Cita: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
Palabras clave: terapia génica retiniana, edición de bases CRISPR, liposomas, entrega de proteínas, ceguera hereditaria