Clear Sky Science · es
Perspectivas sobre la estructura y la modulación de TWIK-2 humano
Por qué importa esta diminuta puerta en nuestras células
En el interior de nuestras células, compuertas microscópicas formadas por proteínas controlan el flujo de átomos cargados, determinando cómo disparan los nervios, cómo se contraen los vasos sanguíneos y cómo responde nuestro sistema inmunitario. Una de esas compuertas, llamada TWIK-2, se ha vinculado con la hipertensión pulmonar y la inflamación dañina, pero hasta ahora los científicos sabían muy poco sobre su arquitectura o cómo modularla con fármacos. Este estudio revela la estructura detallada de TWIK-2 humano, muestra su comportamiento eléctrico y describe cómo podría dirigirse para desarrollar nuevos fármacos antiinflamatorios.
Un canal silencioso con grandes implicaciones para la salud
TWIK-2 pertenece a una amplia familia de canales de potasio de “fuga” que ayudan a establecer el voltaje de reposo celular permitiendo que iones de potasio atraviesen la membrana. Mientras que otros miembros de esta familia, como los canales TREK y TASK, han sido estudiados intensamente y se han vinculado al dolor y al estado de ánimo, TWIK-2 ha permanecido en gran medida oscuro porque es difícil de registrar y se expresa pobremente en sistemas de laboratorio estándar. No obstante, estudios en animales y en células han asociado TWIK-2 con hipertensión pulmonar, lesión pulmonar aguda, pérdida de audición y la activación de un complejo inmunitario llamado inflammasoma NLRP3, que promueve inflamación dañina en la sepsis y otras enfermedades. Comprender cómo funciona TWIK-2 es por tanto esencial tanto para la biología básica como para el diseño de terapias dirigidas.
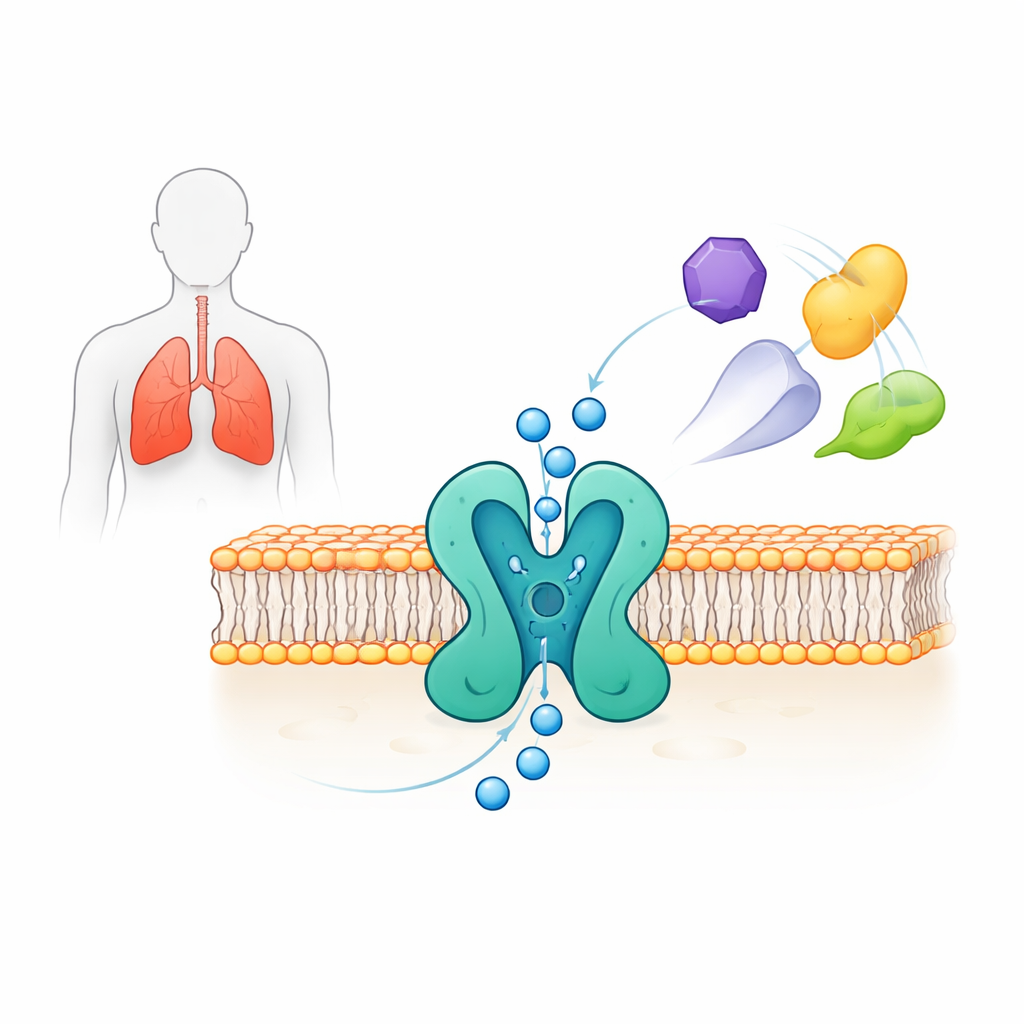
Ver la compuerta con detalle atómico
Los investigadores expresaron TWIK-2 humano de longitud completa en líneas celulares humanas y utilizaron crio‑microscopía electrónica de una sola partícula para determinar su estructura tridimensional a una resolución de aproximadamente 3,7 Å. El canal forma un ensamblaje de dos partes que en conjunto crean un poro central por el que pasan los iones de potasio. Cada mitad contiene cuatro segmentos transmembrana y dos “hélices de poro” que conforman una región estrecha llamada filtro de selectividad, donde se distingue el potasio de otros iones. Por encima del poro, dos estructuras arqueadas en forma de “caperuza” crean dos vías de entrada separadas para los iones desde el exterior celular. La estructura también revela pequeñas asimetrías entre los dos lados del poro que dan a TWIK-2 una disposición pseudo‑cuatripartita, un rasgo característico de esta familia de canales.
Lípidos ocultos y una vía iónica finamente ajustada
A lo largo de la vía de conducción iónica, el equipo trazó cómo los iones potasio se mueven desde el interior celular, a través de un “puño” hidrofóbico, por el filtro de selectividad y hacia afuera por debajo de la caperuza. El punto más estrecho sigue siendo lo bastante ancho para que el potasio viaje en fila india. Aunque la proteína se purificó sin añadir lípidos, los mapas de crio‑EM mostraron densidades tubulares alojadas cerca de la parte inferior del poro y en huecos laterales entre hélices. Estas densidades probablemente representan lípidos o colas de detergente que se adhirieron a TWIK-2 durante la purificación, lo que sugiere que los lípidos de la membrana natural pueden alojarse en estas cavidades y desplazar sutilmente la forma de hélices cercanas. Tales desplazamientos, especialmente en una hélice llamada M4 y en los bucles del filtro de selectividad, se piensa que ajustan si el canal está abierto, cerrado o en un estado intermedio.
Explorar la compuerta con mutaciones y bloqueadores
Para conectar la estructura con la función, los científicos usaron un sistema automatizado de patch‑clamp para medir corrientes de células que expresaban TWIK-2 normal o versiones con aminoácidos concretos alterados. Encontraron que TWIK-2 es fuertemente dependiente del voltaje pero, a diferencia de su pariente TWIK-1, en gran medida insensible a cambios en la acidez externa. Mutaciones en dos treoninas conservadas en la base del filtro de selectividad hicieron que el canal se abriera más rápido y condujera más corriente, lo que sugiere que estos sitios actúan como bisagras clave que estabilizan el estado cerrado. Cambios en la entrada y salida del poro modificaron la rapidez con que el canal se encendía y apagaba, revelando lo estrictamente controlada que está la vía iónica. El equipo probó después cuatro pequeñas moléculas conocidas por modular canales relacionados. Dos de ellas, ML365 y NPBA, bloquearon potentemente TWIK-2, mientras que las otras no tuvieron efecto. Al comparar cómo distintas mutaciones alteraban la sensibilidad a los fármacos, los autores infieren que estos compuestos probablemente se unen justo bajo el filtro de selectividad y en cavidades adyacentes, y que diferentes fármacos usan modos de unión solapados pero distintos.
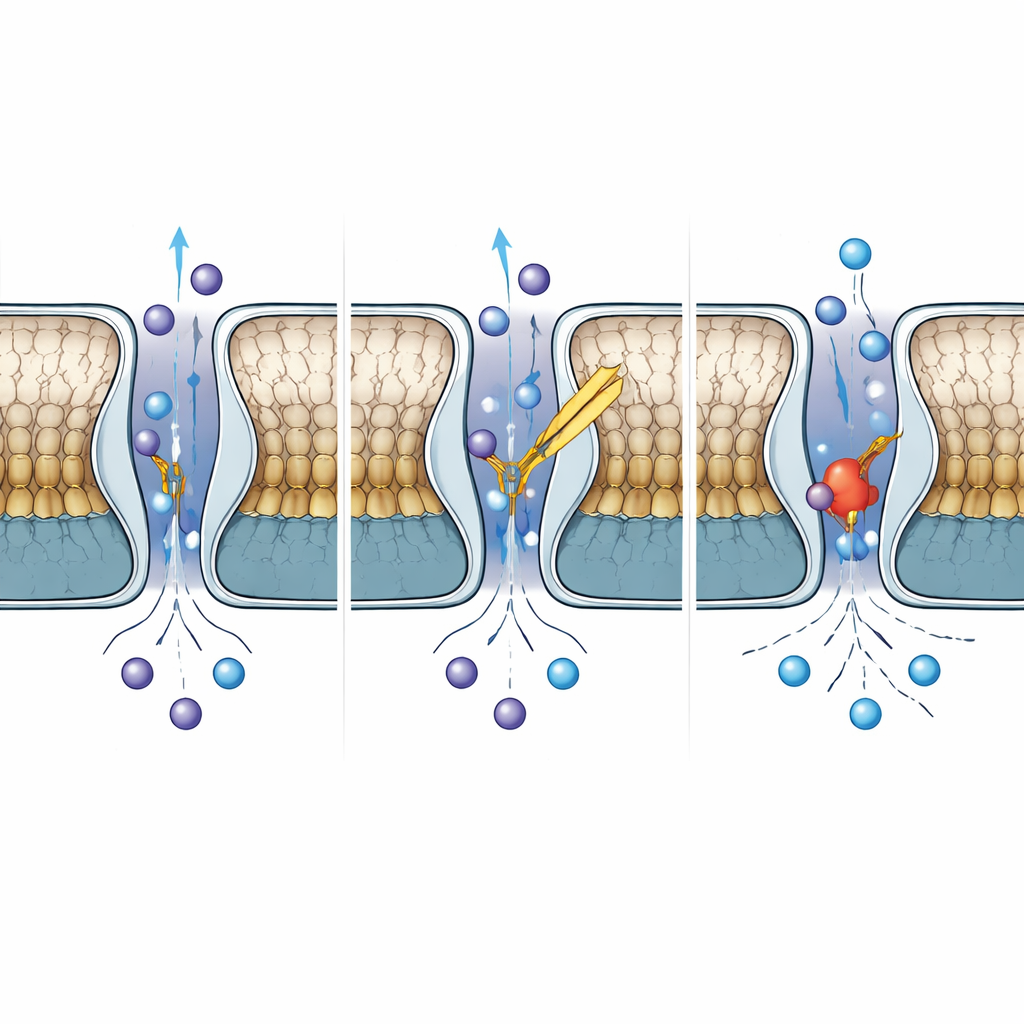
Cómo TWIK-2 difiere de sus parientes cercanos
Aunque TWIK-2 comparte más de la mitad de su secuencia con TWIK-1, su comportamiento diverge en aspectos importantes. Al comparar TWIK-2 con estructuras publicadas de TWIK-1 a pH neutro y ácido, los autores encontraron que la región de la caperuza de TWIK-2 se asemeja a la forma inhibida por ácido de TWIK-1, sin embargo su filtro de selectividad permanece dispuesto como en la forma conductora y abierta. Una histidina única en TWIK-1, conocida por detectar protones e introducirse en el poro para bloquear el flujo iónico a pH bajo, está reemplazada por una tirosina en TWIK-2. Incluso cuando el equipo reintrodujo una histidina en esa posición en TWIK-2, el canal no se volvió sensible al pH, demostrando que el control por pH en estos canales depende de una red más amplia de residuos y movimientos, no solo de un aminoácido “interruptor”.
De la estructura a futuras terapias
En conjunto, este trabajo ofrece la primera imagen de alta resolución de TWIK-2 humano y cartografía cómo características estructurales específicas modelan su flujo iónico, su respuesta al voltaje y su susceptibilidad a bloqueadores de pequeñas moléculas. El hallazgo de que compuestos existentes pueden inhibir selectivamente TWIK-2, junto con una plataforma robusta de cribado automatizado, abre la puerta a búsquedas a gran escala de fármacos más seguros y potentes. Dado que la actividad de TWIK-2 en células inmunitarias se ha vinculado a la inflamación descontrolada, especialmente en los pulmones, tales fármacos podrían sentar las bases de nuevos tratamientos antiinflamatorios que actúen atenuando con delicadeza esta diminuta pero poderosa compuerta de la membrana celular.
Cita: Ma, Q., Hernandez, C.C., Navratna, V. et al. Insights into the structure and modulation of human TWIK-2. Nat Commun 17, 2201 (2026). https://doi.org/10.1038/s41467-026-69072-1
Palabras clave: canal de potasio TWIK-2, canales K2P de dos poros, estructura de canal iónico por crio‑EM, moduladores de canales de potasio, inflamación pulmonar