Clear Sky Science · es
Proteómica espacial unicelular del colon y modelos murinos vinculan la disfunción mitocondrial con la deficiencia de células plasmáticas secretoras de IgA dimérica en la enfermedad de Crohn
Por qué importan los anticuerpos intestinales en la enfermedad de Crohn
La enfermedad de Crohn es más conocida por los dolorosos brotes de inflamación intestinal, pero mucho antes de que los síntomas se disparen pueden producirse cambios sutiles en la forma en que el sistema inmunitario protege el intestino. Este estudio plantea una pregunta simple pero importante: ¿las personas con enfermedad de Crohn en remisión siguen fabricando el tipo correcto de anticuerpos para mantener a raya a los microbios intestinales? Combinando muestras de pacientes, perfilado tisular de alta resolución, análisis metabólicos y modelos animales, los autores descubren una debilidad oculta en el escudo de anticuerpos del intestino que está vinculada a la producción de energía celular.
Un recubrimiento protector que se queda corto
Nuestros intestinos dependen de un anticuerpo especial llamado IgA secretora que se libera en el moco que recubre el intestino. La IgA, especialmente en su forma “doble” denominada IgA dimérica, recubre bacterias y otros microbios, ayudando a mantenerlos en la superficie en lugar de penetrar en el tejido. En este trabajo, los investigadores examinaron biopsias de colon, sangre y heces de personas con enfermedad de Crohn en remisión y de controles no inflamados. Dentro del tejido colónico, los pacientes con Crohn presentaban en realidad más células B y células productoras de anticuerpos y niveles más altos de genes y proteínas relacionados con la IgA. Sin embargo, cuando el equipo midió la IgA en las heces, hallaron lo contrario de lo que cabría esperar: la IgA secretora en la luz intestinal estaba significativamente reducida. 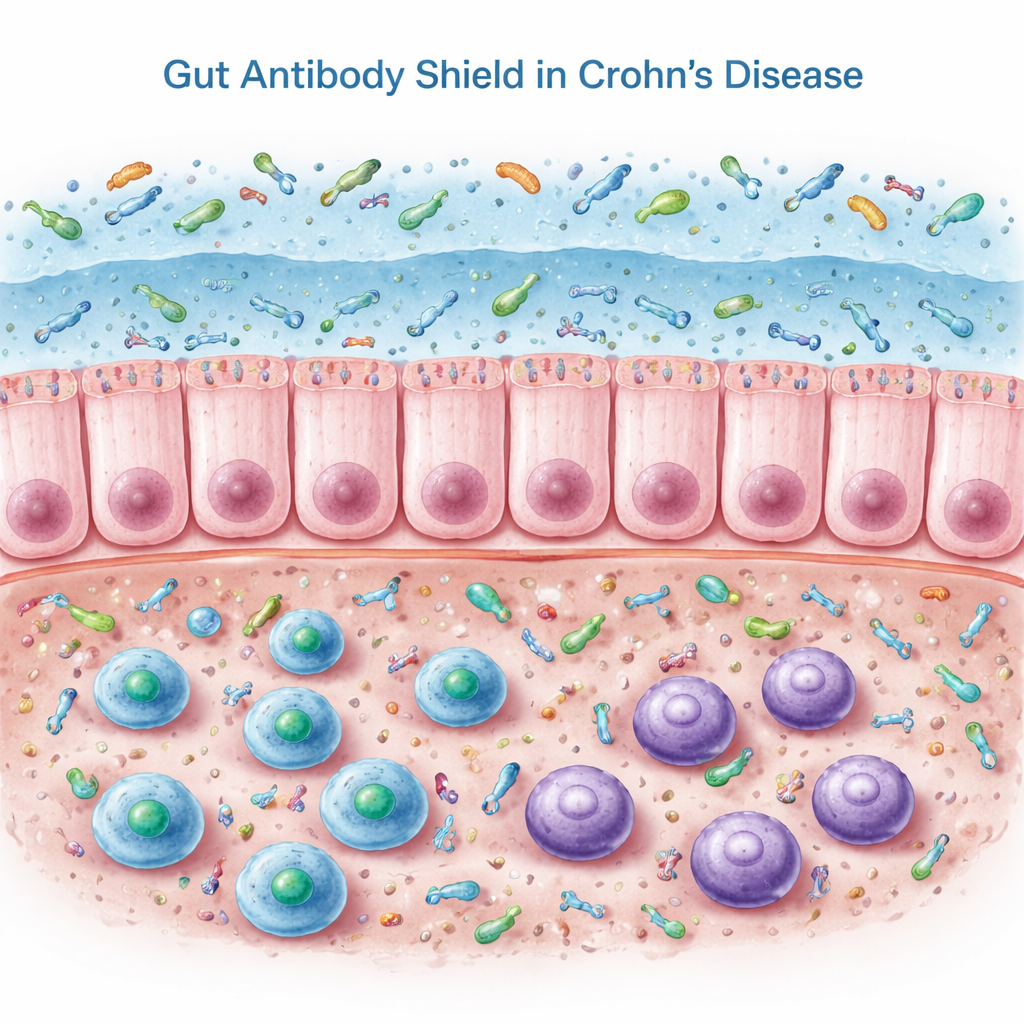
Atascadas a mitad de camino: células productoras de anticuerpos que no maduran por completo
Las células que secretan IgA —las células plasmáticas— normalmente maduran a través de etapas definidas, desde precursores activas y de corta vida hasta especialistas de larga vida que expulsan grandes cantidades de IgA dimérica. Utilizando proteómica espacial unicelular, que mapea muchas proteínas en células individuales dentro del tejido intacto, los autores pudieron distinguir subgrupos de células plasmáticas inmaduras y totalmente maduras en el colon. En pacientes con Crohn, los plasmablastos tempranos y las células plasmáticas inmaduras estaban ampliados, mientras que las células plasmáticas más maduras se reducían. Análisis bioquímicos confirmaron que la proporción de IgA dimérica frente a monomérica era menor en los colones de Crohn, y cada célula productora de anticuerpos secretaba menos IgA dimérica de media. Cuando el equipo aisló células B de memoria con clase cambiada del colon y las indujo a convertirse en células plasmáticas en cultivo, las células procedentes de pacientes con Crohn no lograron aumentar marcadores clave de maduración y produjeron menos IgA total y dimérica, aunque la producción de IgG permaneció en gran medida normal. Esto sugiere un bloqueo intrínseco en el programa de maduración específico de las células plasmáticas secretoras de IgA.
Fábricas de energía bajo tensión
Para entender qué impulsa este bloqueo, los investigadores recurrieron al metabolismo celular. Encontraron que las células plasmáticas en el tejido de Crohn expresaban niveles más altos de CD38, una enzima en la superficie celular que consume NAD+, un combustible central para la producción de energía mitocondrial. Los genes implicados en la fosforilación oxidativa mitocondrial —la vía principal por la que las células generan ATP a partir de nutrientes— estaban ampliamente regulados a la baja en el tejido colónico de pacientes con Crohn, y los patrones de metabolitos plasmáticos eran consistentes con un desplazamiento lejos de la respiración mitocondrial eficiente. En experimentos ex vivo, las células plasmáticas derivadas de Crohn consumieron poca glucosa, liberaron menos lactato y mostraron expresión reducida de genes de energía mitocondrial, indicando un estado metabólicamente «quiescente» o debilitado. 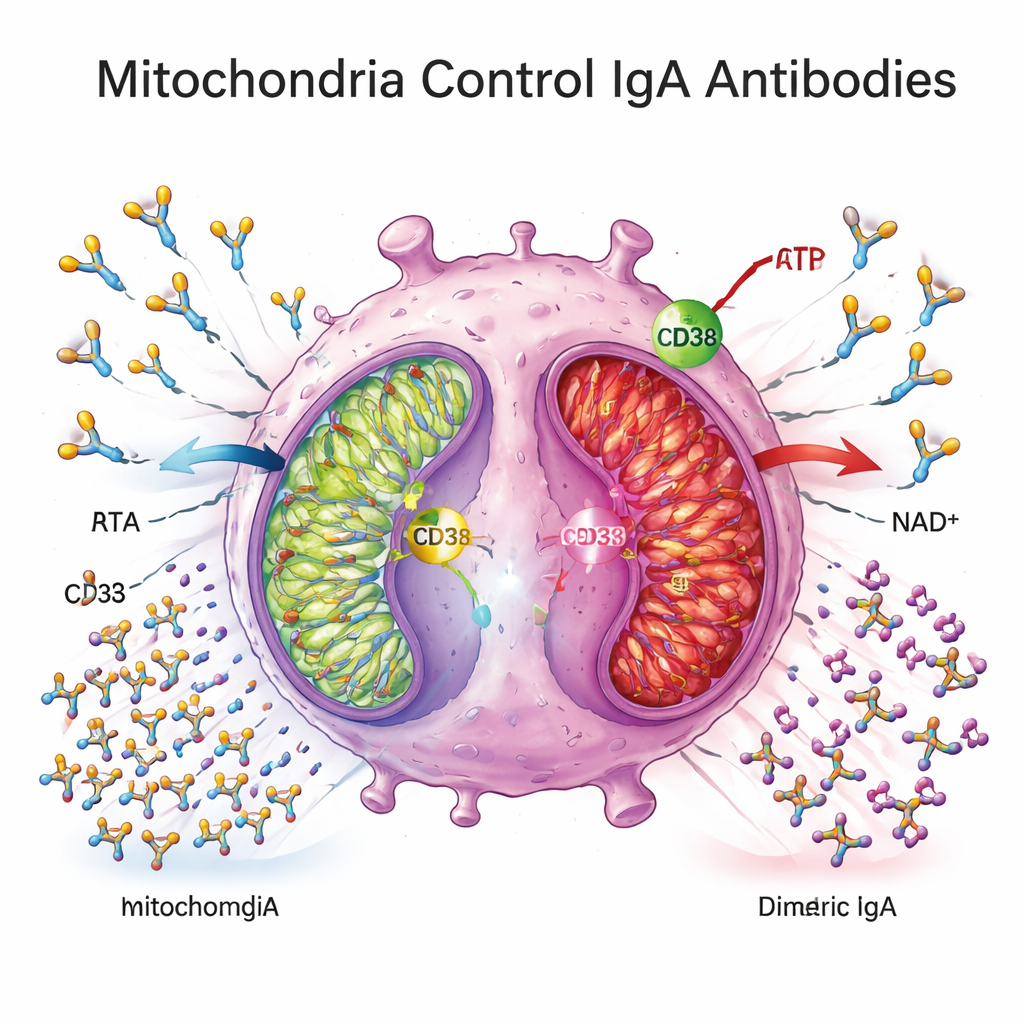
Pistas de modelos murinos y la dieta
Los modelos murinos aportaron apoyo adicional. Ratones portadores de una mutación mitocondrial definida que perjudica el complejo V productor de ATP presentaron menos células plasmáticas maduras en los tejidos linfoides asociados al intestino, menor expresión de marcadores de células plasmáticas en el colon y niveles más bajos tanto de IgA monomérica como dimérica en el tejido colónico. Por el contrario, ratones sanos alimentados con una dieta sin glucosa y alta en proteínas, que potencia la actividad mitocondrial en el colon, desarrollaron más células productoras de IgA y mayor IgA fecal. Estos experimentos complementarios vinculan directamente el rendimiento mitocondrial con la capacidad de las células plasmáticas para madurar y mantener una barrera robusta de IgA en el intestino.
Qué significa esto para las personas con enfermedad de Crohn
En conjunto, el estudio dibuja un panorama en el que la enfermedad de Crohn, incluso durante la remisión clínica, se asocia con una sobreabundancia de células de linaje B inmaduras en el colon y una escasez de células plasmáticas totalmente maduras y de alta demanda energética que secretan IgA dimérica en el moco. El intestino puede parecer tranquilo, pero su escudo de anticuerpos es más fino y menos eficaz. Al vincular este defecto con la disfunción mitocondrial —posiblemente impulsada en parte por una mayor actividad de CD38—, el trabajo sugiere que terapias dirigidas a restaurar el metabolismo energético celular o a afinar la señalización de CD38 podrían ayudar a reconstruir la barrera mucosal de IgA. Para los pacientes, esto plantea la posibilidad de que futuros tratamientos no solo supriman la inflamación cuando aparezca, sino que también fortalezcan las defensas de primera línea del intestino para prevenir la aparición de brotes.
Cita: Raschdorf, A., de Almeida, L.N., Solbach, P. et al. Colonic spatial single-cell proteomics and murine models link mitochondrial dysfunction to dimeric IgA-secreting plasma cell deficiency in Crohn’s disease. Nat Commun 17, 1590 (2026). https://doi.org/10.1038/s41467-026-69069-w
Palabras clave: Enfermedad de Crohn, anticuerpos intestinales, IgA, mitocondrias, inmunidad intestinal