Clear Sky Science · es
FidlTrack: seguimiento de partículas individuales con alta fidelidad y consciente de la estructura resuelve el movimiento molecular intracelular en orgánulos que detectan el procesamiento de APP
Observando moléculas individuales dentro de células vivas
Dentro de cada célula, innumerables moléculas están en continuo movimiento: colisionan, se unen y se disocian. Los microscopios modernos pueden seguir moléculas individuales una por una, prometiendo una vista detallada de cómo funciona la vida a las escalas más pequeñas. Pero cuando muchas moléculas se desplazan rápidamente en espacios estrechos y enredados, como el retículo endoplásmico o las mitocondrias, sus trayectorias se entrelazan y resultan fáciles de interpretar mal. Este trabajo presenta FidlTrack, una nueva forma de desenmarañar esa confusión para que los investigadores puedan confiar en lo que ven al rastrear moléculas individuales en tiempo real.
Por qué es tan difícil rastrear movimientos minúsculos
El seguimiento de partículas individuales funciona siguiendo el mismo punto brillante a través de muchos fotogramas de una película. En una superficie celular relativamente plana, donde las moléculas se mueven despacio y están separadas, esto es manejable. Sin embargo, en el interior de la célula las moléculas difunden mucho más rápido y se agolpan en tubos y láminas estrechos y curvos. Entre fotogramas, el mismo punto puede haberse desplazado una gran distancia, y varios puntos idénticos pueden quedar a su alcance. El software tradicional debe “adivinar” qué punto en el fotograma siguiente corresponde a la misma molécula, y esas conjeturas pueden fallar con facilidad. Aún peor, trayectorias correctas e incorrectas pueden parecer muy similares, por lo que es difícil saber qué partes de los datos son fiables.
Diseñar experimentos para obtener datos honestos
Los investigadores primero construyeron un simulador realista que genera películas de “verdad de referencia” de moléculas en difusión, donde las trayectorias reales son conocidas. Usaron estos conjuntos de datos sintéticos para probar sistemáticamente cómo factores clave afectan la fiabilidad del seguimiento: la velocidad de movimiento de las moléculas, cuántas aparecen en cada imagen, con qué frecuencia se adquieren las imágenes y cuánto puede saltar una molécula entre fotogramas. A partir de esto, crearon mapas que muestran, para cada situación dada, qué ajustes maximizan la fracción de movimientos correctamente reconstruidos. Estos mapas revelan que para moléculas lentas a densidades moderadas el seguimiento puede ser muy fiable, pero para moléculas rápidas a altas densidades los errores crecen con rapidez y añadir más moléculas deja de aportar información útil.
Detectar y recortar pasos dudosos
Después, el equipo abordó una idea sutil pero poderosa: la ambigüedad. Un movimiento se llama ambiguo cuando más de un posible punto siguiente está al alcance, obligando al algoritmo a elegir entre varios enlaces plausibles. Usando sus simulaciones, los autores mostraron que una gran parte de los errores de seguimiento proviene de estos pasos ambiguos. Definieron una Puntuación de Ambigüedad que contabiliza con qué frecuencia ocurren tales situaciones y, a continuación, exploraron qué sucede si se eliminan todos los pasos ambiguos tras el seguimiento. Esta poda sacrifica algunos datos y acorta trayectorias, pero aumenta bruscamente la fiabilidad global de lo que queda y mejora las estimaciones de la velocidad de movimiento de las moléculas. Aplicado a películas reales de un marcador en el retículo endoplásmico, la ambigüedad era mayor en regiones densas cercanas al núcleo celular, y eliminar los enlaces ambiguos limpió esas zonas sin perjudicar regiones más simples.
Dejar que la arquitectura celular guíe el seguimiento
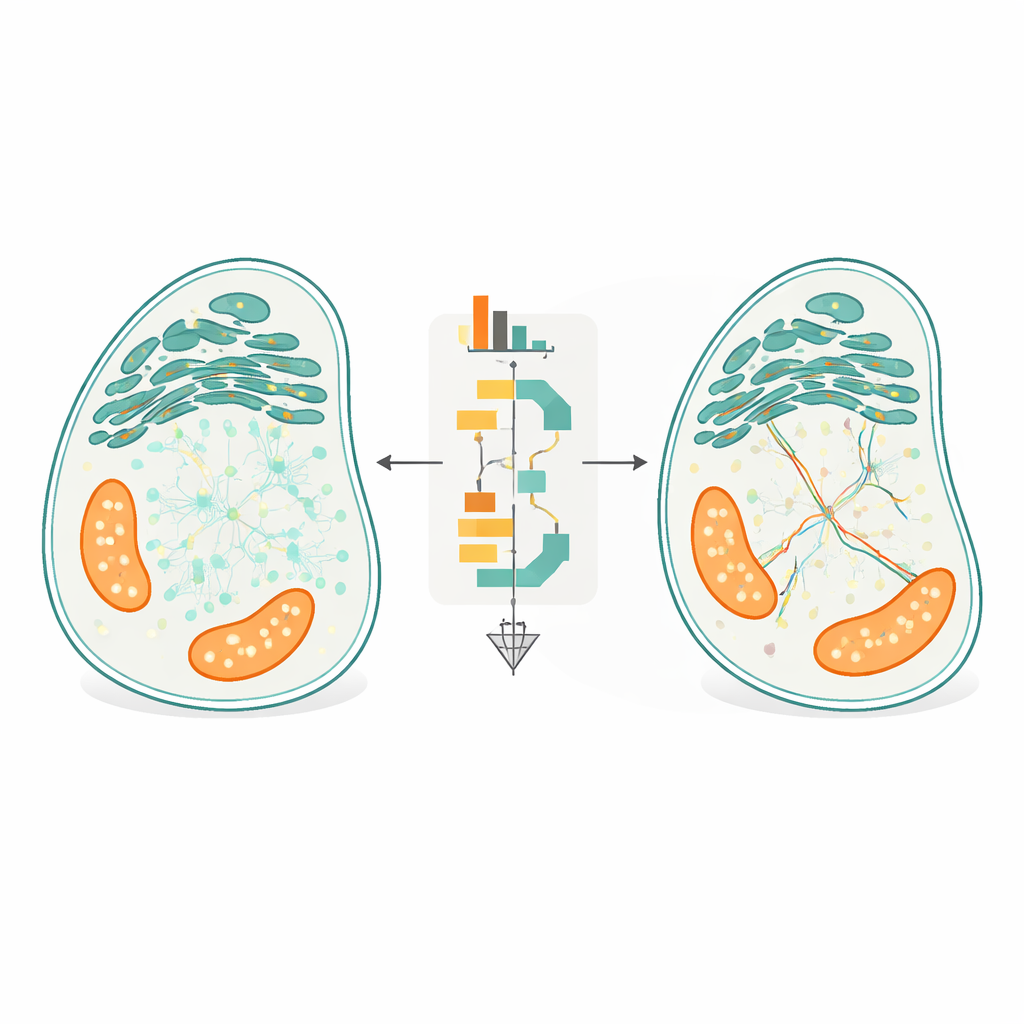
La innovación central de FidlTrack es el seguimiento “consciente de la estructura”. En lugar de tratar cada punto como si se moviera en un espacio vacío, el método utiliza imágenes de la arquitectura interna de la célula—como los contornos del retículo endoplásmico, las mitocondrias o las delgadas proyecciones neuronales—para restringir dónde las moléculas pueden desplazarse de forma realista. La imagen del orgánulo se convierte en un grafo de píxeles conectados, y las distancias se miden a lo largo de ese grafo en lugar de líneas rectas a través del espacio. Enlaces que requerirían que una molécula saltara a través de un hueco entre dos túbulos separados pueden así marcarse como imposibles y rechazarse. En simulaciones de tubos muy apiñados y en películas reales de procesos neuronales y orgánulos, esta conciencia estructural redujo las conexiones ambiguas hasta a la mitad e incrementó varias veces la cantidad de datos de movimiento no ambiguos y fiables.
Revelando comportamientos celulares ocultos y eventos relevantes para la enfermedad
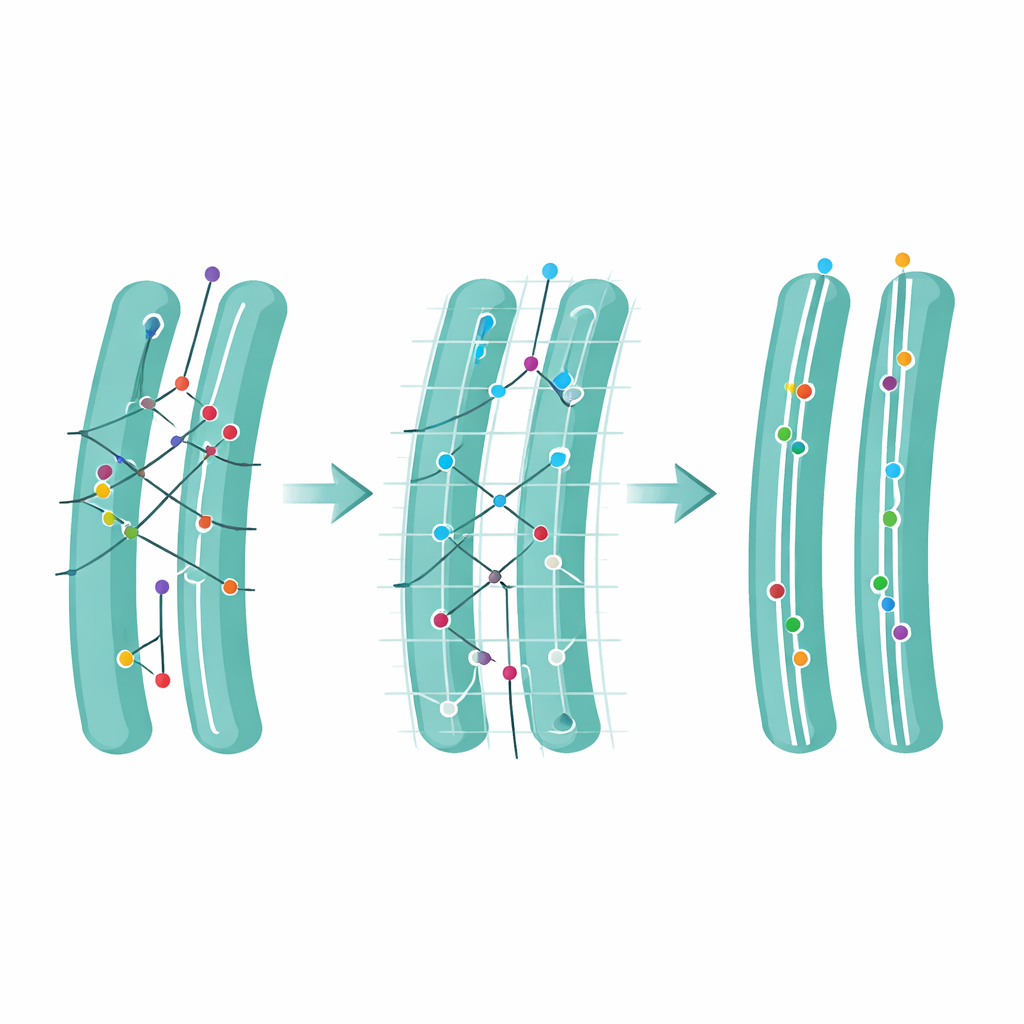
Armados con estas herramientas—ajustes optimizados, filtrado de ambigüedad y conciencia estructural—los autores revisitaron varias preguntas biológicas que antes estaban fuera de alcance. En el retículo endoplásmico, pudieron seguir con claridad cómo se mueven las proteínas al interactuar con sitios de salida que canalizan carga hacia el aparato de Golgi, distinguiendo los «paseos rápidos» de estancias más largas. Captaron momentos raros en los que la proteína relacionada con el Alzheimer, APP, es cortada por la enzima BACE1, visible como un cambio brusco de un movimiento lento ligado a la membrana a una difusión libre más rápida. También siguieron moléculas diseñadas semejantes a anticuerpos en el RE y, a partir de cambios en su movimiento, inferieron cuándo estaban unidas a su diana frente a cuando derivaban libremente. En estos casos diversos, FidlTrack recuperó trayectorias más fiables y agudizó diferencias que el seguimiento estándar difuminaba o subestimaba.
Qué significa esto para la biología celular futura
Para los no especialistas, el mensaje clave es que no todas las trayectorias de moléculas singulares son iguales: algunas son fiables, otras engañosas, y hasta ahora ha sido difícil diferenciarlas. FidlTrack ofrece una forma práctica y de código abierto tanto de medir cuán fiable es un conjunto de datos dado como de mejorar esa fiabilidad ajustando las condiciones experimentales, eliminando pasos ambiguos y usando la propia geometría celular como guía. Esto hace posible observar con mayor confianza cómo las moléculas navegan por el intrincado interior celular y detectar eventos raros o sutiles, desde el enrutamiento de proteínas hasta procesos relevantes para enfermedades, que antes quedaban enterrados en el ruido.
Cita: Parutto, P., Yuan, Y., Davì, V. et al. FidlTrack: high-fidelity structure-aware single particle tracking resolves intracellular molecular motion in organelles sensing APP processing. Nat Commun 17, 2639 (2026). https://doi.org/10.1038/s41467-026-69067-y
Palabras clave: seguimiento de partículas individuales, dinámica intracelular, estructura de orgánulos, movimiento de proteínas, enfermedad de Alzheimer