Clear Sky Science · es
FLASH-MM: análisis diferencial de expresión unicelular rápido y escalable usando modelos lineales de efectos mixtos
Por qué las células diminutas necesitan gran potencia informática
La biología moderna puede ahora leer la actividad de miles de genes en cientos de miles de células individuales a la vez. Esta visión unicelular promete una comprensión más precisa de cómo nuestros cuerpos combaten infecciones, difieren entre hombres y mujeres o desarrollan enfermedades. Pero convertir estos enormes y ruidosos conjuntos de datos en descubrimientos fiables es dolorosamente lento y, si se hace de forma ingenua, puede llevar a conclusiones erróneas. Este artículo presenta FLASH-MM, una nueva manera de procesar datos unicelulares que mantiene la integridad estadística mientras hace que el cómputo sea lo suficientemente rápido para los estudios más grandes de hoy.
El reto de datos celulares ruidosos y multitudinarios
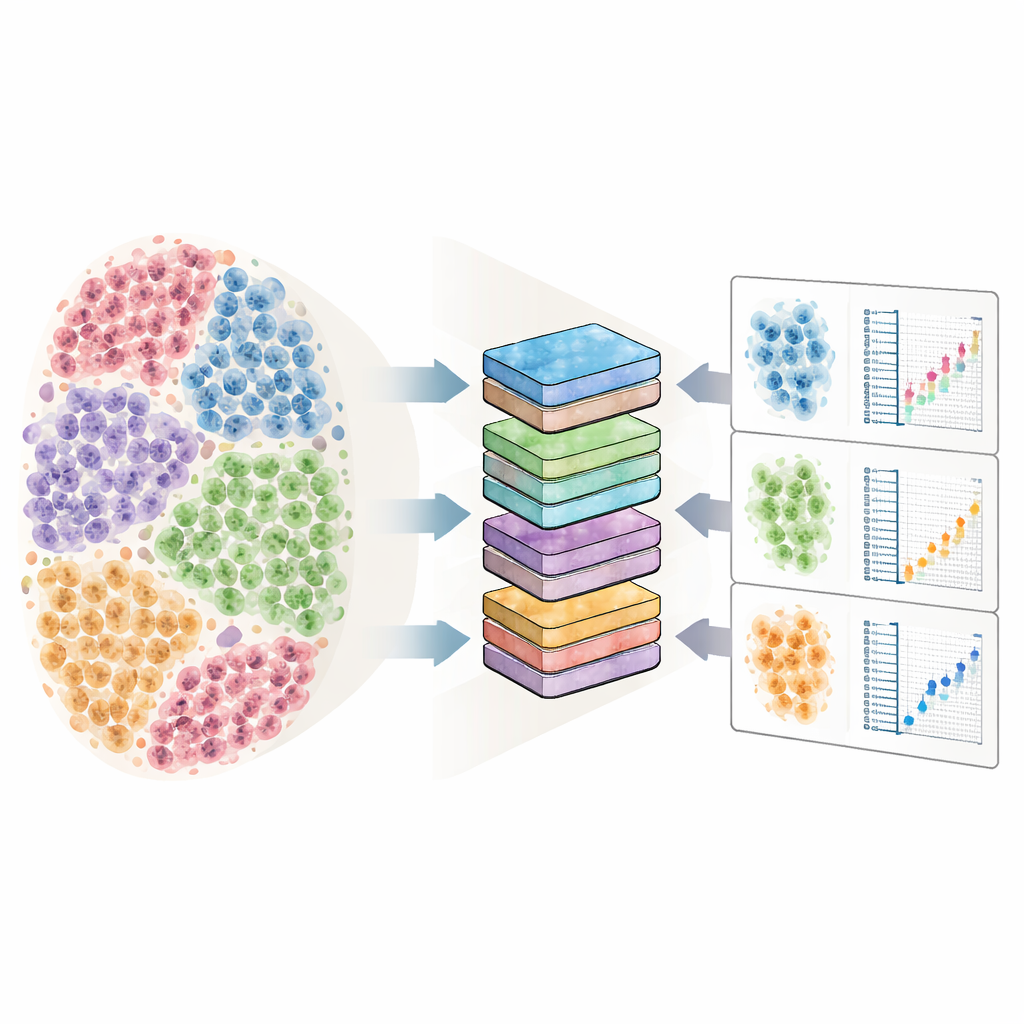
La secuenciación de ARN unicelular mide qué genes están “encendidos” o “apagados” en cada célula, a lo largo de muchas personas y condiciones. Las células del mismo individuo tienden a parecerse porque comparten genética e historia de vida, mientras que los individuos difieren mucho entre sí. Esto crea una estructura en capas en los datos: muchas células dentro de cada persona y muchas personas dentro de cada condición, como enfermo frente a sano. Si se ignoran estas relaciones, los métodos estándar pueden etiquetar erróneamente miles de genes como cambiados cuando no lo están, simplemente por tratar cada célula como un punto de datos independiente. Al mismo tiempo, los conjuntos de datos unicelulares han estallado en tamaño, incluyendo ahora cientos de sujetos y hasta millones de células, lo que estira las herramientas estadísticas convencionales más allá de sus límites tanto en tiempo como en memoria.
Una forma más inteligente de modelar personas y células
Para abordar estas complejidades, los estadísticos suelen recurrir a modelos lineales de efectos mixtos, que separan explícitamente las diferencias consistentes entre condiciones (por ejemplo, estado frente a tuberculosis o sexo) de las diferencias aleatorias entre individuos. En principio, estos modelos son ideales para estudios unicelulares porque pueden tener en cuenta tanto las similitudes entre células del mismo individuo como la variación entre personas. En la práctica, sin embargo, el software de uso general para estos modelos se vuelve muy lento o agota la memoria en experimentos unicelulares grandes. Por ello, los investigadores a menudo recurren a atajos, como promediar los recuentos de todas las células del mismo tipo dentro de cada persona, lo que descarta gran parte de la información celular fina que hace tan valiosos a los datos unicelulares.
Cómo FLASH-MM acelera el trabajo pesado
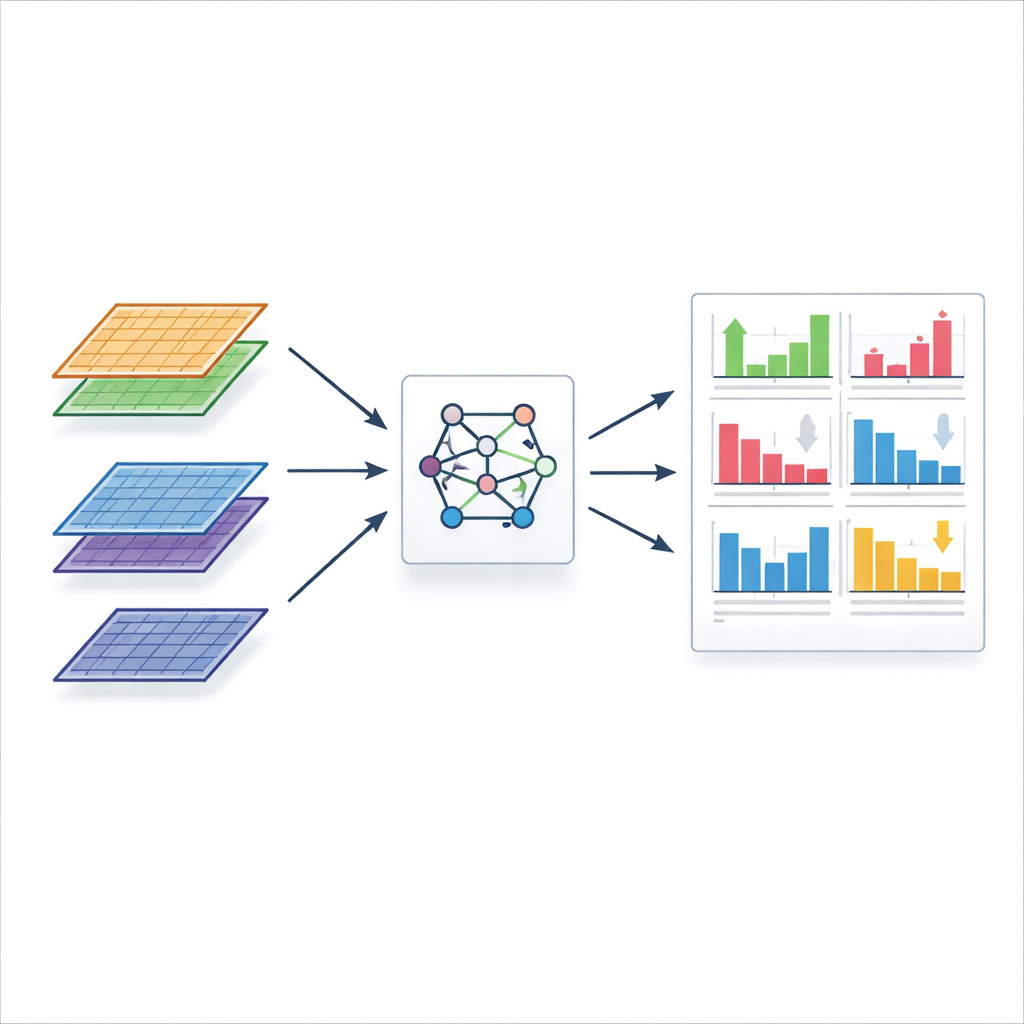
FLASH-MM conserva las ventajas de los modelos de efectos mixtos mientras reingeniería cómo se realizan los cálculos. En vez de recorrer repetidamente enormes tablas de medidas célula-por-gen, FLASH-MM primero destila cada conjunto de datos en un conjunto compacto de números resumen que capturan cómo las células se relacionan con características conocidas como el tamaño de biblioteca, tipo celular, tratamiento o donante. El algoritmo central trabaja luego solo con estas matrices más pequeñas, reduciendo la carga computacional de escalar con cada célula a escalar con el mucho menor número de ingredientes del modelo. Los autores también ajustan la forma en que se representa la variabilidad del modelo para que las pruebas estadísticas estándar sigan siendo válidas, permitiendo que estadísticas sencillas t y z evalúen tanto los efectos principales de interés como el valor añadido de incluir la variación entre personas. Estudios de simulación con datos artificiales realistas muestran que las respuestas de FLASH-MM coinciden con las del software de referencia hasta varios decimales, mientras que se ejecuta entre aproximadamente 50 y 140 veces más rápido y emplea mucha menos memoria.
Poner el método a prueba en tejidos reales
Para demostrar su impacto en el mundo real, el equipo aplicó FLASH-MM a dos conjuntos de datos unicelulares exigentes. En un mapa de más de 27.000 células renales humanas sanas de 19 donantes, FLASH-MM buscó diferencias en la actividad génica entre donantes masculinos y femeninos dentro de cada tipo celular, tratando a cada persona como un factor aleatorio para evitar conclusiones demasiado confiadas. Encontró los patrones ligados al sexo más fuertes en un tipo específico de célula del túbulo renal, donde las células masculinas favorecían vías relacionadas con el manejo del ácido y la presión arterial, y las femeninas mostraban enriquecimiento en procesos de señalización y reciclaje de receptores. FLASH-MM completó este análisis en aproximadamente un minuto, comparado con casi dos horas para una herramienta estándar. El método también analizó alrededor de medio millón de células T de memoria de 259 personas en una cohorte de tuberculosis, identificando conjuntos de genes y vías vinculadas al estado de la enfermedad en diferentes estados activados de células T. Aquí, FLASH-MM terminó en menos de una hora y media, frente a más de dos días con el enfoque convencional.
Qué significa esto para futuros estudios célula a célula
Desde un punto de vista divulgativo, el mensaje es que ahora podemos aprovechar mejor el alud de datos unicelulares sin recortar pasos críticos. FLASH-MM hace un seguimiento de qué células proceden de qué persona y condición, de modo que los cambios génicos detectados tienen más probabilidades de reflejar biología genuina en lugar de peculiaridades del muestreo o efectos de lote. Al mismo tiempo, sus cálculos eficientes hacen factible analizar cientos de miles de células en ordenadores estándar, abriendo la puerta a estudios más ambiciosos sobre señales sutiles de enfermedad, diferencias sexuales y estados celulares raros. Dado que el enfoque es general y está disponible tanto en R como en Python, puede extenderse a tecnologías más nuevas como el mapeo génico espacial y mediciones moleculares en múltiples capas, ayudando a los investigadores a convertir vastos conjuntos de datos a nivel celular en conclusiones robustas y clínicamente relevantes.
Cita: Xu, C., Pouyabahar, D., Voisin, V. et al. FLASH-MM: fast and scalable single-cell differential expression analysis using linear mixed-effects models. Nat Commun 17, 2384 (2026). https://doi.org/10.1038/s41467-026-69063-2
Palabras clave: secuenciación de ARN unicelular, expresión diferencial, modelos lineales de efectos mixtos, genómica estadística, biología computacional