Clear Sky Science · es
Los miofibroblastos positivos para tenascina C agravan la hiperplasia neointimal vascular al propagar las interacciones nervio-macrófago en ratones
Cuando los vasos sanguíneos se curan de forma equivocada
Los procedimientos que reabren arterias obstruidas, como la angioplastia y la cirugía de derivación, salvan innumerables vidas. Sin embargo, con frecuencia dejan un problema oculto: con el tiempo, el vaso tratado puede cicatrizar hacia dentro, volviéndose a estrechar y devolviendo a los pacientes al riesgo. Este estudio en ratones descubre una conversación inesperada a tres bandas entre células de sostén, nervios y células inmunitarias en la pared vascular que impulsa este sobrecurado dañino, y señala a una molécula llamada tenascina C como un objetivo prometedor para romper el ciclo.
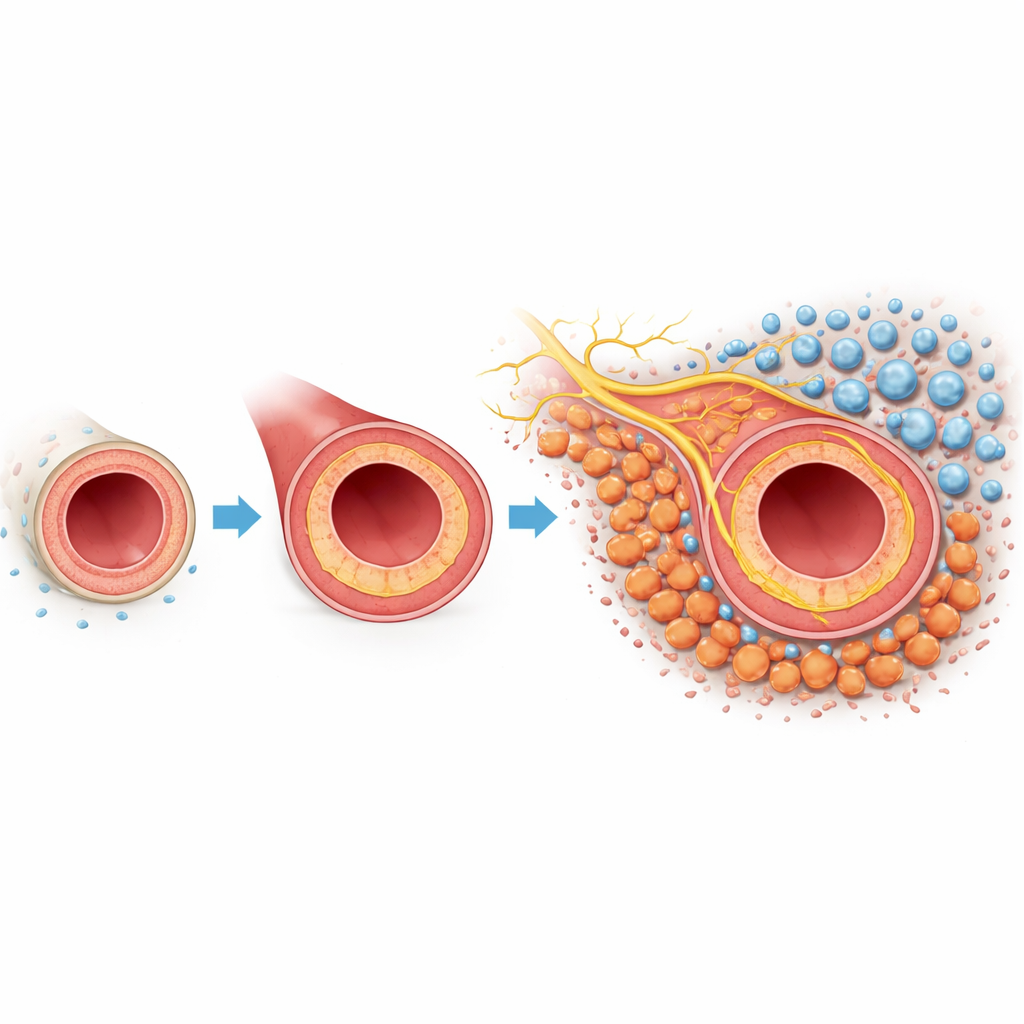
Una mirada más de cerca a la cicatrización problemática en las arterias
Cuando una arteria resulta lesionada o se manipula durante una cirugía, el revestimiento interno puede regenerarse de forma excesiva. Este crecimiento hacia dentro, denominado hiperplasia neointimal, engrosa la pared vascular y reduce el conducto por el que fluye la sangre. La capa más externa del vaso, la adventicia, contiene fibroblastos: células de sostén que normalmente mantienen la estructura vascular. En este modelo murino, donde la arteria carótida se ligó parcialmente para imitar la lesión, los investigadores emplearon perfilado genético unicelular y mapeo espacial para catalogar cada tipo celular principal implicado. Encontraron que los fibroblastos eran especialmente abundantes y cambiaron su comportamiento de forma drástica tras la lesión, lo que sugiere que estas células podrían ser actores centrales en la respuesta de cicatrización.
El surgimiento de células formadoras de cicatriz con tenascina C
Al profundizar en la población de fibroblastos, el equipo descubrió un subconjunto distintivo que apareció solo después de la lesión. Estas células mostraban rasgos de miofibroblastos: altos niveles de la proteína contráctil actina de músculo liso α y otro marcador denominado periostina, lo que indica que habían cambiado a un modo productor de cicatriz. De manera crucial, este subconjunto también producía grandes cantidades de tenascina C, una proteína de la matriz habitualmente escasa en tejidos adultos sanos pero abundante en enfermedad y reparación tisular. Experimentos de laboratorio mostraron que exponer fibroblastos adventiciales normales al factor de crecimiento transformante beta o a tenascina C adicional los empujaba a convertirse en estos miofibroblastos positivos para tenascina C. Las células secretaban entonces aún más tenascina C, creando un bucle auto-reforzador a través de un par específico de receptores de superficie, la integrina αvβ1, que fue ampliando de forma sostenida la población formadora de cicatriz.
Los nervios y las células inmunitarias se mudan al vecindario
La historia no terminó con la formación de la cicatriz. Utilizando imágenes 3D de montaje completo y transcriptómica espacial, los investigadores observaron que los miofibroblastos ricos en tenascina C se agrupaban cerca de fibras nerviosas en crecimiento y de células inmunitarias llamadas macrófagos en la capa externa del vaso. Las arterias lesionadas mostraron nervios sensoriales densos y enmarañados y más estructuras de tipo sináptico que las normales, tanto en ratones como en muestras humanas de arterias con hiperplasia neointimal. Los macrófagos en estas regiones exhibían un sello inflamatorio, produciendo moléculas como IL-1β y TGF-β1 que pueden alimentar aún más la cicatrización. En conjunto, los datos dibujaron el panorama de un microambiente reorganizado en el que las células formadoras de cicatriz, los nervios y los macrófagos se entrelazan físicamente e influyen entre sí.
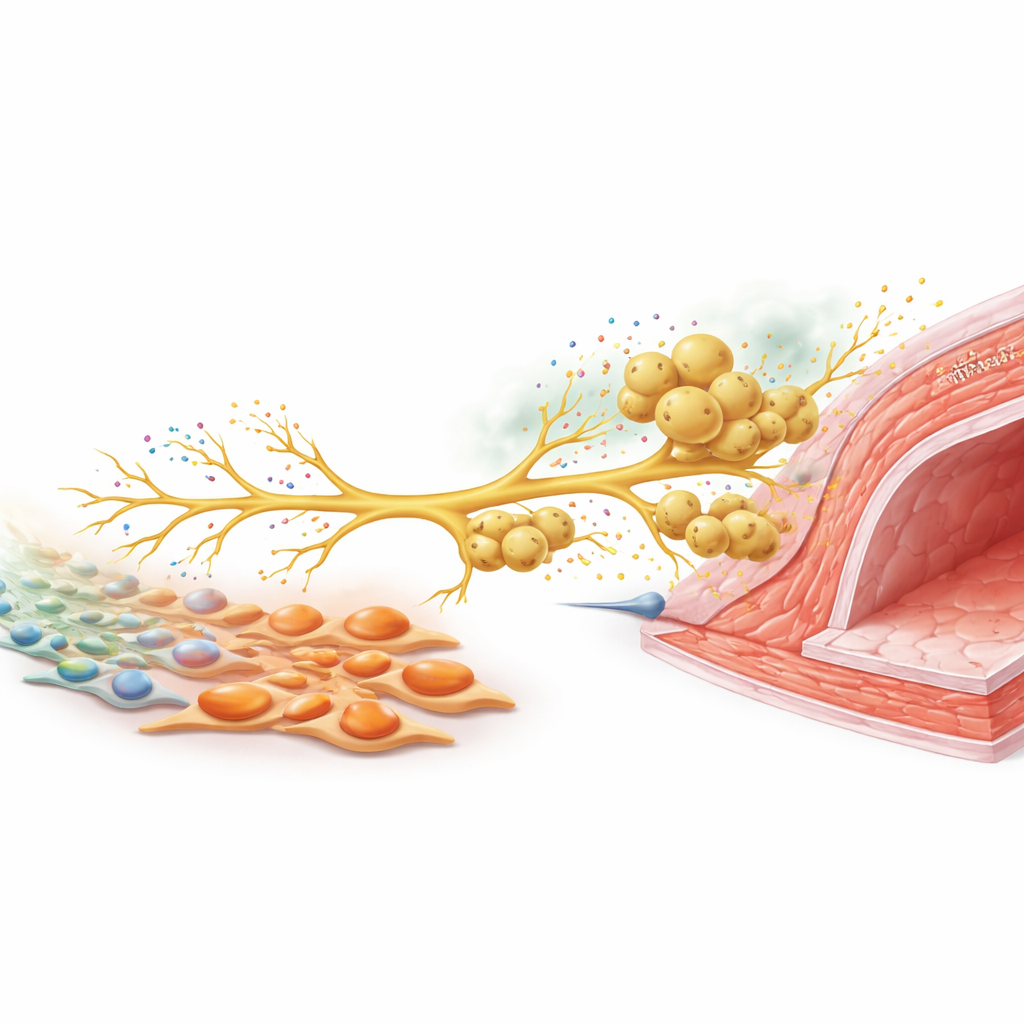
Una señal nerviosa que llama a más defensores
Para entender cómo se comunican estos tipos celulares, el equipo se centró en los nervios sensoriales que detectan estímulos nocivos. En cultivo, los miofibroblastos ricos en tenascina C potenciaron el crecimiento de fibras nerviosas procedentes de neuronas de los ganglios de la raíz dorsal. En ratones lesionados, estas neuronas sensoriales aumentaron la producción de CCL2, una señal química bien conocida por atraer macrófagos. Cuando neuronas y macrófagos se cultivaron juntos, los macrófagos migraron a lo largo de las fibras nerviosas en crecimiento, tal como lo hicieron alrededor de las arterias in vivo. Silenciar la CCL2 en las neuronas redujo marcadamente el reclutamiento de macrófagos. En los animales, reducir la actividad de los nervios sensoriales con una toxina, o eliminar selectivamente la tenascina C solo en fibroblastos, redujo tanto la densidad nerviosa, los niveles de CCL2 y la acumulación de macrófagos, como el engrosamiento de la pared vascular. Combinar ambas intervenciones no aportó un beneficio adicional, lo que sugiere que actúan a lo largo de la misma vía.
Por qué importa esta nueva vía
En conjunto, los hallazgos revelan un círculo vicioso: la lesión induce a los fibroblastos a convertirse en miofibroblastos productores de tenascina C; estas células remodelan la matriz y estimulan los nervios sensoriales; los nervios activados liberan CCL2, que atrae macrófagos; y los macrófagos secretan factores inflamatorios y fibróticos que empeoran la cicatrización y estrechan la arteria. Al identificar la tenascina C y su eje nervio–macrófago downstream como impulsores centrales de este bucle, el trabajo sugiere que los tratamientos dirigidos a esta molécula o a sus socios de señalización podrían ayudar a mantener las arterias reparadas abiertas durante más tiempo, ofreciendo a los pacientes una protección más duradera tras procedimientos cardiovasculares.
Cita: Tong, X., Shi, G., Fang, Z. et al. Tenascin C+ myofibroblasts exacerbate vascular neointimal hyperplasia by propagation of nerve-macrophage interactions in mice. Nat Commun 17, 2199 (2026). https://doi.org/10.1038/s41467-026-69062-3
Palabras clave: hiperplasia neointimal, tenascina C, remodelado vascular, nervios sensoriales, inflamación de macrófagos