Clear Sky Science · es
Paclitaxel impulsa la expansión de macrófagos TREM2+ que subyace a su eficacia terapéutica inferior frente a Nab-paclitaxel
Por qué importa este estudio
Muchas mujeres con cáncer de mama reciben quimioterapia con fármacos llamados taxanos, siendo los más habituales el paclitaxel o una versión más nueva unida a pequeñas partículas de albúmina, conocida como nab‑paclitaxel. Los médicos sospechaban desde hace tiempo que el fármaco más nuevo suele funcionar mejor, pero las razones no estaban claras. Este estudio analiza tanto datos de pacientes como experimentos en animales para mostrar que el paclitaxel estándar puede, de forma no intencionada, facilitar la diseminación del cáncer a los pulmones al remodelar las células inmunitarias del organismo, y apunta a una forma de bloquear este efecto adverso.
Dos fármacos similares, dos resultados distintos
Los investigadores compararon primero el rendimiento en el mundo real del paclitaxel y del nab‑paclitaxel en miles de mujeres con cáncer de mama. Al agrupar los resultados de 17 estudios clínicos con 6.486 pacientes, encontraron que el nab‑paclitaxel produjo tasas más altas de reducción tumoral y más desapariciones completas del cáncer en la mama y los ganglios cercanos antes de la cirugía. Esta ventaja fue especialmente marcada en pacientes tratadas después de que fracasaran terapias previas. Sin embargo, ambos fármacos se administraron en dosis similares y están diseñados para atacar a las células tumorales en división de manera muy parecida, lo que sugiere que algo más allá de la citotoxicidad directa debe ser diferente entre ellos.
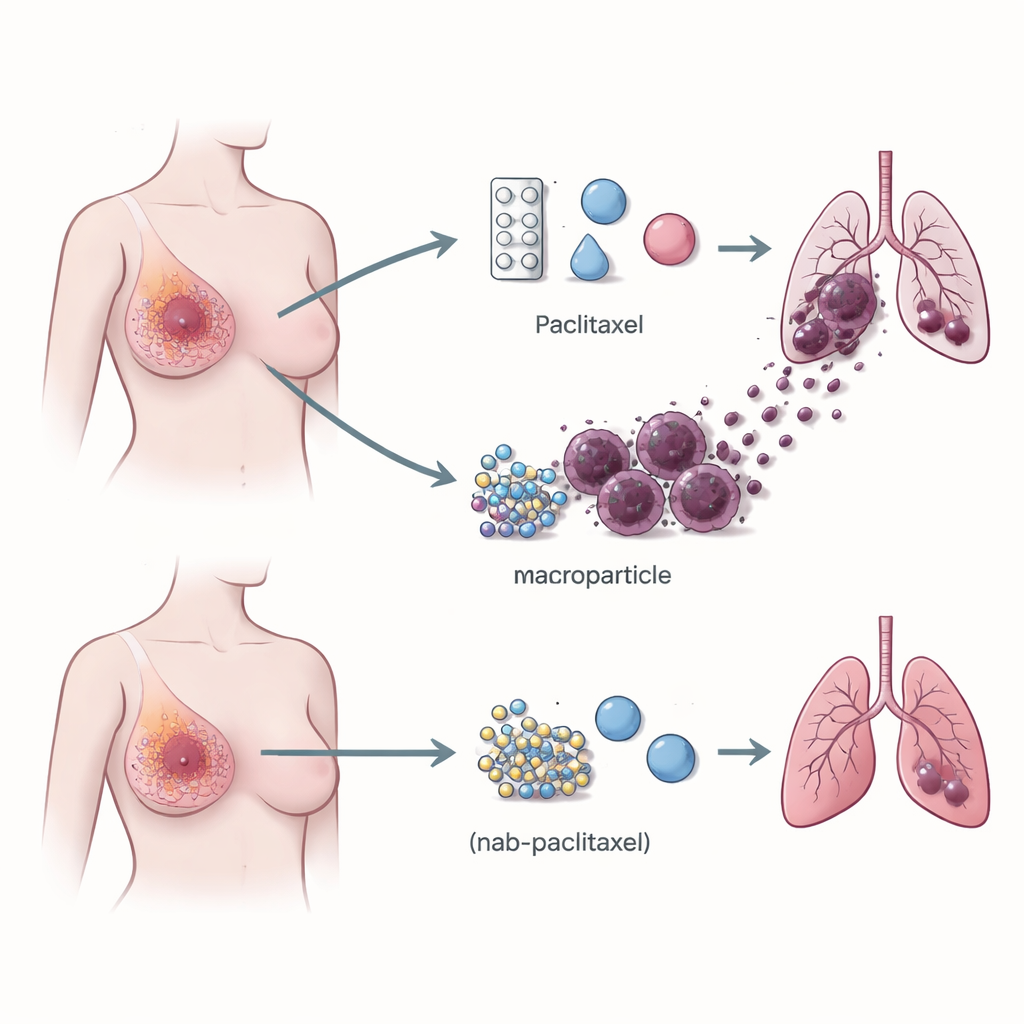
Células inmunitarias que ayudan al cáncer a viajar
La atención se dirigió al entorno inmune del tumor: la mezcla de glóbulos blancos que pueden luchar contra el cáncer o, con sorprendente frecuencia, ayudar a que crezca. Usando secuenciación de ARN a nivel de célula única, que lee la actividad génica en miles de células individuales, el equipo comparó tumores de pacientes tratados con paclitaxel frente a nab‑paclitaxel. Hallaron que los tumores tratados con paclitaxel contenían muchos más macrófagos que portan un receptor llamado TREM2 en su superficie. Estos macrófagos TREM2‑positivos se concentraban en los bordes del tumor y eran mucho más abundantes en pacientes que luego desarrollaron metástasis pulmonares que en aquellas cuyo cáncer permaneció localizado. El patrón se mantuvo en cohortes más grandes y en modelos murinos, estableciendo un vínculo sólido entre este tipo de macrófago y el riesgo de diseminación del cáncer.
Cuando el tratamiento reduce tumores pero favorece la diseminación
En ratones con tumores mamarios, el paclitaxel hizo lo que debe: ralentizó o redujo los tumores primarios. Pero al mismo tiempo aumentó el número de depósitos cancerosos en los pulmones y potenció los macrófagos TREM2‑positivos en los tumores y en la sangre. El nab‑paclitaxel, en contraste, redujo el tamaño tumoral sin promover metástasis pulmonares ni expandir estos macrófagos, pese a ser igualmente eficaz para encoger el tumor principal. Cuando se eliminó el gen de TREM2 en ratones, o cuando se redujo TREM2 con oligonucleótidos antisentido (pequeños fragmentos de ADN que silencian genes específicos), el paclitaxel siguió reduciendo los tumores primarios pero perdió en gran medida su capacidad de fomentar la diseminación pulmonar. Esto muestra que los macrófagos que portan TREM2 no son meros espectadores; son socios necesarios en la metastatización inducida por paclitaxel.
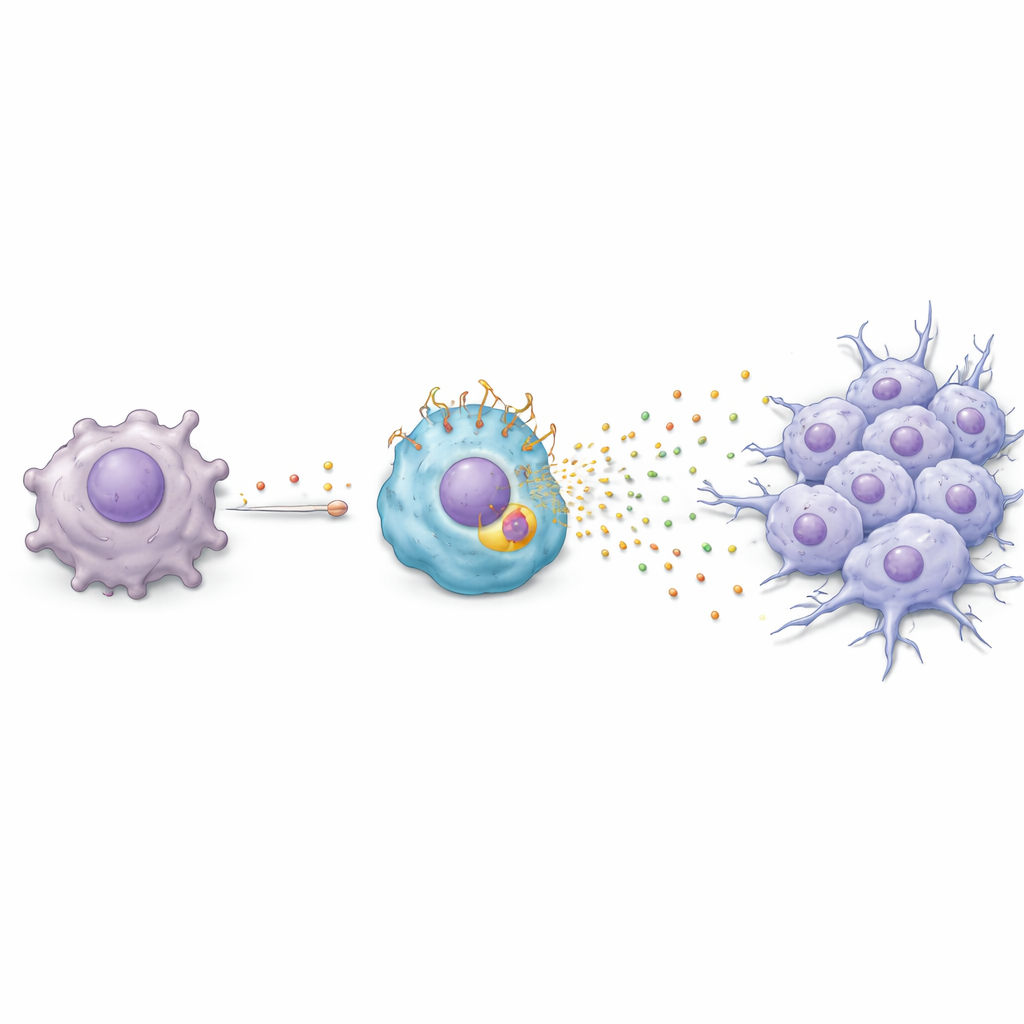
Una reacción en cadena química del tumor a la célula inmune
El equipo investigó luego cómo el paclitaxel induce que los macrófagos adopten este estado perjudicial rico en TREM2. Descubrieron una reacción en cadena: el paclitaxel induce en las células cancerosas la activación de un gen de respuesta al estrés llamado ATF3, que a su vez aumenta la producción de un factor de crecimiento llamado FGF2. Las células tumorales liberan entonces FGF2 en su entorno, donde actúa sobre los macrófagos próximos. En esos macrófagos, FGF2 activa otro regulador, EGR1, que eleva los niveles de TREM2. Una vez alto TREM2, los macrófagos comienzan a secretar una mezcla de proteínas —incluyendo Serpin E1, HGF, CCL3 y CXCL2— que empujan a las células tumorales hacia una forma más móvil e invasiva conocida como transición epitelio‑mesénquima. En cultivos y en ratones, este diálogo químico hizo que las células tumorales fueran más propensas a migrar e invadir, pasos clave en la ruta hacia la metástasis.
Convertir una espada de doble filo en una herramienta más segura
Desde una perspectiva divulgativa, el mensaje clave es que el paclitaxel puede comportarse como una espada de doble filo: mientras ataca los tumores, también instruye a ciertas células inmunitarias para que ayuden al cáncer a escapar hacia órganos distantes. El nab‑paclitaxel parece evitar desencadenar este fallo inmune concreto. La noticia alentadora es que bloquear TREM2 —o partes de la vía de señalización FGF2–EGR1–TREM2— puede separar los beneficios de reducción tumoral del paclitaxel de sus riesgos de promoción de metástasis en modelos animales. Si estrategias similares resultan seguras y efectivas en humanos, los médicos podrían seguir usando un fármaco de quimioterapia familiar y ampliamente disponible mientras reducen su tendencia a favorecer la diseminación del cáncer, conduciendo a mejores resultados a largo plazo para las pacientes.
Cita: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
Palabras clave: cáncer de mama, paclitaxel, microambiente tumoral, macrófagos, metástasis