Clear Sky Science · es
Reutilización fiable del interactoma de anticuerpos dentro de la célula
Convertir anticuerpos en pequeñas herramientas dentro de nuestras células
Los anticuerpos son famosos como las armas de precisión del torrente sanguíneo, localizando virus y otras amenazas. Pero gran parte de la actividad en muchas enfermedades, incluidas la enfermedad de Alzheimer, el Parkinson y algunos cánceres, ocurre dentro de las células, donde los anticuerpos convencionales rara vez llegan o funcionan bien. Este estudio muestra cómo reconstruir sistemáticamente anticuerpos existentes en versiones más pequeñas, llamadas “intrabodies”, que funcionan de forma fiable dentro de células humanas vivas, abriendo la puerta a nuevos diagnósticos, herramientas de investigación y, potencialmente, futuras terapias que actúen directamente en el núcleo de los procesos patológicos.
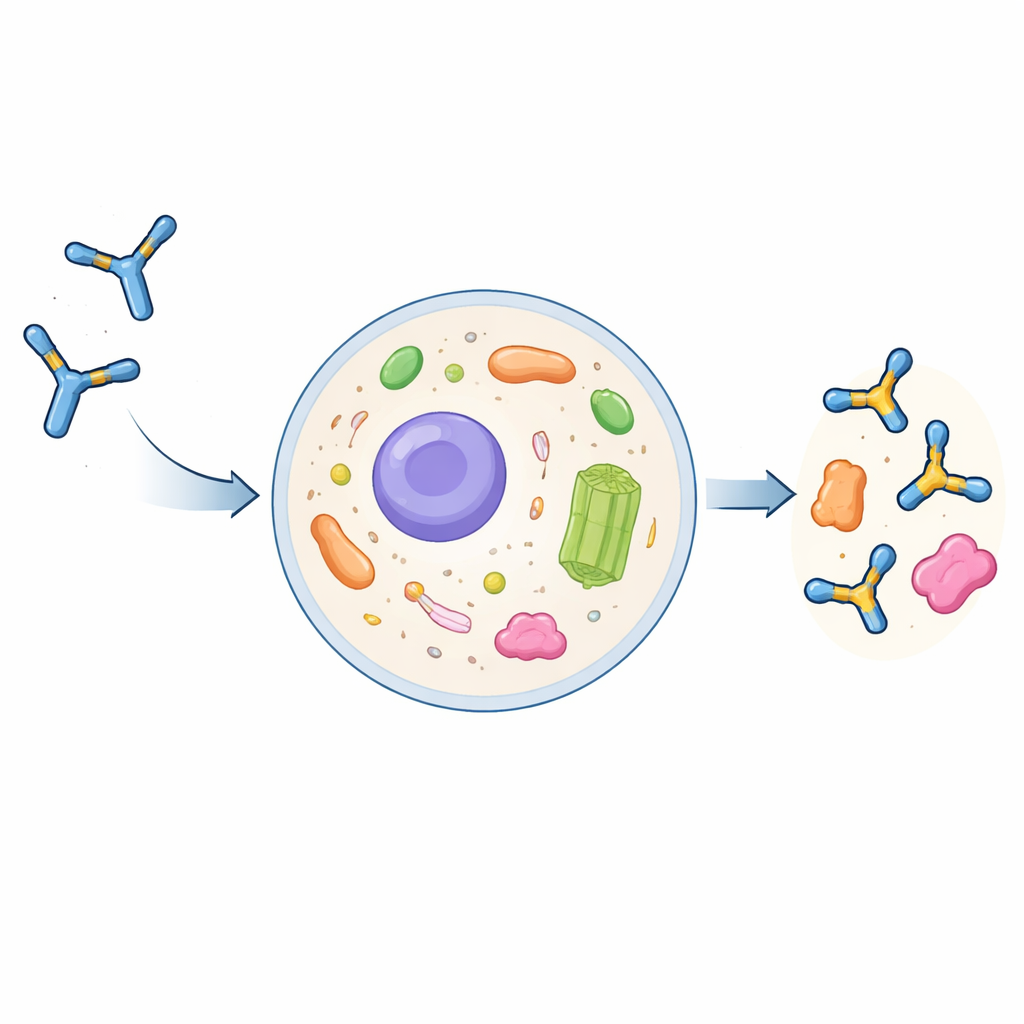
Por qué los anticuerpos convencionales tienen dificultades dentro de las células
Los anticuerpos de tamaño completo son proteínas grandes con forma de Y evolucionadas para funcionar fuera de las células. Se ensamblan y modifican químicamente en la vía secretora de la célula y luego se liberan al torrente sanguíneo. Si las células los internalizan, normalmente acaban en compartimentos de degradación en lugar del interior fluido de la célula, el citoplasma. Los científicos pueden recortar los anticuerpos hasta sus partes esenciales de reconocimiento, llamadas fragmentos variables de cadena única (scFv), y expresar estos como intrabodies dentro de las células. Sin embargo, estos intrabodies a menudo se agrupan, se vuelven insolubles y pierden su capacidad para unirse a sus dianas. Hasta ahora, no había una receta general y fiable para convertir un anticuerpo convencional en un intrabody que se comporte bien.
Encontrar las reglas de diseño para intrabodies solubles
Los investigadores empezaron midiendo cuánto se mantenían disueltos 45 intrabodies distintos cuando se producían en células humanas. Compararon sistemáticamente muchas características de las proteínas —como la hidrofobicidad global, la calidad de la estructura predicha y las propiedades de los bucles de unión— para ver cuáles explicaban mejor si un intrabody permanecía soluble. Un factor simple destacó: la carga eléctrica global a pH cercano al fisiológico. Los intrabodies con una carga neta fuertemente negativa tenían mucha más probabilidad de mantenerse solubles, mientras que los de carga neutra o positiva tendían a agregarse. Otros predictores sofisticados, incluidos los puntajes de confianza estructural del sistema AlphaFold, no se correlacionaron con la solubilidad. Esto permitió al equipo construir un modelo práctico basado en la carga que puede estimar qué fracción de un intrabody se encontrará en la fracción soluble de un extracto celular.
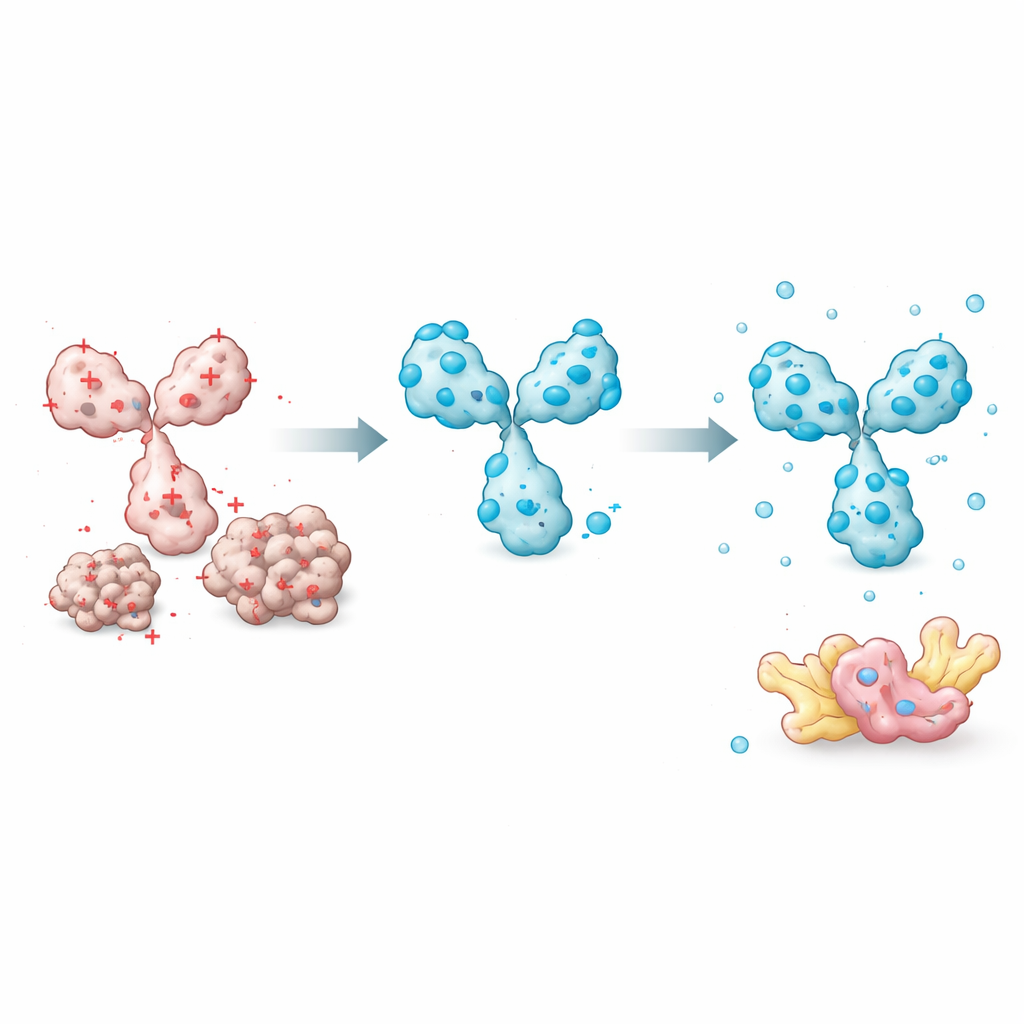
Reingeniería de conectores y dominios para mejorar el comportamiento
Con este conocimiento, el equipo se centró en características que podían ajustar fácilmente sin alterar cómo un intrabody reconoce su diana. Un elemento clave es el péptido corto «conector» que une los dos dominios variables. La mayoría de los diseños existentes usan conectores neutros que no alteran la carga. Al sustituir aminoácidos con carga negativa en estas posiciones, los investigadores pudieron bajar la carga global del intrabody, mejorando drásticamente la solubilidad sin afectar la unión a la diana. También descubrieron que el orden de los dominios variables (si la parte pesada o la ligera va primero) y posiciones específicas del marco fuera de los bucles de unión influyen en la facilidad con que la proteína se pliega y se mantiene disuelta. Elegir un orden de dominios que proteja las regiones más frágiles e introducir mutaciones de intercambio de carga colocadas con cuidado incrementó aún más el rendimiento.
Usar inteligencia artificial para construir intrabodies a escala
Para ir más allá del ensayo y error individual, los autores combinaron sus sencillas reglas de carga con software avanzado de diseño de proteínas basado en aprendizaje profundo. Partiendo de esqueletos de anticuerpos conocidos, utilizaron un enfoque de «plegamiento inverso» para proponer nuevas secuencias que adoptaran la forma deseada pero presentaran características superficiales —especialmente patrones de carga— que favorecieran la estabilidad y la solubilidad. Restringieron los cambios en los bucles de unión clave para preservar el reconocimiento, permitiendo al algoritmo rediseñar las superficies circundantes. Las pruebas mostraron que muchos de estos intrabodies guiados por IA no solo eran altamente solubles, sino también más estables térmicamente que variantes diseñadas por humanos, y conservaban la capacidad de unirse a dianas relevantes para la enfermedad como SOD1 malplegada, p53, α-sinucleína y otras proteínas vinculadas a la neurodegeneración.
Construir una biblioteca de captadores de proteínas dentro de la célula
Aplicando estas reglas y herramientas a gran escala, el equipo reformateó computacionalmente 672 anticuerpos en intrabodies predichos para funcionar bien dentro de las células. Estas moléculas diseñadas abarcan más de 60 dianas intracelulares diferentes, incluidas proteínas implicadas en las enfermedades de Alzheimer, Parkinson y Huntington, así como factores relacionados con el cáncer y modificaciones postraduccionales como la fosforilación y la acetilación. En experimentos, intrabodies seleccionados lograron capturar formas específicas de proteínas vinculadas a enfermedades, como SOD1 mutante o conformaciones particulares de α-sinucleína, mientras ignoraban las versiones normales. Todas las secuencias se han publicado abiertamente, y los autores ofrecen una herramienta web que permite a otros estimar la solubilidad de intrabodies a partir de la secuencia usando el mismo modelo basado en la carga.
Qué significa esto para futuras medicinas e investigación
En términos prácticos, este trabajo convierte la vasta colección existente de anticuerpos —muchos ya estudiados en clínica— en un conjunto de herramientas que puede adaptarse de forma fiable para su uso dentro de las células. Siguiendo un conjunto sencillo de reglas de diseño, los investigadores pueden ahora crear intrabodies que probablemente funcionen en el primer intento, ahorrando tiempo y costes. Para un público general, el mensaje clave es que los científicos han encontrado una forma simple de «reconfigurar» nuestros mejores detectores proteicos para que funcionen en el interior abarrotado de las células vivas, donde empiezan muchas enfermedades. Esto podría acelerar el desarrollo de nuevas maneras de rastrear, estudiar y, eventualmente, tratar condiciones impulsadas por proteínas mal plegadas o que funcionan mal.
Cita: O’Shea, C.M., Shahzad, R., Aghasoleimani, K. et al. Reliable repurposing of the antibody interactome inside the cell. Nat Commun 17, 2222 (2026). https://doi.org/10.1038/s41467-026-69057-0
Palabras clave: intrabodies, ingeniería de anticuerpos, solubilidad de proteínas, enfermedad neurodegenerativa, inteligencia artificial en biología