Clear Sky Science · es
Secuenciación dual de ARN in vivo descubre efectores clave de la interrupción de la barrera epitelial por un patógeno extracelular
Cómo algunos gérmenes se cuelan más allá de nuestras vallas celulares
Nuestros órganos están revestidos por células estrechamente empaquetadas que actúan como muros, manteniendo la sangre, los microbios y las toxinas donde deben estar. Sin embargo, ciertos gérmenes aún se deslizan entre estas células y se dispersan por el cuerpo. Este estudio revela con nitidez cómo la bacteria que causa la leptospirosis, una enfermedad grave a nivel mundial, alcanza silenciosamente órganos como el hígado y los riñones, y luego utiliza un truco inteligente que involucra el calcio dentro de nuestras células para forzar la apertura de estas barreras protectoras.
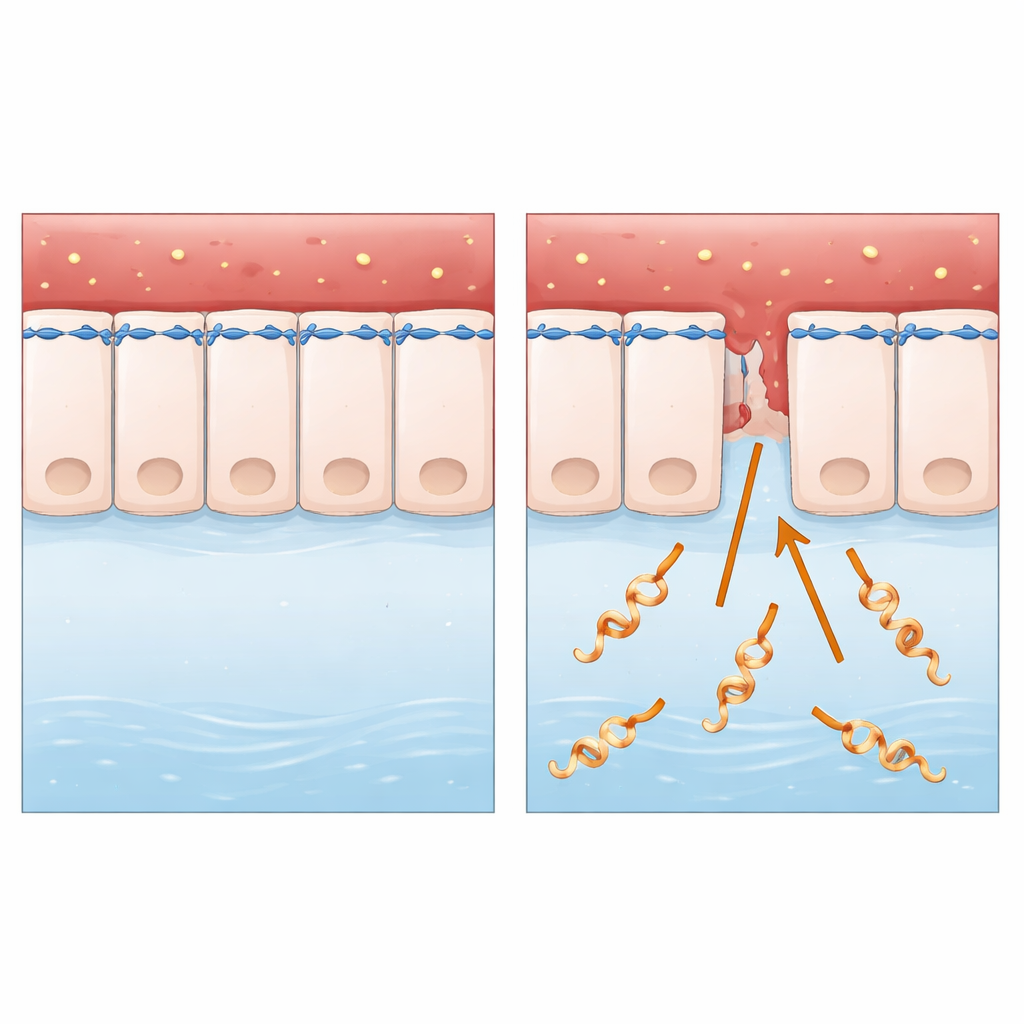
Un invasor sigiloso de tejidos animales y humanos
La investigación se centra en Leptospira interrogans, una bacteria en forma de espiral que se transmite principalmente de animales a humanos a través de agua o suelo contaminados. Tras entrar por pequeñas roturas en la piel o mucosas, viaja por el torrente sanguíneo y puede desencadenar una enfermedad grave, incluyendo fallo hepático y renal y hemorragias internas. A diferencia de muchos microbios bien estudiados, Leptospira vive fuera de las células y carece de algunas de las “armas moleculares” clásicas que los científicos suelen buscar. Eso la convirtió en un caso ideal para plantear una pregunta básica: ¿cómo atraviesa con tanta eficacia una bacteria aparentemente simple y extracelular capas celulares intactas?
Viendo simultáneamente el diálogo entre genes del huésped y del germen
Para capturar el proceso de infección dentro de un animal vivo, el equipo usó secuenciación dual de ARN en hámsters, un modelo de leptospirosis aguda. Este método registra qué genes se activan o desactivan tanto en el huésped como en el patógeno al mismo tiempo. Los científicos infectaron hámsters y recogieron tejido de hígado y riñón al día uno y al día tres. Al principio, a pesar de los altos números de bacterias, las células del animal apenas cambiaron su actividad génica, lo que sugiere que Leptospira inicialmente pasa desapercibida para el sistema inmunitario. Sin embargo, al día tres, ambos órganos mostraron una reacción fuerte, especialmente el hígado: los genes implicados en la inflamación, las uniones célula‑célula y el armazón interno de las células se alteraron notablemente, lo que apunta a una remodelación activa de las barreras tisulares.
Rompiendo la cremallera celular desde fuera hacia dentro
Las capas celulares están selladas por uniones estrechas y adherentes, que enlazan células vecinas y las anclan a un anillo de actina y miosina, la misma pareja de proteínas que ayuda a contraer los músculos. La microscopía de células epiteliales humanas infectadas con Leptospira mostró que su forma cambiaba, se abrían huecos entre las células y las proteínas clave de las uniones se debilitaban o redistribuían. Importante: las células no morían, lo que indica que la barrera se estaba desmantelando, no destruyendo. Los investigadores también observaron señales de estrés en las fábricas de plegamiento de proteínas de las células, pero bloquear ese estrés no restauró las uniones, lo que los orientó hacia otro sospechoso.
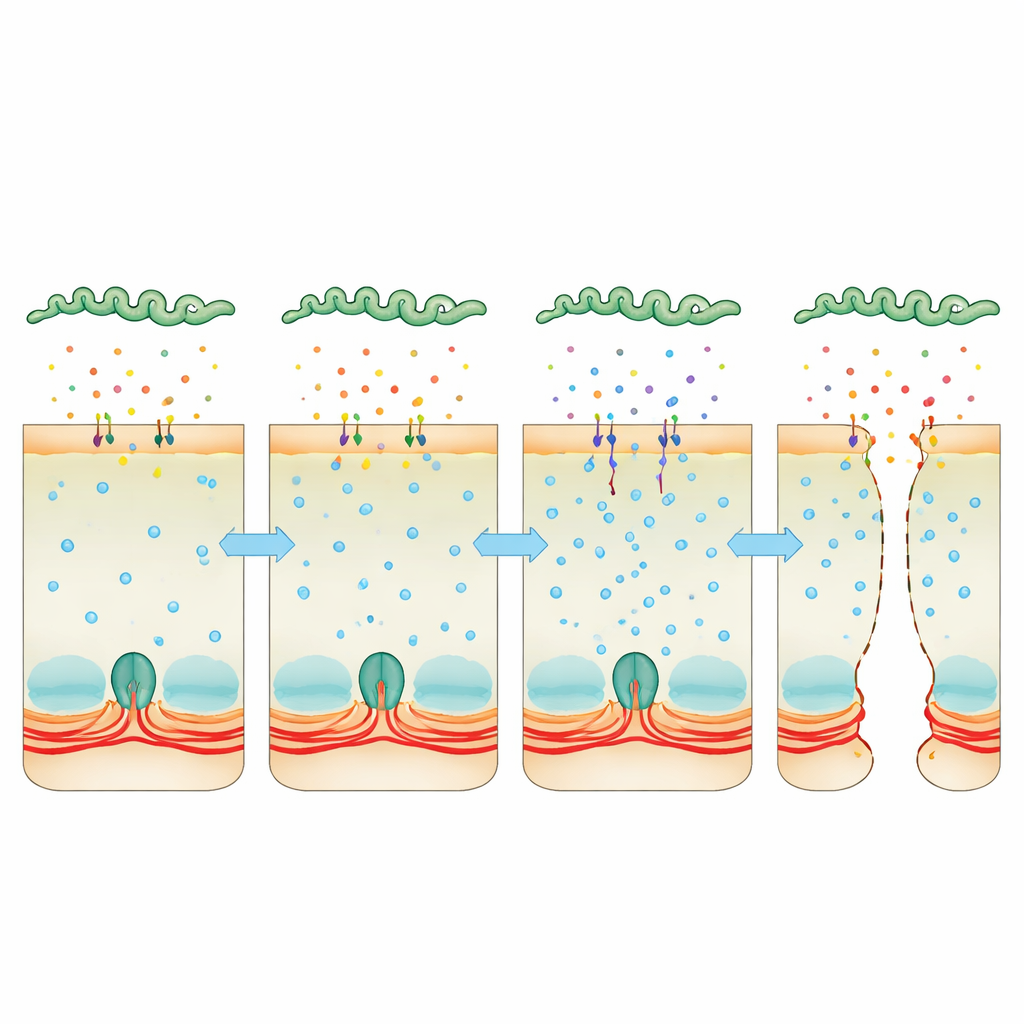
Secuestrando el calcio como palanca oculta
La atención se centró en el calcio, una señal universal dentro de las células que puede tensar o relajar el anillo de actina‑miosina. Las células infectadas acumularon más calcio, y esto se vinculó a una mayor actividad de la quinasa de la cadena ligera de miosina, una enzima que hace que el anillo contráctil tire de las uniones. Cuando el equipo usó un compuesto que elimina el calcio, o fármacos que inhiben la calmodulina o esta quinasa, las capas celulares permanecieron más intactas y a las bacterias les resultó más difícil colarse. Al mismo tiempo, la secuenciación profunda del ARN bacteriano reveló que, dentro del huésped, Leptospira aumenta fuertemente la producción de dos proteínas “modificadoras de virulencia” que se asemejan a toxinas. Estas proteínas se secretan al entorno, se adhieren a las células del huésped y se encuentran dentro de ellas. Cuando las bacterias carecían de una o ambas de estas proteínas, tenían mucha menos capacidad para atravesar capas celulares o causar una enfermedad letal, y su caldo secretado ya no elevaba los niveles de calcio ni desmantelaba las uniones con la misma eficacia.
Qué significa esto para la enfermedad y las defensas futuras
En conjunto, los resultados delinean una historia clara. Tras entrar en el cuerpo casi sin ser detectada, Leptospira comienza a secretar proteínas modificadoras de virulencia similares a toxinas. Estas proteínas se unen a las células epiteliales y alteran el equilibrio de calcio en su interior, lo que a su vez activa una vía contráctil que separa la “cremallera” celular que mantiene unidas a las células vecinas. A medida que las uniones estrechas y adherentes se aflojan, aparecen huecos microscópicos que permiten a las bacterias pasar entre las células, colonizar órganos y desencadenar una enfermedad grave. Al identificar este mecanismo impulsado por el calcio y las proteínas bacterianas responsables, el estudio abre un camino hacia nuevas estrategias —como bloquear estas proteínas o su ruta de señalización— para reforzar nuestras vallas celulares y limitar la diseminación de la leptospirosis y posiblemente de otras infecciones que explotan tácticas similares.
Cita: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
Palabras clave: leptospirosis, barrera epitelial, señalización del calcio, toxinas bacterianas, interacciones huésped‑patógeno