Clear Sky Science · es
nDIA-MS potenciado con supercarga permite el perfilado global de los cambios de solubilidad del proteoma inducidos por fármacos
Por qué importa el comportamiento de las proteínas más allá de las simples cantidades
Los medicamentos pueden cambiar no solo cuánto de una proteína produce una célula, sino también a dónde va esa proteína y si circula libremente o se aglutina sobre estructuras celulares. Esas variaciones en el “dónde” y el “cómo” de la existencia de las proteínas dentro de la célula están estrechamente vinculadas a enfermedades como el cáncer y la neurodegeneración, pero son difíciles de medir a gran escala. Este estudio presenta una forma rápida y potente de escanear miles de proteínas humanas a la vez para ver cómo cambia su solubilidad —si están en un estado más libre o más fijo— cuando las células se exponen a dos fármacos experimentales de uso común.
Una manera más rápida y nítida de observar proteínas
Los autores se apoyan en una tecnología central de la biología moderna: la espectrometría de masas, una técnica que pesa y cuenta fragmentos proteicos. Los métodos estándar ya sobresalen en decirnos cuánto hay de cada proteína, pero tienen dificultades para revelar cambios en el estado proteico, como la unión al ADN o la incorporación en ensamblajes densos. Aquí, los investigadores refinan una versión de espectrometría llamada adquisición de datos independiente en ventana estrecha (nDIA-MS). Al añadir pequeños agentes químicos, denominados reactivos de supercarga, al líquido que transporta péptidos dentro del instrumento, aumentan las cargas eléctricas de esos fragmentos y refuerzan considerablemente la señal.
Tras probar dos aditivos comunes de supercarga, dimetilsulfóxido (DMSO) y m-nitrobencil alcohol (mNBA), encuentran que un 3% de DMSO ofrece el mayor incremento de señal global y el mayor número de proteínas detectadas, mientras que mNBA es mejor para aumentar el número y la carga de fragmentos peptídicos individuales. Con la configuración optimizada, el equipo puede identificar alrededor de 9.600 proteínas humanas a partir de solo un microgramo de un digest estándar de células en una corrida de 15 minutos; una combinación notable de velocidad y profundidad para experimentos de rutina. Este rendimiento prepara el terreno para usar nDIA-MS no solo para cuantificar proteínas, sino para sondear cómo su estado físico responde al estrés.
Convertir la solubilidad en una lectura del cambio celular
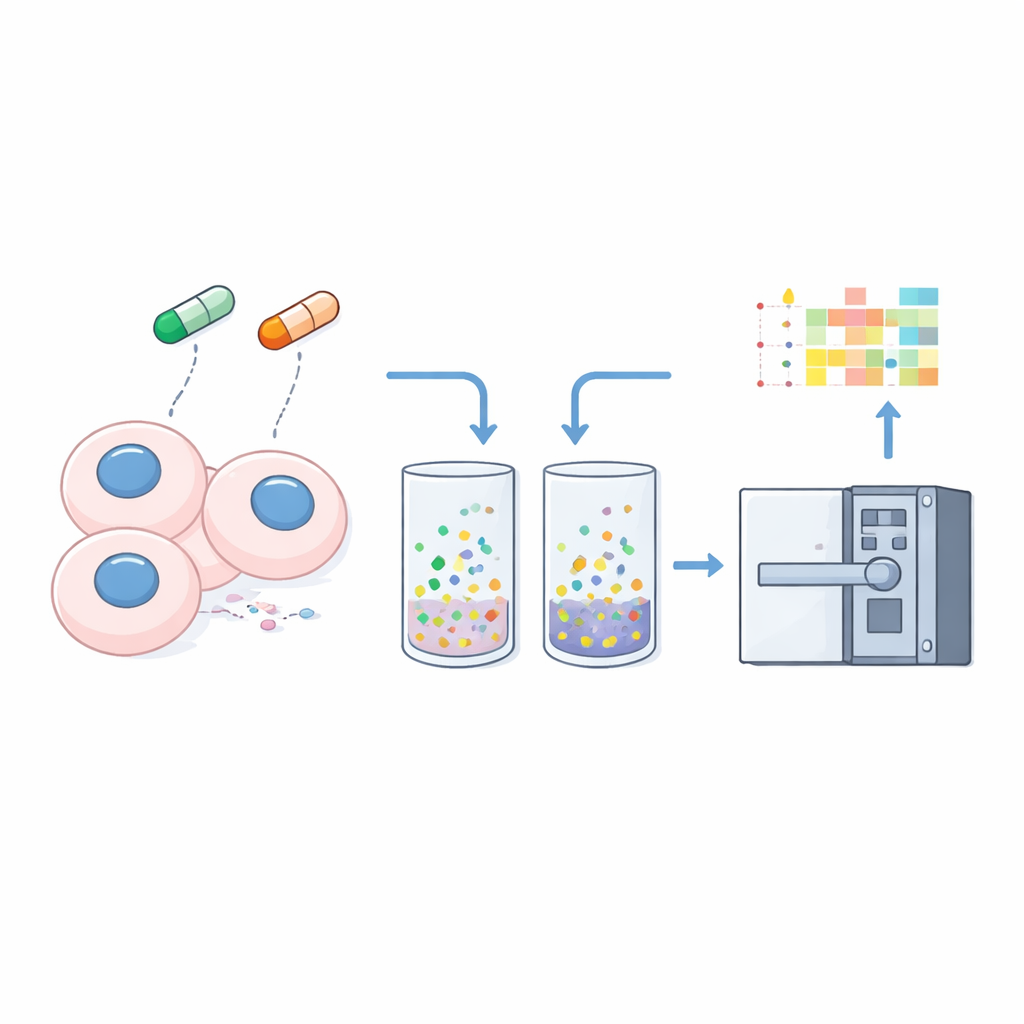
Para transformar la solubilidad en una señal medible, los investigadores tratan suavemente las células con un detergente leve que extrae las proteínas libremente solubles, dejando atrás material fuertemente asociado al ADN, a las membranas u otras estructuras. Analizan tanto el lisado celular total como este pellet “insoluble” de tres líneas celulares cancerígenas usando el método nDIA-MS optimizado. Al comparar la abundancia de cada proteína en el pellet respecto a la muestra total, calculan una “relación de insolubilidad” sencilla: valores más altos sugieren una asociación más fuerte con estructuras celulares, valores más bajos sugieren un estado más soluble y libre.
El equipo expone luego las células durante solo una hora a dos fármacos: MG132, un bloqueador del proteasoma que impide que la célula degrade proteínas no deseadas, y ML‑792, un inhibidor de la activación de SUMO que interfiere con un sistema clave de etiquetado proteico. Esta exposición breve es deliberada; pretende capturar cambios rápidos y tempranos en el comportamiento proteico antes de que los cambios en la expresión génica se desarrollen por completo. Incluso en esta ventana corta, pueden cuantificar cambios de solubilidad y abundancia para 8.694 proteínas y confirmar que su fraccionamiento separa limpiamente proteínas clásicamente solubles, como la tubulina, de proteínas unidas a la cromatina, como las histonas.
Fármacos que remodelan el paisaje proteico celular
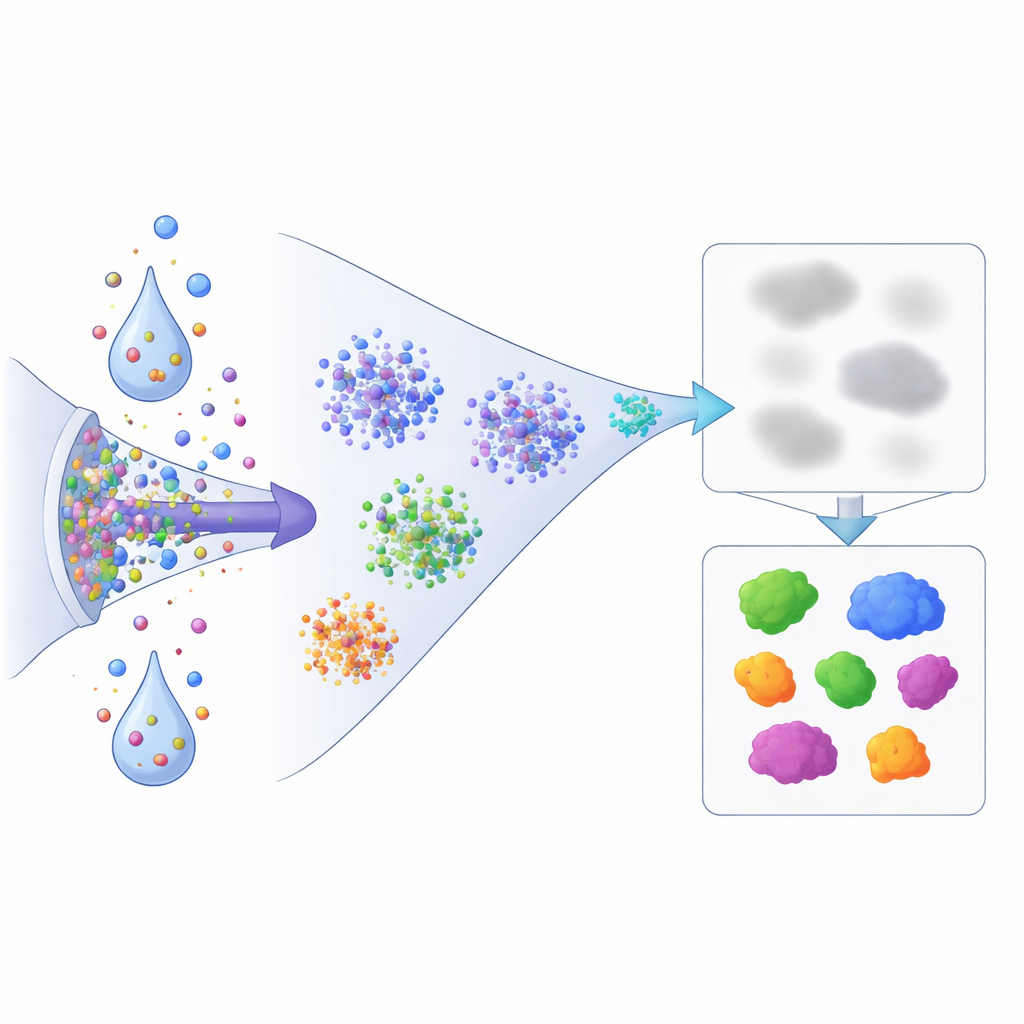
MG132 y ML‑792 producen una remodelación extensa pero distinta de la solubilidad proteica. MG132 hace que más de mil proteínas se vuelvan más insolubles y que más de seiscientas se vuelvan más solubles a lo largo de las tres líneas celulares. Muchas proteínas afectadas se sitúan en la intersección del control de calidad proteico, la respuesta al daño del ADN, la regulación génica y la autofagia —el sistema de limpieza celular—. Por ejemplo, componentes del complejo activador del proteasoma y adaptadores que ayudan a etiquetar proteínas defectuosas se vuelven menos solubles, lo que sugiere que cuando la degradación está bloqueada, factores clave de control de calidad quedan atrapados en estructuras como la cromatina o las membranas celulares. Proteínas de la autofagia y actores de la respuesta al daño, incluido el regulador del estrés HSF1, también se desplazan hacia estados más insolubles, similares a condensados, consistente con la formación de cuerpos de estrés nucleares.
ML‑792, en contraste, apunta con fuerza a proteínas implicadas en la transcripción y en el propio sistema SUMO. Cientos de proteínas se vuelven más insolubles o más solubles cuando se bloquea la activación de SUMO, y las proteínas SUMO centrales se incorporan a la fracción soluble, como era de esperar. El estudio destaca comportamientos llamativos: subunidades de la ARN polimerasa III se vuelven más insolubles, lo que sugiere una alteración en la importación nuclear o en la unión a la cromatina; represores clave asociados a cuerpos nucleares, como SP100 y DAXX, se vuelven más solubles, lo que indica que las marcas SUMO ayudan a mantenerlos secuestrados en esos compartimentos. Cuando ambos fármacos se aplican solos o en secuencia, algunas proteínas, incluidas NAB2, SMAD2 y RB1, muestran cambios de insolubilidad coordinados o incluso opuestos, revelando una interacción matizada entre los sistemas de etiquetado por ubiquitina y SUMO en el control de la localización proteica.
Qué significa esto para el descubrimiento de fármacos futuro
Para el público no especialista, el mensaje central es que las proteínas no solo aumentan o disminuyen en cantidad cuando las células están estresadas o tratadas con fármacos; también se mueven, se condensan y cambian cuán fuertemente están vinculadas a estructuras celulares. Este trabajo ofrece una forma a gran velocidad y a nivel proteómico de observar esos cambios. Al combinar un flujo de trabajo de espectrometría de masas afinado con una comparación simple soluble-versus-insoluble, los autores muestran que fármacos experimentales comunes reorganizan rápidamente el paisaje proteico interno de maneras que las mediciones de abundancia estándar pasarían por alto. El enfoque abre la puerta a cartografiar cómo los candidatos a fármacos remodelan los estados proteicos en toda la célula, ayudando a los investigadores a descubrir dianas inesperadas, vías de estrés y puntos de fallo que podrían ser cruciales para entender tanto la acción terapéutica como los efectos secundarios.
Cita: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
Palabras clave: solubilidad del proteoma, espectrometría de masas, inhibidor del proteasoma MG132, inhibidor de SUMOilación ML-792, transiciones de estado proteico