Clear Sky Science · es
La arquitectura interna diseñada de nanopartículas lipídicas núcleo-capa promueve una liberación endosomal eficiente del ARNm
Por qué importa este nuevo truco de entrega
Muchos de los medicamentos más prometedores, desde las vacunas contra la COVID-19 hasta tratamientos experimentales contra el cáncer, están hechos a partir de ARN mensajero, o ARNm. Pero hay un problema persistente: una vez que estas cadenas frágiles entran en nuestras células, la mayoría queda atrapada y destruida en pequeños compartimentos internos llamados endosomas. Este estudio presenta un rediseño ingenioso de las diminutas burbujas grasas, conocidas como nanopartículas lipídicas, que transportan el ARNm. Al reorganizar su estructura interna alrededor de un núcleo de oro sólido, los investigadores mejoran drásticamente la cantidad de ARNm que escapa al espacio de trabajo de la célula, donde puede realmente producir proteínas útiles.
Dar a los pequeños mensajeros un mejor plano corporal
Las vacunas y terapias de ARNm actuales dependen en su mayoría de partículas blandas y amorfas compuestas por una mezcla de lípidos que envuelven el ARNm. En teoría, lípidos “ionizables” especiales en estas partículas deberían volverse cargados positivamente en el interior ácido de los endosomas y romper la membrana endosomal, liberando el ARNm. En la práctica, la carga negativa del ARNm cancela gran parte de este efecto, por lo que solo alrededor del 2 % del ARNm entregado llega alguna vez a la maquinaria celular de producción de proteínas. Los autores se hicieron una pregunta simple pero poderosa: en lugar de cambiar solo la química de los lípidos, ¿y si re‑ingenieran la arquitectura interna de la partícula para controlar dónde se sitúan el ARNm y los lípidos entre sí?
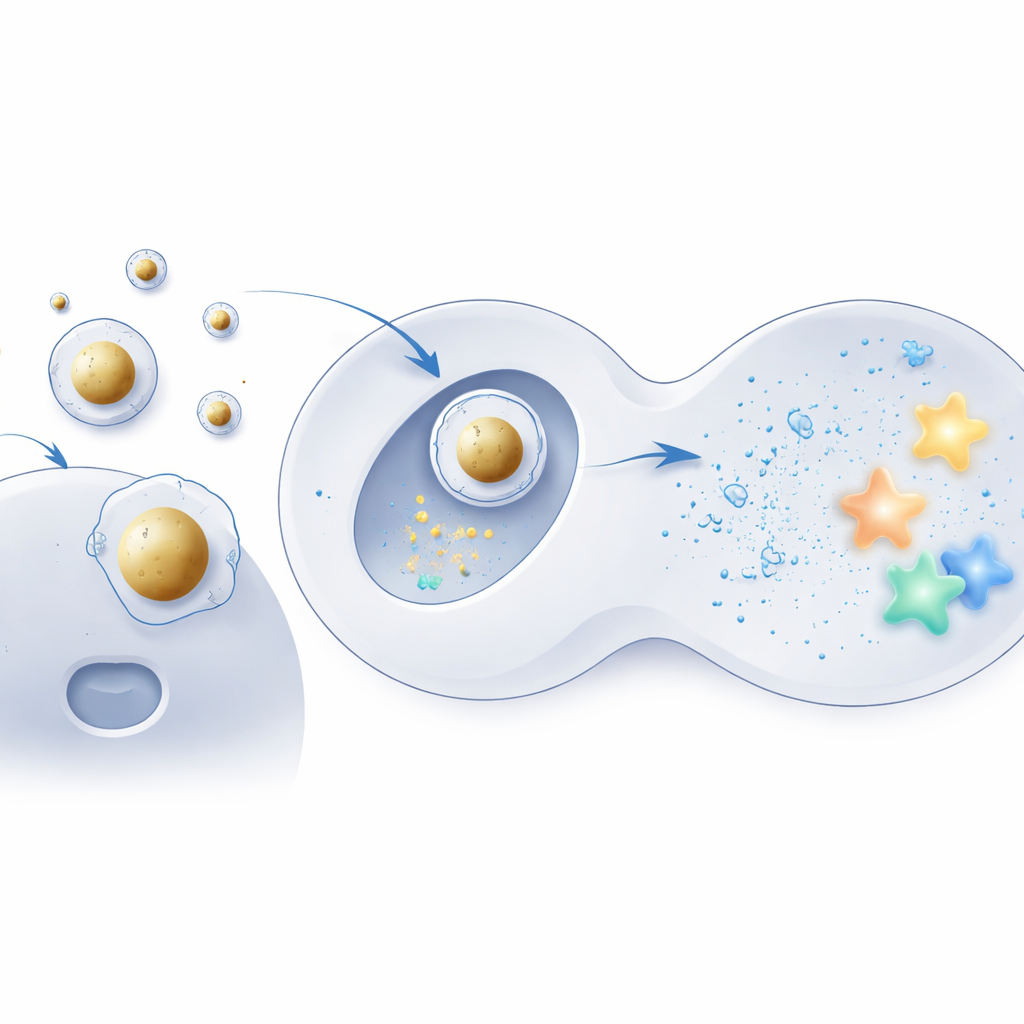
Construir una cubierta de entrega centrada en oro
Para probar esta idea, el equipo utilizó esferas diminutas de oro como núcleos rígidos y las recubrió con los mismos lípidos ionizables usados en formulaciones convencionales. El ARNm, cargado negativamente, se condensó primero sobre estos núcleos y solo después el ensamblaje se envolvió en una mezcla conocida de lípidos auxiliares y moléculas estabilizadoras, creando una estructura núcleo–capa ordenada. La microscopía electrónica y las simulaciones por ordenador mostraron que estas “Au‑LNPs” eran muy uniformes, termodinámicamente estables y mantenían bien su forma en condiciones acuosas y similares al cuerpo. Es importante que su composición lipídica global permaneciera igual que la de las partículas estándar, aislando la estructura interna —no los ingredientes— como el cambio clave.
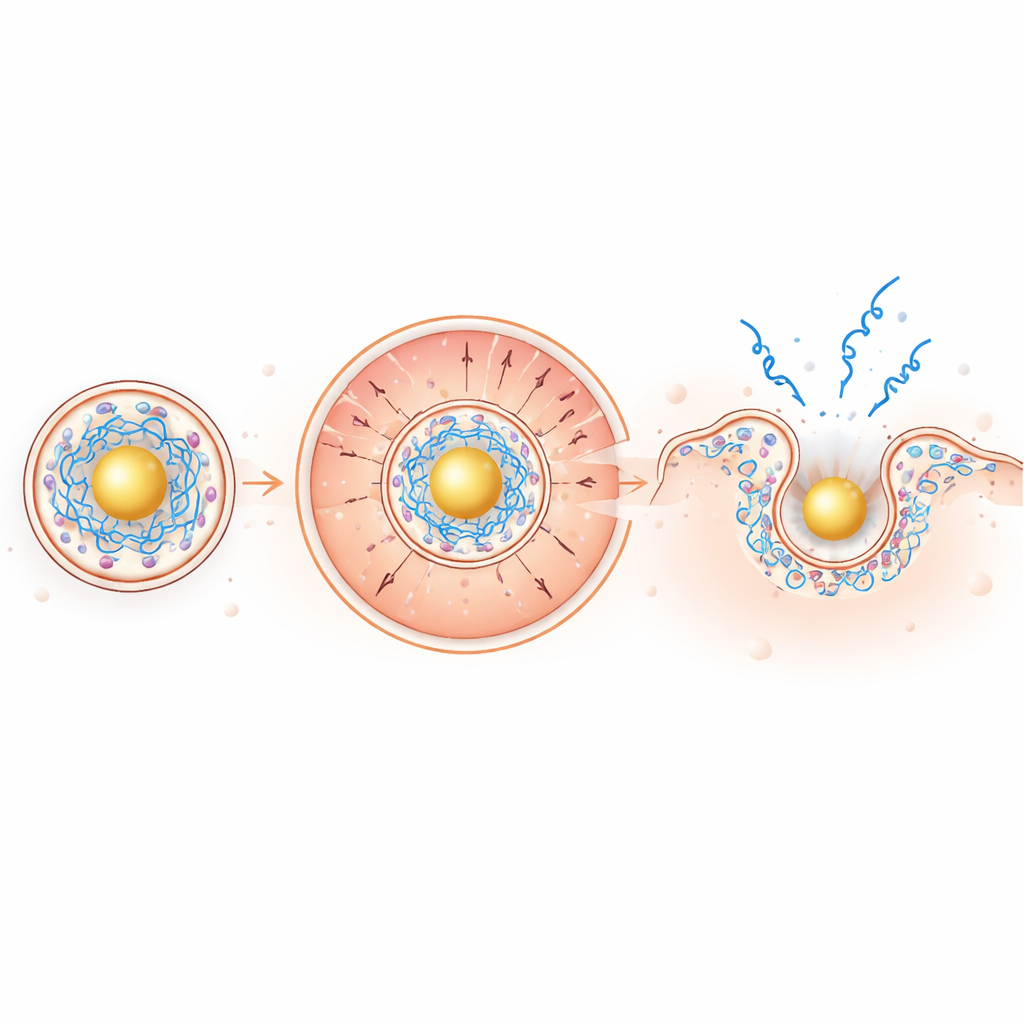
Cómo un interior reorganizado potencia el escape
En el ambiente endosomal, levemente ácido, el núcleo basado en oro se vuelve fuertemente positivo, atrayendo al ARNm cargado negativamente hacia el interior mientras empuja a los lípidos ionizables cargados positivamente hacia afuera, hacia la membrana circundante. Esta segregación impulsada por cargas concentra los lípidos disruptores de membrana exactamente donde se necesitan. En pruebas con membranas modelo y en glóbulos rojos, las nuevas partículas fueron más efectivas perforando membranas a pH bajo mientras permanecían inactivas a pH neutro, una característica de seguridad deseable. En células vivas, la imagen del ARNm fluorescente reveló aproximadamente un aumento de dos veces en el escape endosomal y un asombroso aumento de ~100 veces en la extensión del ARNm por el citoplasma en comparación con las partículas convencionales.
De placas a ratones: señales más fuertes y mayor protección
Estas ventajas físicas se tradujeron en ganancias biológicas reales. En varios tipos celulares, las partículas con núcleo de oro impulsaron una producción de proteínas reporteras mucho mayor que las formulaciones estándar, especialmente a dosis bajas. En ratones, aumentaron la producción de proteína dirigida por ARNm hasta cinco‑siete veces tras inyecciones en músculo o venas, sin cambiar dónde tienden a acumularse las partículas en el cuerpo. Al usarlas para entregar una vacuna de ARNm contra la espícula del SARS‑CoV‑2, las partículas rediseñadas duplicaron aproximadamente los niveles de anticuerpos tras la primera dosis y los incrementaron más después de un refuerzo, además de generar anticuerpos neutralizantes del virus más potentes. En un modelo desafiante de cáncer de mama triple negativo, las vacunas de ARNm transportadas por las nuevas partículas redujeron los tumores de forma más efectiva, disminuyeron las señales de actividad tumoral y prolongaron notablemente la supervivencia.
Seguridad y un camino hacia futuros medicamentos
A pesar de usar oro en su núcleo, las partículas parecieron bien toleradas en ratones. El peso corporal, los marcadores inflamatorios y los exámenes de tejidos no mostraron toxicidad importante, y los niveles de oro en los órganos volvieron cerca de la línea de base en dos días. Los autores subrayan que el oro sirve principalmente como andamiaje de prueba de concepto: el mismo principio de diseño interno podría aplicarse a otros materiales seguros o biodegradables. El mensaje central para no especialistas es que cómo empaquetamos el ARNm dentro de su diminuto transportador puede importar tanto como con qué lo empaquetamos. Al dotar a las nanopartículas lipídicas de una disposición interna más disciplinada, este trabajo ofrece una nueva forma de superar un cuello de botella de larga data en la entrega de ARNm —desbloqueando vacunas y terapias más efectivas contra enfermedades infecciosas, cáncer y más allá.
Cita: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
Palabras clave: entrega de ARNm, nanopartículas lipídicas, escape endosomal, nanomedicina, vacunas de ARNm