Clear Sky Science · es
La terapia combinada dirigida y basada en epigenética mejora la inmunidad antitumoral estabilizando la expresión de MHCI dependiente de GATA6 en el adenocarcinoma ductal pancreático
Por qué esta investigación importa para el cáncer de páncreas
El adenocarcinoma ductal pancreático es uno de los cánceres más letales, en gran parte porque se oculta del sistema inmunitario y resiste la mayoría de los fármacos. Este estudio descubre un estado celular tumoral concreto, impulsado por un gen llamado GATA6, que hace que las células del cáncer de páncreas sean más visibles al ataque inmunitario. Los autores también muestran cómo la combinación de dos tipos de fármacos puede preservar este estado vulnerable y potenciar la capacidad de los linfocitos T citotóxicos para atacar los tumores en modelos experimentales.
Un estado celular tumoral que invita al sistema inmunitario
No todas las células del cáncer de páncreas se comportan igual. Algunas mantienen una identidad más ordenada, de tipo epitelial, mientras que otras cambian hacia un estado más móvil y agresivo, de tipo mesenquimal. El factor de transcripción GATA6 ayuda a mantener la identidad epitelial y se asocia con mejores resultados en los pacientes. En amplias cohortes de pacientes, los tumores con niveles altos de GATA6 contenían más células inmunitarias, incluidos linfocitos T CD8 “asesinos”, que los tumores con poco o nada de GATA6. Mediante imágenes espaciales avanzadas en muestras tumorales humanas, los investigadores encontraron que las células cancerosas positivas para GATA6 se situaban con más frecuencia junto a linfocitos T CD8 y mostraban niveles más altos de una molécula llamada MHCI, que actúa como una bandera que indica a los T qué hay dentro de la célula. Estas observaciones sugirieron que GATA6 marca una población de células tumorales que es intrínsecamente más visible para el sistema inmunitario. 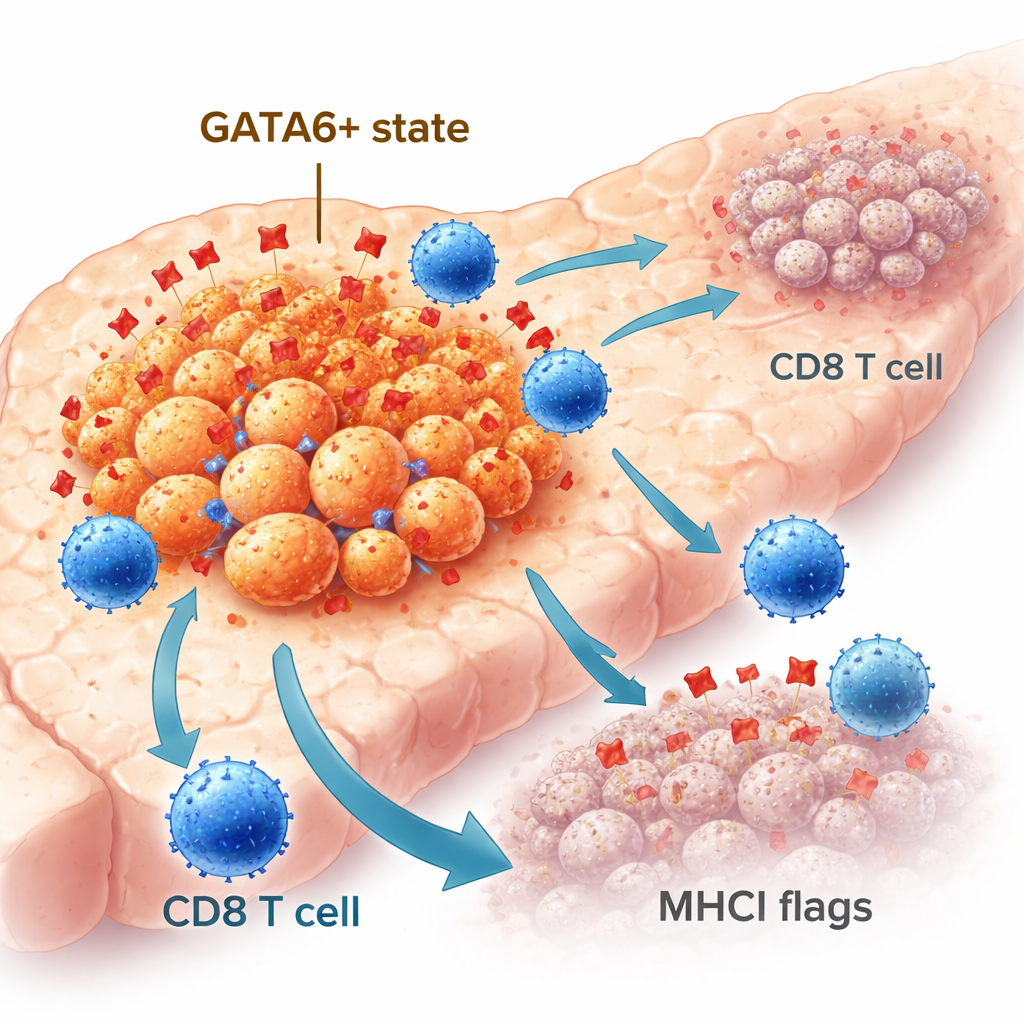
Terapia dirigida que aumenta la visibilidad tumoral —pero con un coste
El equipo preguntó a continuación si los fármacos dirigidos podían incrementar aún más esa visibilidad. Se centraron en los inhibidores de MEK, una clase de fármacos que bloquean una vía de señalización de crecimiento frecuentemente activa en el cáncer de páncreas. En líneas celulares pancreáticas de ratón y en tumores implantados en ratones y en xenoinjertos derivados de pacientes, la inhibición de MEK aumentó MHCI en la superficie de las células tumorales con alto GATA6, haciéndolas potencialmente mejores objetivos para los T. Cuando tumores con alto GATA6 fueron tratados con inhibidores de MEK en ratones, el crecimiento tumoral se ralentizó, MHCI aumentó y más linfocitos T CD8 portadores de moléculas citotóxicas infiltraron los tumores. La inhibición directa de GATA6, ya sea por eliminación genética o por degradación rápida de la proteína, abolió este aumento de MHCI inducido por el inhibidor de MEK y el control tumoral resultante, demostrando que GATA6 es esencial para este efecto beneficioso.
Cómo se adaptan los tumores: desplazándose a un estado más difícil de eliminar
Sin embargo, la historia tuvo un giro. El tratamiento prolongado con inhibidores de MEK hizo que muchas células tumorales pasaran del estado epitelial positivo para GATA6 a un estado más mesenquimal con bajo GATA6, asociado a resistencia al tratamiento. Tanto en modelos de ratón como en xenoinjertos derivados de pacientes, los tumores tratados con inhibidores de MEK mostraron finalmente menos células positivas para GATA6, más marcadores de la transición epitelio-mesenquimal y, en conjunto, un beneficio menos duradero. Aunque células individuales positivas para GATA6 seguían regulando al alza MHCI en respuesta al fármaco, la reducción del tamaño de esta población limitó la mejora global en la presentación de antígenos tumorales, lo que ayuda a explicar por qué los inhibidores de MEK por sí solos han decepcionado en ensayos clínicos de cáncer de páncreas.
Fármacos epigenéticos que mantienen a los tumores en el estado vulnerable
Para contrarrestar esta fuga adaptativa, los investigadores recurrieron a inhibidores de histona desacetilasa, o inhibidores de HDAC, una clase de fármacos epigenéticos conocidos por influir en la identidad celular y la visibilidad inmunitaria. En cultivos celulares y modelos de ratón, la combinación de inhibidores de MEK con inhibidores de HDAC de la clase I, como domatinostat, restauró la expresión de GATA6 que había sido suprimida por la inhibición de MEK, revirtió signos de transición epitelio-mesenquimal y aumentó aún más los niveles de MHCI en las células tumorales. De forma importante, esta terapia combinada condujo a una mayor infiltración y activación de linfocitos T CD8 y a más muerte de células tumorales en tumores ortotópicos de ratón y en un modelo de ratón genéticamente modificado que imita de cerca el cáncer de páncreas humano. La depleción de linfocitos T CD8 eliminó gran parte del beneficio, confirmando que la combinación funciona en gran medida al potenciar a los linfocitos T citotóxicos.
Hacia terapias combinadas más inteligentes para un cáncer difícil
Juntando estos hallazgos, el estudio propone una estrategia en la que la inhibición dirigida de MEK y la inhibición epigenética de HDAC se usan conjuntamente para estabilizar un estado celular tumoral impulsado por GATA6 que es rico en MHCI y, por tanto, altamente reconocible por el sistema inmunitario. Al aumentar tanto el número de células positivas para GATA6 como sus “banderas” de MHCI, la combinación favorece una infiltración más profunda de linfocitos T CD8, una actividad citotóxica más intensa y una supervivencia más prolongada en modelos murinos agresivos de cáncer de páncreas. Aunque los inhibidores de HDAC pueden conllevar efectos secundarios importantes y el trabajo es preclínico, esta investigación apunta hacia enfoques terapéuticos futuros que podrían emparejar fármacos dirigidos a vías y modificadores epigenéticos cuidadosamente escogidos para hacer que los tumores pancreáticos sean más vulnerables a las defensas inmunitarias del propio organismo. 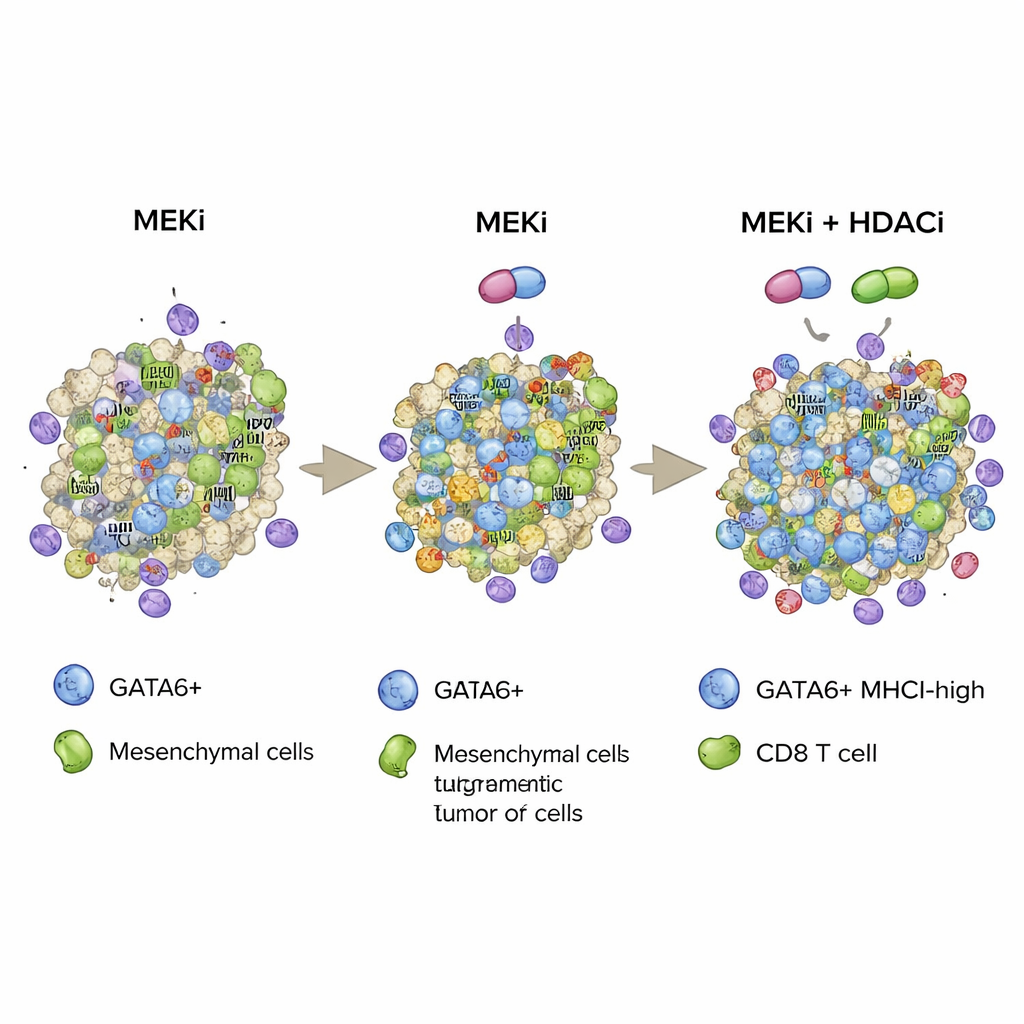
Cita: Peng, J., Yang, J., Antonopoulou, G. et al. Combined targeted and epigenetic-based therapy enhances antitumor immunity by stabilizing GATA6-dependent MHCI expression in pancreatic ductal adenocarcinoma. Nat Commun 17, 1476 (2026). https://doi.org/10.1038/s41467-026-69013-y
Palabras clave: cáncer de páncreas, inmunidad tumoral, GATA6, inhibidor de MEK, inhibidor de HDAC