Clear Sky Science · es
AACRNL evolucionó de factor de virulencia a parásito epigenético impulsor de la expansión genómica en eucariotas de vida libre
Cuando las toxinas antiguas aprenden trucos nuevos
Nuestros genomas no son manuales de instrucciones silenciosos. Son arenas concurridas donde genes, virus y ADN móvil se disputan constantemente espacio y control. Este estudio descubre a un actor sorprendente en esa lucha: una proteína que empezó su vida como una toxina usada por microbios para atacar hospedadores, pero que desde entonces se ha reutilizado dentro de animales de vida libre como una especie de “parásito epigenético” que ayuda a ampliar su propia huella en el genoma.
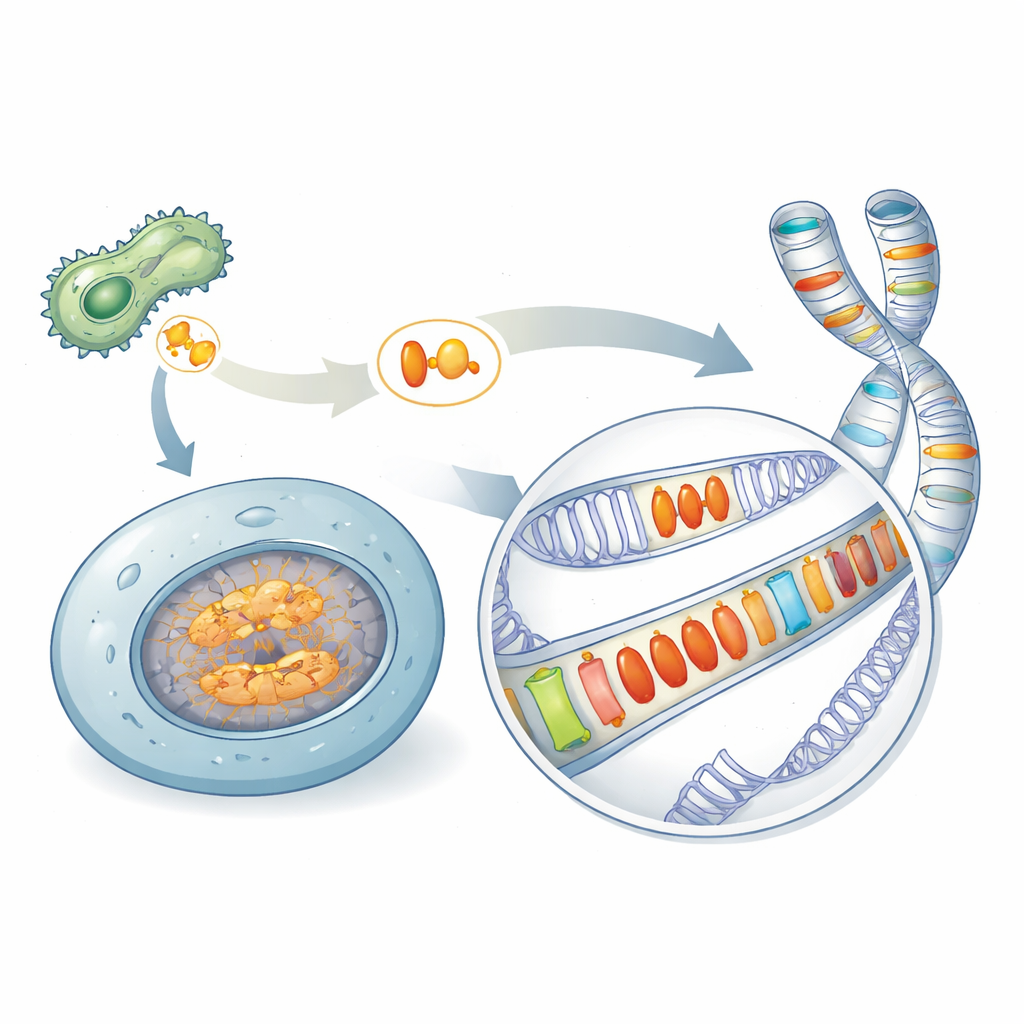
Un legado oculto de armas microbianas
Muchos microbios patógenos dependen de proteínas especiales, llamadas efectores, para sabotear las defensas de los organismos que infectan. Una familia famosa, conocida como Crinklers, se creyó durante mucho tiempo exclusiva de patógenos. Al examinar una amplia variedad de especies, los autores descubrieron proteínas relacionadas —aquí agrupadas bajo el nombre AACRNL— en lugares inesperados, incluidas esponjas, corales, erizos de mar y peces óseos que no son patógenos clásicos. Estas proteínas AACRNL conservan el núcleo tipo toxina capaz de modificar químicamente otras proteínas, pero su porción frontal de “entrega”, que los patógenos usan para invadir células hospedadoras, se ha desintegrado en gran medida. Ese cambio estructural sugiere un desplazamiento de atacar a otros organismos a actuar dentro de las propias células del hospedador.
Un cambio egoísta en el genoma
En los peces óseos, los genes AACRNL aparecen en múltiples copias dispersas por distintos cromosomas. Al comparar tramos de ADN vecinos, los investigadores mostraron que algunas líneas de AACRNL han dejado de copiarse, mientras que otras se han multiplicado con la ayuda de segmentos de ADN saltarín llamados transposones. Estos transposones actúan como transbordadores genómicos: cuando se mueven o se duplican, pueden arrastrar a AACRNL consigo. El resultado es un mosaico de copias repetidas de AACRNL incrustadas entre secuencias de transposones, una señal de que un gen se está propagando por su propio beneficio más que por el del hospedador.
Rompiendo el botón de silencio del genoma
Normalmente, las células mantienen ese ADN móvil bajo control estricto. Una salvaguarda clave es una etiqueta química en las proteínas que empaquetan el ADN, conocida como H3K27me3, que ayuda a mantener apagadas regiones peligrosas o ruidosas. Los autores hallaron que una versión activa de AACRNL en peces, llamada AACRNLβ, puede modificar químicamente a EZH2, la enzima que pone esta marca represiva. Cuando AACRNLβ altera a EZH2, la cantidad de H3K27me3 en su propia dirección genética y en los transposones cercanos disminuye, el ADN local se abre y tanto AACRNLβ como sus vecinos transposones se expresan con mayor fuerza. En efecto, la proteína pulsa su propio botón de “encendido” y levanta los frenos sobre los elementos móviles que pueden transportarla a nuevas posiciones en el genoma.
Eludiendo a los vigilantes inmunitarios
Desatar transposones y actividad genética inusual corre el riesgo de atraer la atención del sistema inmunitario. El estudio muestra que AACRNLβ también aborda este problema. Añade una pequeña marca química a TRAF6, una proteína central que ayuda a activar señales antivirales e inflamatorias. Marcado de esta manera, TRAF6 se vuelve menos estable y es etiquetado con mayor frecuencia para su eliminación por la maquinaria de desecho celular. Con este nodo de señal debilitado, las vías defensivas clave se activan con menos intensidad, creando un entorno más tolerante en el que AACRNLβ y sus transposones asociados pueden persistir y copiarse con menos consecuencias por ser detectados.
Una delicada carrera armamentística dentro de la célula
La historia no termina con AACRNLβ funcionando sin control. La misma proteína TRAF6 que es objetivo de AACRNLβ puede, a su vez, añadir sus propias marcas a AACRNLβ, señalando a la proteína tipo parásito para su destrucción. Este ida y vuelta se parece a una carrera armamentística molecular: AACRNLβ usa química derivada de toxinas para inclinar la cromatina y la inmunidad a su favor, mientras que las proteínas del hospedador contraatacan degradándola y manteniendo su actividad esporádica y arriesgada. Los autores sostienen que este tira y afloja ha permitido que un antiguo arma microbiana sobreviva como un residente egoísta de genomas de vida libre, expandiendo el contenido de ADN y remodelando las reglas del conflicto genético desde dentro.
Por qué esto importa para nuestra visión de los genomas
Para un no especialista, el mensaje clave es que los genomas no son solo planos optimizados para la supervivencia del hospedador. También albergan oportunistas. Este trabajo muestra que incluso las toxinas clásicas pueden ser domesticadas en tales elementos, usando su química destructiva original para sortear cerraduras epigenéticas y alarmas inmunitarias, y para propagarse por el genoma a lo largo del tiempo evolutivo. Comprender este tipo de conflicto oculto ayuda a explicar por qué los genomas son tan grandes, complejos y dinámicos —y sugiere que otras toxinas “retiradas” pueden estar reescribiendo silenciosamente el ADN en muchas especies, quizá incluso en la nuestra.
Cita: Xu, T., Geng, S., Lv, X. et al. AACRNL evolved from virulence factor to epigenetic parasite driving genome expansion in free-living eukaryotes. Nat Commun 17, 2130 (2026). https://doi.org/10.1038/s41467-026-69012-z
Palabras clave: elementos genéticos egoístas, evolución del genoma, regulación epigenética, transposones, inmunidad innata