Clear Sky Science · es
Inmovilización sinérgica multicomponente mediante estrategias de intercambio in situ y dinámico para construir biofarmacéuticos jerárquicos
Por qué importa crear medicamentos más inteligentes
Muchos de los fármacos más potentes de hoy son grandes y frágiles moléculas biológicas, como proteínas y enzimas. Pueden combatir el cáncer, eliminar bacterias nocivas y acelerar la curación, pero se degradan con facilidad y son difíciles de transportar hasta el lugar adecuado del organismo. Este artículo describe una nueva manera de “empaquetar” varios de estos componentes delicados juntos dentro de un material protector similar a una esponja, de modo que puedan actuar en secuencia con mayor eficacia y menos efectos secundarios.
Convertir un cristal en un edificio de apartamentos molecular
Los investigadores parten de un material poroso especial compuesto por iones metálicos y pequeñas unidades orgánicas. Se comporta como un diminuto y flexible edificio de apartamentos lleno de habitaciones y pasillos. Demuestran que este entramado, llamado marco pirimidínico zeolítico, puede crecer alrededor de proteínas de modo que éstas queden protegidas dentro del cristal. Este atrapamiento “in situ” no aplasta ni desactiva las proteínas, y estudios de imagen detallados confirman que están distribuidas de forma homogénea por el interior, como inquilinos que ocupan todas las plantas de un edificio.
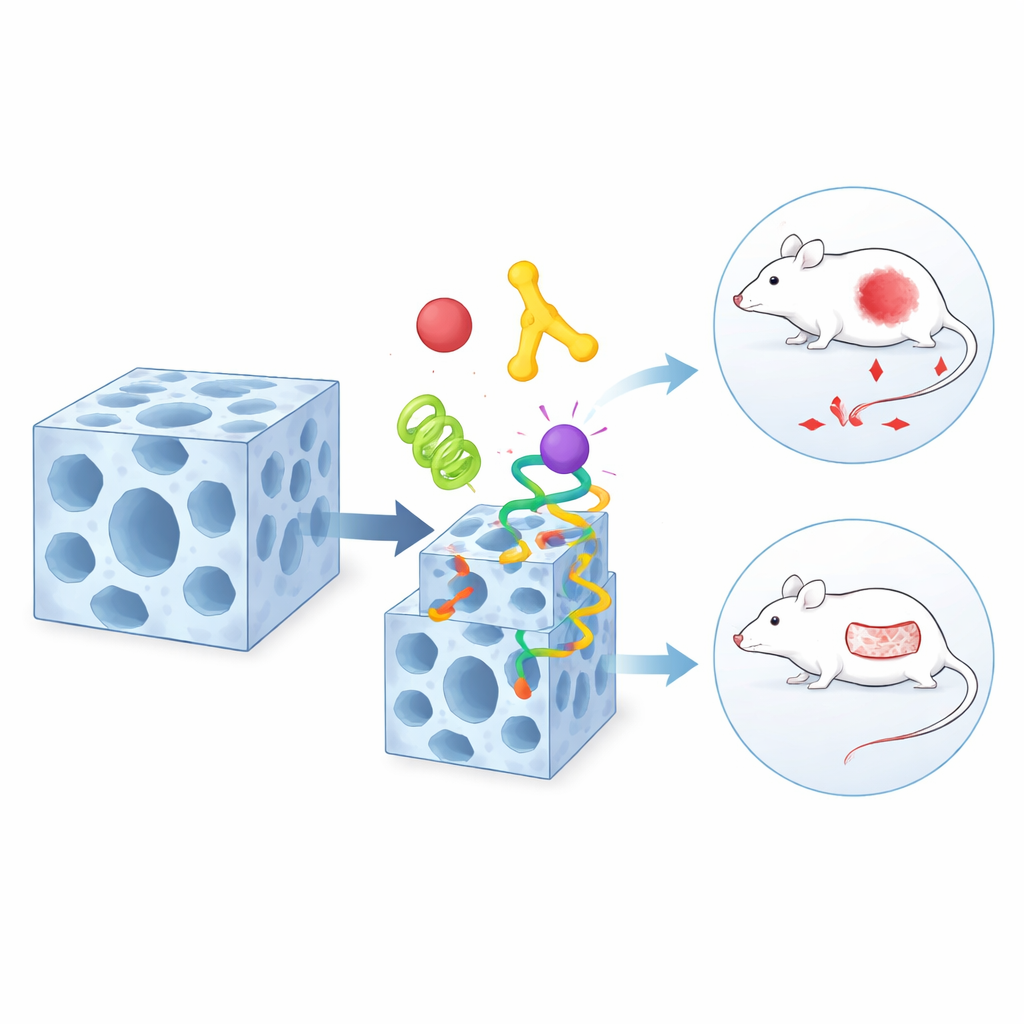
Un huésped que cambia de forma para decorar la superficie
El mismo material tiene un segundo truco sorprendente: puede cambiar reversiblemente su estructura interna cuando se expone a ciertos disolventes o al agua. Durante este suave cambio de forma, algunas conexiones químicas en el entramado se aflojan y luego se reforman. El equipo descubrió que determinados grupos químicos en las superficies de las proteínas —como los presentes en ciertos aminoácidos— pueden aprovechar este momento de debilidad. Compiten temporalmente con los bloques constructores originales del entramado y se insertan en los “defectos” recién formados cerca de la superficie. Como resultado, se ancla una capa de proteínas principalmente en el exterior del cristal, mientras que las internas permanecen en su lugar. Este proceso de intercambio dinámico permite a los científicos decidir qué componentes viven en el interior profundo y cuáles decoran la cubierta externa.
Diseñar líneas de ensamblaje enzimáticas
Con el control tanto del espacio interior como del exterior, los autores construyen pequeñas “líneas de ensamblaje” enzimáticas. En un ejemplo, una enzima que convierte azúcar en un subproducto agresivo queda encerrada dentro del entramado, mientras que una segunda enzima que descompone de forma segura ese subproducto queda fijada cerca de la superficie. Esta disposición interior–exterior hace que la reacción sea más rápida y eficiente que los diseños tradicionales núcleo–capa o mezclas aleatorias de enzimas. Debido a que las enzimas exteriores son más accesibles para las moléculas, y el intermedio perjudicial se elimina con rapidez, el sistema permanece activo durante muchos ciclos y tolera mejor el calor, condiciones adversas y el uso repetido.
Paquetes inteligentes anticáncer y antibacterianos
El verdadero potencial de este enfoque aparece cuando se aplica a la medicina. El equipo combina en una sola partícula estratificada una proteína que dirige hacia tumores, una enzima que consume glucosa y un fármaco de quimioterapia convencional. El componente orientador en la superficie guía la partícula hacia las células cancerosas, la enzima agota su suministro energético consumiendo el azúcar local y la molécula pequeña del fármaco asesta un golpe letal adicional. En ratones con implantes tumorales humanos, este conjunto de tres elementos reduce los tumores con mucha más eficacia que cualquiera de los componentes por separado o que mezclas más sencillas. En otro diseño, los autores adaptan el entramado para heridas cutáneas infectadas colocando un péptido antibacteriano y una enzima remodeladora de tejidos en distintas regiones del mismo portador. En modelos de rata, estas partículas reducen drásticamente la infección y aceleran el cierre de heridas difíciles en comparación con los tratamientos convencionales.

Cómo este trabajo impulsa la medicina
Para un lector no especialista, el mensaje clave es que este estudio convierte un único cristal poroso en un hogar programable para múltiples tipos de moléculas terapéuticas. Al decidir quién vive dentro, quién reside en la superficie y en qué proporción, los investigadores pueden orquestar tratamientos escalonados —primero localizar, luego atacar y después reparar— dentro de un único objeto diminuto. Esta estrategia no solo protege fármacos biológicos frágiles, sino que también les permite cooperar, lo que conduce a terapias anticáncer y antibacterianas más potentes y precisas. Los mismos principios de diseño podrían adaptarse a muchos futuros “medicamentos inteligentes” que requieran que varios componentes trabajen juntos en el lugar y momento adecuados.
Cita: Yang, M., Meng, X., Shi, R. et al. Multicomponent synergistic immobilization via in-situ and dynamic exchange strategies for constructing hierarchical biopharmaceuticals. Nat Commun 17, 2208 (2026). https://doi.org/10.1038/s41467-026-69009-8
Palabras clave: marcos metal-orgánicos, inmovilización de enzimas, nanomedicina contra el cáncer, cicatrización de heridas, entrega de biofármacos