Clear Sky Science · es
Escherichia coli promueve la metástasis del cáncer colorrectal manteniendo bucles enhancers-promotores mediante la liberación de trampas extracelulares de neutrófilos
Microbios intestinales y la autopista secreta del cáncer
El cáncer colorrectal a menudo resulta letal no por el tumor primario en el intestino, sino porque las células cancerosas viajan al hígado y allí se asientan. Este estudio descubre un cómplice inesperado en ese viaje: una bacteria intestinal común, Escherichia coli. Siguiendo la cadena de eventos desde las bacterias en el intestino hasta los tumores agresivos en el hígado, los investigadores revelan cómo microbios, células inmunitarias y la arquitectura del ADN dentro de las células cancerosas pueden actuar juntos para alimentar la metástasis, y sugieren nuevas maneras de romper esa cadena.
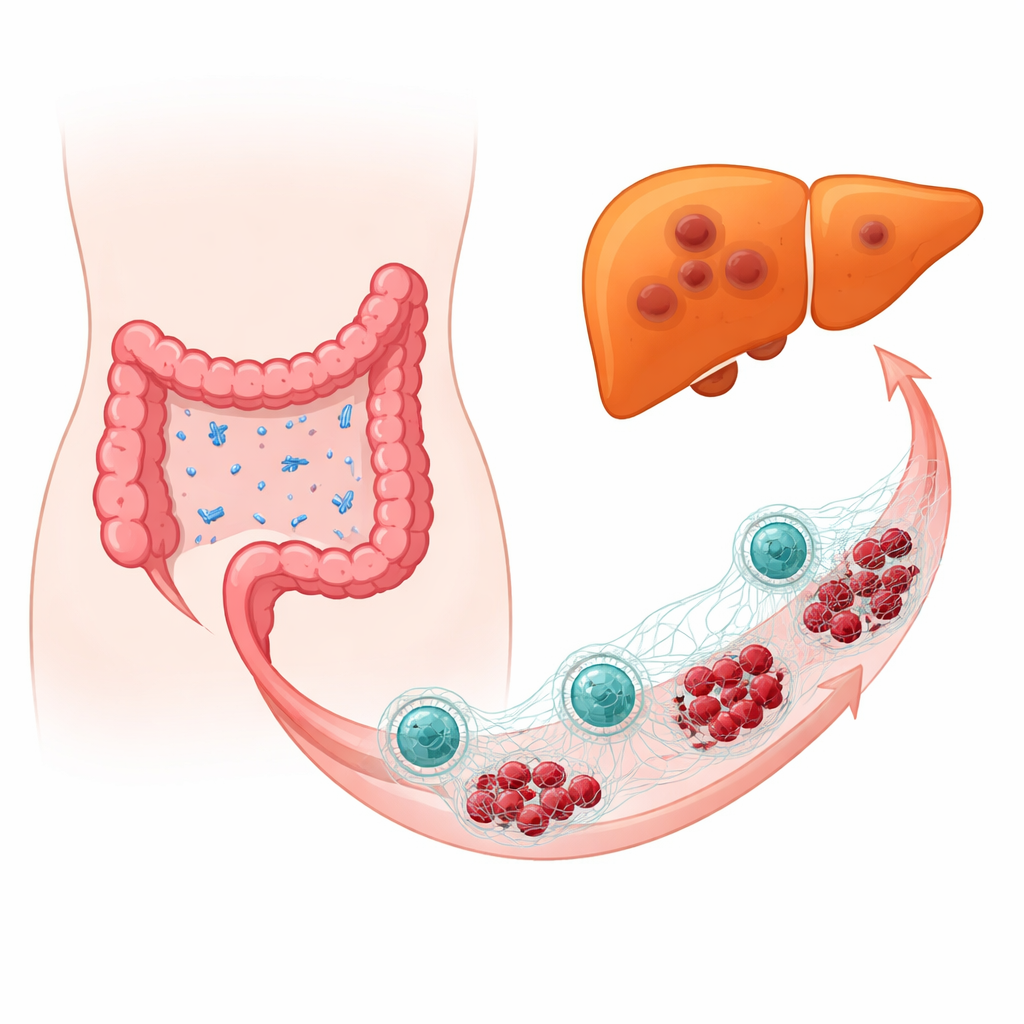
Cuando bacterias amigas se vuelven hostiles
El equipo examinó muestras tumorales de personas con cáncer colorrectal, comparando las de quienes habían desarrollado metástasis hepáticas con las de quienes no. Mediante perfiles microbianos de alta resolución basados en ADN, hallaron que E. coli era mucho más abundante en los tumores que ya habían sembrado el hígado. En modelos murinos y en ratones con sistemas inmunitarios humanizados, la introducción deliberada de E. coli cerca de tumores colorrectales aumentó el tamaño y la frecuencia de las metástasis hepáticas, y empujó a las células tumorales hacia un estado más móvil e invasivo. Incluso cuando la mayor parte de la flora intestinal normal fue eliminada con antibióticos y solo se reintrodujo E. coli, la bacteria siguió potenciando el crecimiento y la diseminación tumoral, lo que implica a E. coli en sí misma más que a una alteración general del microbioma.
Redes inmunitarias que ayudan al escape del cáncer
Los neutrófilos—células inmunitarias de primera línea que normalmente atrapan y matan microbios—surgieron como intermediarios cruciales. En respuesta a E. coli, los neutrófilos liberaron estructuras semejantes a redes llamadas trampas extracelulares, compuestas de ADN y proteínas tóxicas. Estas redes están pensadas para capturar bacterias, pero en este contexto protegieron e hicieron más poderosas a las células cancerosas. Cuando los investigadores degradaron las redes con enzimas o bloquearon enzimas clave necesarias para formarlas, las metástasis hepáticas se redujeron y los tumores se volvieron menos agresivos. Agotar neutrófilos tuvo un efecto protector similar, lo que apunta a una paradoja: la propia respuesta inmunitaria que combate la infección estaba siendo secuestrada para ayudar a la diseminación del cáncer.
De señales eléctricas a interruptores genéticos
¿Cómo podían las redes pegajosas de ADN fuera de una célula tumoral cambiar lo que sucede en lo profundo de su núcleo? La respuesta residía en el calcio, un ion simple que actúa como señal eléctrica en las células. El estudio mostró que las trampas de neutrófilos aumentaban el nivel de una proteína canal, TRPC1, en las células de cáncer colorrectal. TRPC1 dejó entrar calcio extra en la célula, lo que a su vez activó un regulador sensible al calcio llamado NFATC3 y creó un circuito autorreforzante que mantenía altos los niveles de TRPC1. Este aumento de calcio favoreció que dos pequeñas proteínas, S100A8 y S100A9, se unieran entre sí y luego se ligaran a una proteína de control del crecimiento de gran relevancia, STAT3. El trío se desplazó al núcleo, donde hizo algo especialmente llamativo: ayudó a doblar y formar bucles en el ADN para que regiones reguladoras distantes y sitios de inicio de genes se encontraran, estabilizando físicamente los “bucles enhancer–promotor” que aumentan la expresión de ciertos genes.
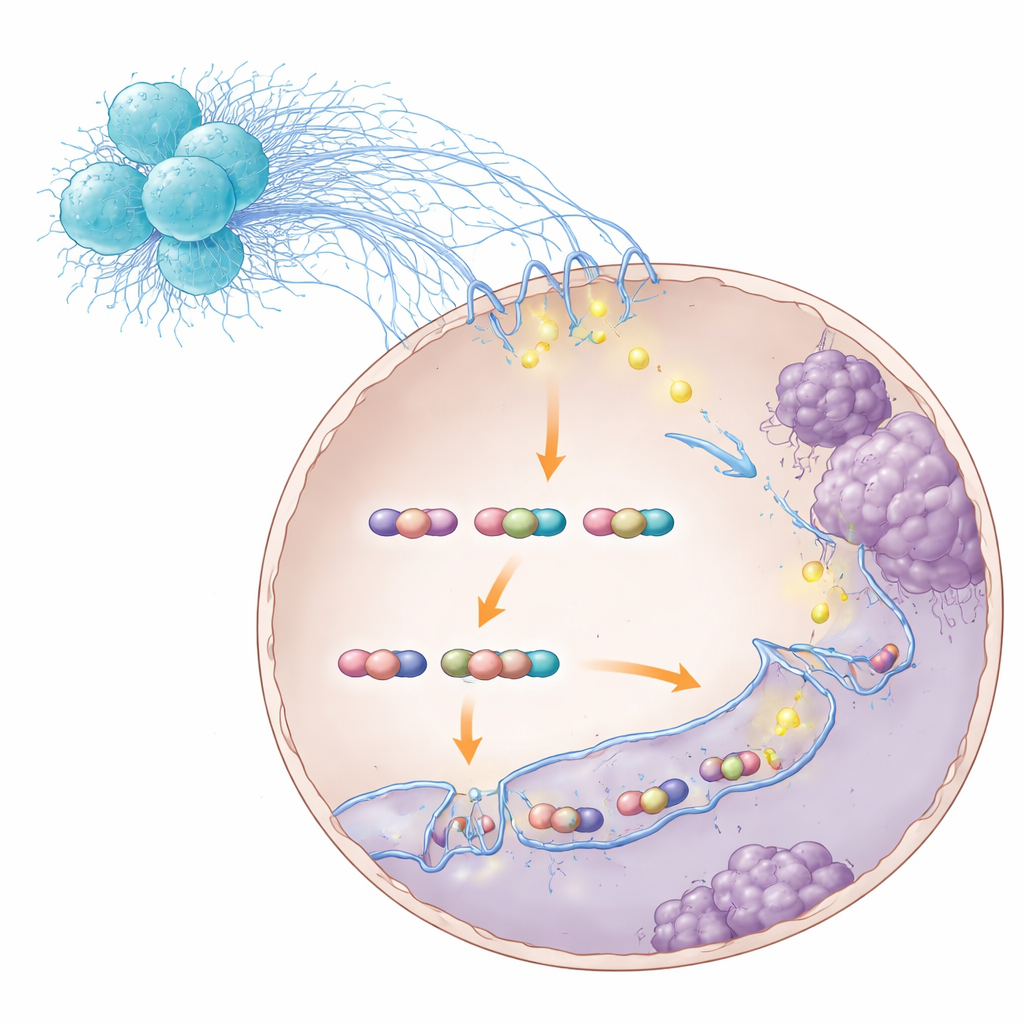
Reconfigurar las células cancerosas para la metástasis
Al cartografiar los contactos tridimensionales a lo largo del genoma, los investigadores encontraron que el complejo STAT3–S100A8/9 promovía bucles que favorecían genes implicados en el movimiento celular y la invasión. Un gen destacado fue TNS1, que impulsa a las células a aflojar sus adhesiones y migrar con mayor facilidad. Cuando se interrumpió el complejo STAT3–S100A8/9, muchos de esos bucles se debilitaban o desaparecían, los niveles de TNS1 bajaron y las células cancerosas perdieron parte de su capacidad para invadir y colonizar el hígado. Es importante señalar que esta interrupción no evitó que STAT3 contactara el ADN por completo; desestabilizó específicamente la arquitectura de bucles que sobrecargaba los programas metastásicos. En modelos animales, bloquear distintos pasos de esta cadena—desde la molécula de señal bacteriana RIPK2 en neutrófilos, hasta S100A8/9 y STAT3 mismo—redujo la metástasis hepática y mejoró la supervivencia.
Romper la cadena entre microbios y tumores
Para el público general, el mensaje clave es que una bacteria intestinal común puede ayudar a que el cáncer colorrectal se disemine al provocar primero que las células inmunitarias lancen redes de ADN y luego usar esas redes para impulsar un relevo potenciado por calcio que reconfigura cómo se activan los genes cancerosos. En lugar de depender de antibióticos de amplio espectro, que pueden dañar microbios beneficiosos y atenuar la inmunoterapia contra el cáncer, el trabajo apunta a dianas farmacológicas más precisas: sensores bacterianos como RIPK2, la cascada TRPC1–calcio–S100A8/9 y los bucles de ADN dirigidos por STAT3 que fijan en estado alto los genes relacionados con la metástasis. Interrumpir esta cadena en uno o varios puntos podría ofrecer una nueva estrategia para evitar que el cáncer colorrectal deje de ser un problema local en el intestino y se convierta en una enfermedad mortal en el hígado.
Cita: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
Palabras clave: metástasis de cáncer colorrectal, microbioma intestinal, trampas extracelulares de neutrófilos, señalización STAT3, regulación epigenética de genes