Clear Sky Science · es
El diseño de inhibidores covalentes confiere actividad frente a las formas de KRAS G12C unidas a GDP y a GTP
Por qué esto importa para los tratamientos oncológicos futuros
Los cánceres impulsados por mutaciones en un gen llamado KRAS se han considerado durante mucho tiempo de los más difíciles de tratar. Recientemente, nuevos fármacos que apagan una forma mutante común, KRAS G12C, han llegado a los pacientes y han empezado a cambiar ese panorama. Este artículo explora una idea aún más ambiciosa: ¿podemos diseñar fármacos que bloqueen KRAS G12C en sus dos principales modos de acción dentro de la célula, y ello haría que el tratamiento del cáncer fuera más rápido, más eficaz o más duradero?
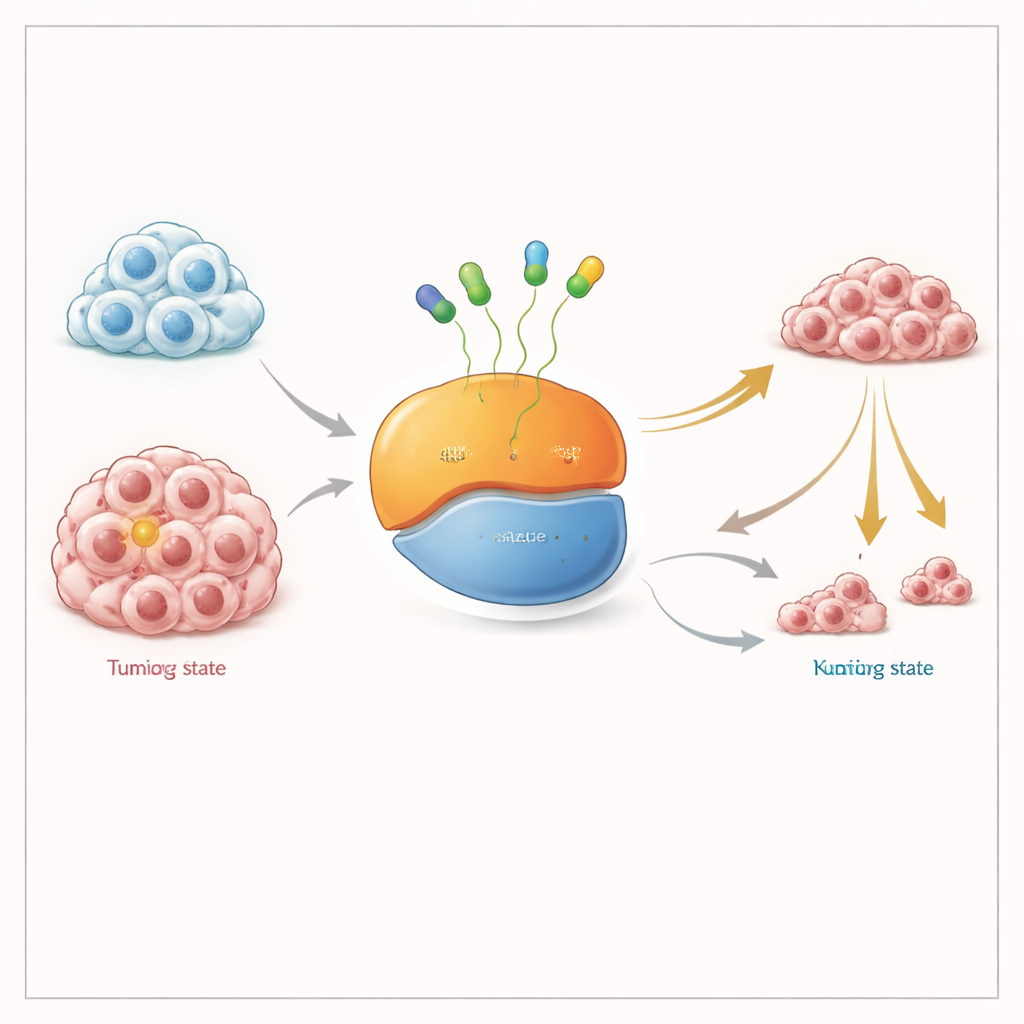
Apagar un interruptor molecular en dos posiciones
KRAS actúa como un pequeño interruptor de encendido y apagado de las señales de crecimiento celular. Cambia entre un estado “apagado”, en el que lleva una molécula transportadora de energía (GDP), y un estado “encendido”, en el que lleva otra (GTP). La mutación KRAS G12C deja este interruptor parcialmente activado y alimenta el crecimiento tumoral. Los medicamentos existentes aprobados por la FDA se enganchan a la forma “apagada” y la bloquean; con el tiempo, a medida que más KRAS pasa por esa forma, el conjunto total de proteína mutante queda desactivado. Muchos científicos han argumentado que un fármaco capaz de capturar KRAS en sus formas activada y desactivada debería funcionar mejor, especialmente en tumores que se adaptan manteniendo más KRAS en el estado activo.
Diseñando un nuevo tipo de anzuelo molecular
Los autores se propusieron construir fármacos de doble propósito. Se centraron en una pequeña hendidura cerca de una región flexible de KRAS llamada Switch II, donde ya se unen los fármacos actuales. En lugar de cambiar la afinidad con que sus moléculas encajaban en esa hendidura, reingenierizaron la porción “warhead” que forma un enlace químico permanente con la cisteína mutante en la posición 12. Mediante modelado por ordenador y la síntesis de docenas de variantes, descubrieron un warhead especial de tres partes que se aproxima a la cisteína desde un ángulo ligeramente distinto. Este desplazamiento sutil crea suficiente espacio para la molécula de GTP más voluminosa, permitiendo que los nuevos compuestos se unan a KRAS tanto si porta GDP como GTP. Pruebas bioquímicas confirmaron que los compuestos líderes podían interferir con la asociación de KRAS con un socio clave de señalización, RAF, en ambos estados.
Ver cómo la proteína se remodela
Para entender por qué funcionaban estas moléculas, el equipo determinó estructuras cristalinas de alta resolución del fármaco unido a KRAS. Estas instantáneas mostraron que el nuevo warhead reacciona en un sitio inusual del andamiaje químico, rompiendo un átomo de flúor y formando un enlace covalente en un carbono distinto al de los fármacos contra el cáncer que normalmente atacan cisteínas. Esta química alterada ayuda al fármaco a encajar en el bolsillo de Switch II incluso cuando GTP está presente. Las estructuras también revelaron que, cuando el inhibidor se une, desplaza una pequeña molécula de agua y reorganiza sutilmente otro bucle, Switch I, que normalmente contacta proteínas de señalización aguas abajo. Esta remodelación alostérica acerca dos aminoácidos para formar un puente salino estrecho, distorsionando la superficie de modo que RAF ya no puede acoplarse y transmitir las señales de crecimiento.
Apagado rápido, pero sin efecto a más largo plazo
Armados con estos conocimientos estructurales, los investigadores refinaron dos moléculas líderes que se enganchan de forma eficiente y selectiva a KRAS G12C, al tiempo que respetan en gran medida otras proteínas con cisteínas. En líneas celulares tumorales, estos inhibidores de doble estado bloquearon rápidamente un relevo de señalización clave conocido como la vía MAPK, medido por la pérdida de una marca química en la proteína ERK y por una fuerte supresión del crecimiento celular. Inactivaron KRAS en las células más rápido que un fármaco de referencia que solo apunta al estado inactivo. En modelos de tumores en ratón, un compuesto líder mostró buena disponibilidad oral, formó rápidamente enlaces covalentes con el objetivo y redujo tumores o ralentizó su crecimiento. Sin embargo, cuando el equipo comparó los fármacos de doble estado y los dirigidos al estado inactivo durante periodos más largos, ambas clases alcanzaron finalmente niveles similares de inactivación de KRAS, inhibición de la vía y control tumoral.
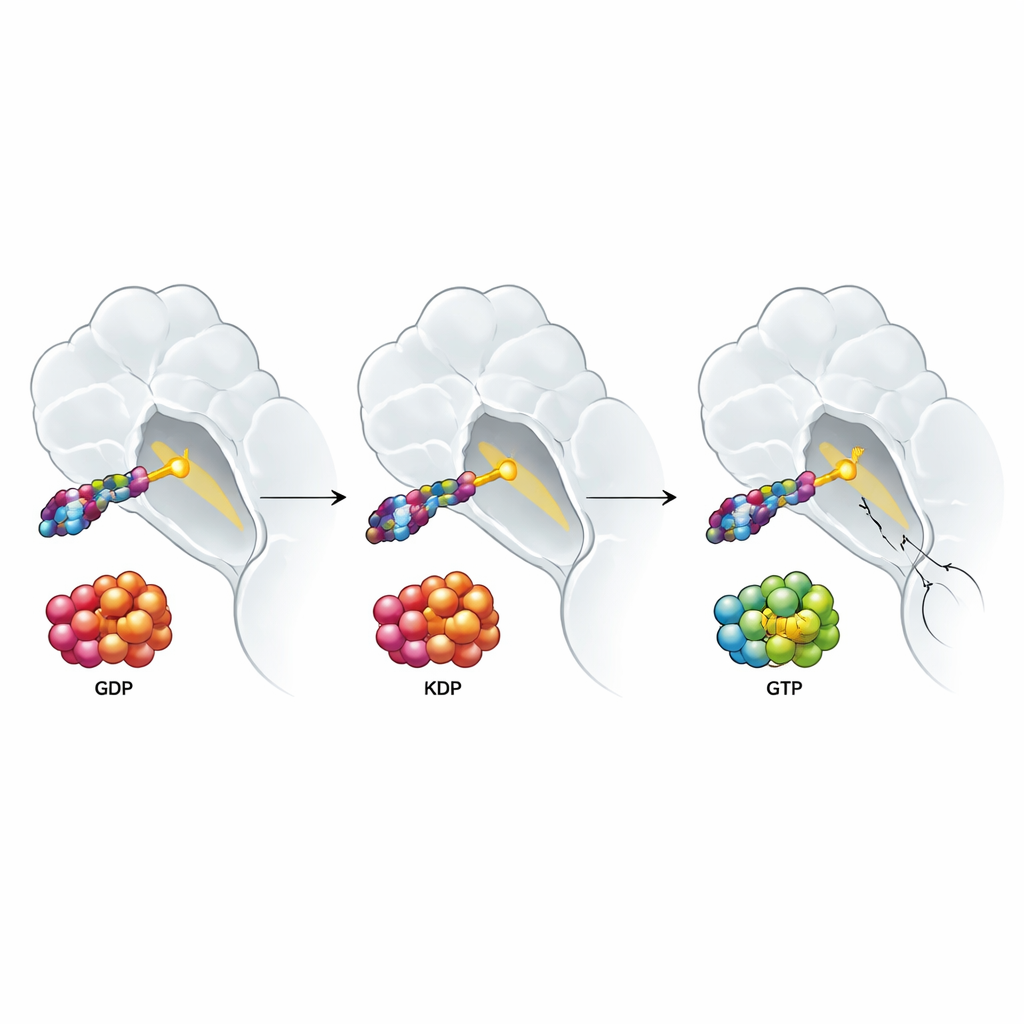
Por qué las señales de crecimiento del entorno tumoral siguen ganando
El estudio también investigó cómo las señales del entorno tumoral afectan a estos fármacos. Factores de crecimiento como EGF y HGF, que son abundantes alrededor de muchos tumores, empujan a las proteínas RAS hacia la forma activa cargada de GTP y son conocidos por atenuar las respuestas a terapias dirigidas. Podría esperarse que un fármaco que se une a la forma activa de KRAS G12C eludiera este problema. En cambio, los autores observaron que tanto los inhibidores de doble estado como los del estado inactivo perdieron potencia cuando estaban presentes dichos factores de crecimiento. Experimentos detallados apuntaron a un culpable sorprendente: la activación de las formas normales, no mutadas, de RAS (H‑RAS y N‑RAS), que pueden sortear KRAS G12C y mantener el flujo de señales de crecimiento. Cuando los investigadores eliminaron H‑RAS y N‑RAS en una línea celular de cáncer de pulmón, la resistencia impulsada por factores de crecimiento desapareció en gran medida para todo tipo de fármacos dirigidos a KRAS G12C, mientras que un fármaco que bloquea un paso aguas abajo de la vía se vio menos afectado desde el principio.
Qué significa esto para pacientes y desarrollo de fármacos
En conjunto, el trabajo demuestra que es químicamente y estructuralmente factible construir fármacos covalentes contra KRAS G12C que capturan la proteína tanto en sus estados activo como inactivo, y que estos inhibidores de doble estado pueden apagar la señalización más rápido que los medicamentos existentes. Sin embargo, el compromiso rápido no se tradujo en un control tumoral claramente superior ni en una solución a la resistencia impulsada por factores de crecimiento en modelos preclínicos. Para los pacientes, esto sugiere que simplemente añadir actividad contra la forma activa de KRAS puede no ser suficiente; pueden ser necesarias estrategias combinadas que también aborden a otros miembros de la familia RAS o nodos de señalización aguas abajo. El nuevo warhead y el plano estructural presentados aquí, no obstante, amplían la caja de herramientas para apuntar a KRAS e informatizarán las futuras generaciones de terapias oncológicas de precisión.
Cita: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
Palabras clave: KRAS G12C, inhibidor covalente, inhibición de doble estado, señalización MAPK, resistencia a fármacos