Clear Sky Science · es
Un circuito basalo-prefrontal-tálamo definido molecularmente regula las dimensiones sensorial y afectiva del dolor en ratones macho
Por qué importa este circuito cerebral para el dolor
El dolor es más que una punzada aguda o un dolor sordo; también conlleva una carga emocional y puede modificar nuestro estado de ánimo y comportamiento durante años. Muchos pacientes con dolor crónico obtienen poco alivio con los fármacos actuales y a menudo sufren efectos secundarios graves. Este estudio en ratones macho descubre un circuito cerebral definido con precisión que ayuda al cerebro a modular el dolor, tanto en cuanto a su intensidad como a su componente desagradable. Al mapear y controlar esta vía, el trabajo apunta a nuevas formas más selectivas de aliviar el dolor crónico sin depender únicamente de los analgésicos tradicionales.
Una ruta oculta desde el cerebro pensante hasta el centro del dolor
Los investigadores se centraron en la corteza prefrontal medial, una región frontal implicada en la toma de decisiones, la emoción y el control del dolor, y en el tálamo, un centro profundo de relevo que moldea tanto la intensidad como lo desagradable del dolor. Descubrieron que un grupo específico de células en la corteza prefrontal medial, marcado por un gen llamado Foxp2, constituye una vía de salida importante hacia el tálamo. Estas células se sitúan principalmente en la capa cortical más profunda y envían fibras largas a núcleos tálamicos particulares, mientras que en gran medida ignoran otros objetivos típicos de la corteza prefrontal. Mediante métodos de trazado y cartografía cerebral completa, el equipo mostró que estas neuronas marcadas por Foxp2 se conectan fuertemente con tres regiones talámicas conocidas por influir en el procesamiento del dolor: el núcleo parataenial, el tálamo mediodorsal y el tálamo ventromedial. 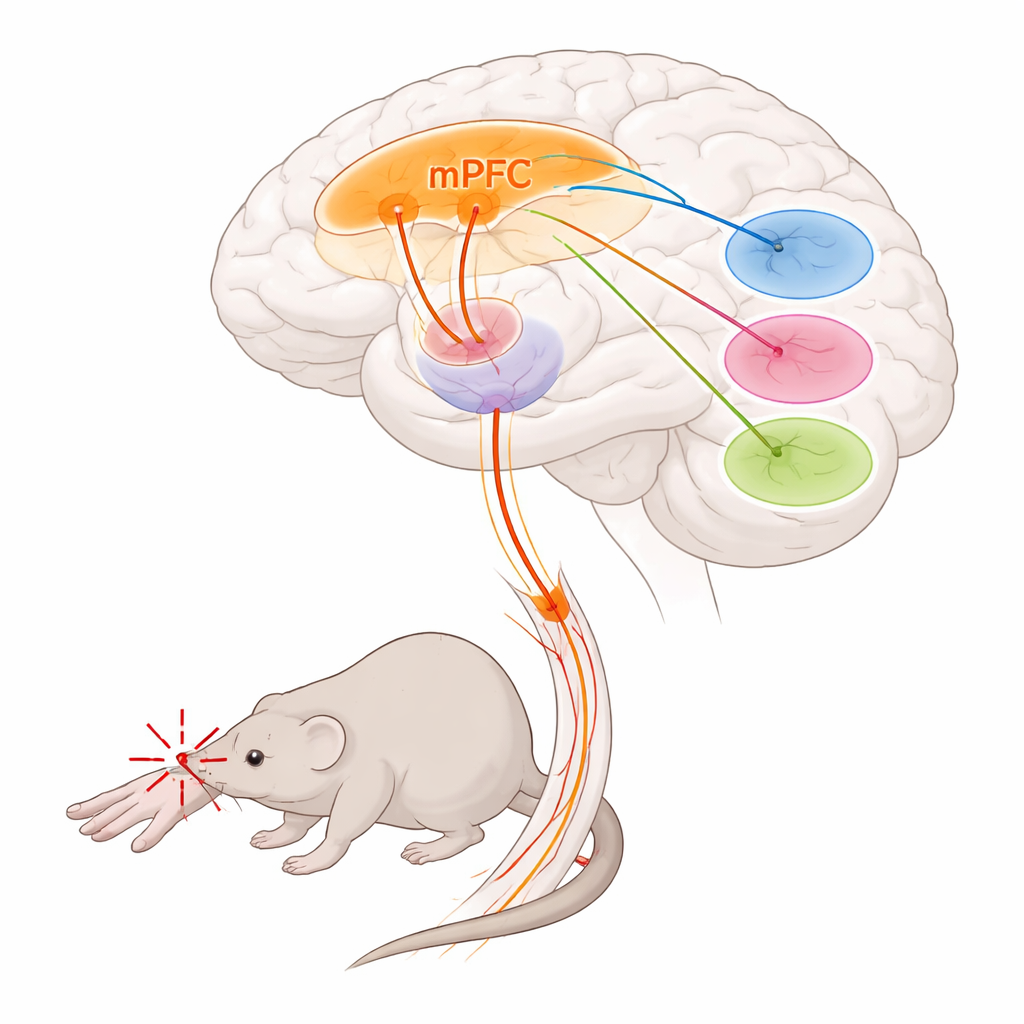
Cuando llega el dolor, un centro clave de control se silencia
Para ver cómo se comporta esta vía durante el dolor, los científicos implantaron pequeñas lentes sobre la corteza prefrontal medial y registraron la actividad de neuronas individuales marcadas por Foxp2 en ratones despiertos. Durante pinzamientos mecánicos breves, dolor químico inducido por formalina y dolor inflamatorio prolongado, estas células se apagaron de forma consistente: la mayoría mostraron menos ráfagas de actividad durante los episodios dolorosos y en los días posteriores a la lesión inflamatoria. Este apagado no fue sutil; en algunas condiciones más de un tercio hasta casi la mitad de las células se volvieron marcadamente menos activas. El hallazgo sugiere que los estados de dolor agudo y crónico pueden reflejar, en parte, el silenciamiento de un sistema prefrontal natural de frenado que de otro modo ayudaría a mantener el dolor bajo control.
Encender y apagar el circuito remodela el dolor
El equipo preguntó entonces si este silenciamiento era solo un efecto secundario del dolor o un motor del mismo. Usando herramientas genéticas, bloquearon de forma persistente la salida de las neuronas marcadas por Foxp2 o aumentaron brevemente su actividad. La inactivación persistente hizo que los ratones fueran más sensibles al tacto y al calor, lo que indica que esta vía normalmente restringe las señales de dolor entrantes. En contraste, la activación a corto plazo elevó el umbral para los estímulos dolorosos, redujo el lamido en la fase tardía en la prueba de formalina (una medida del dolor inflamatorio sostenido) y provocó que los ratones prefirieran entornos donde el circuito había sido activado, señalando alivio de la carga emocional del dolor. Al iluminar ramas específicas de la vía, los investigadores mostraron que las proyecciones al tálamo parataenial reducen tanto la sensibilidad física como las respuestas de afrontamiento, mientras que las proyecciones al tálamo mediodorsal y ventromedial afinan principalmente las dimensiones emocionales y conductuales. En conjunto, estos resultados revelan un esquema de cableado finamente dividido en el que diferentes ramas de la misma población prefrontal controlan distintas facetas de la experiencia del dolor.
Afinación química: un impulso colinérgico para aliviar el dolor
¿Qué controla a estas neuronas prefrontales que alivian el dolor? Experimentos de trazado descubrieron una fuerte entrada desde una región colinérgica en el prosencéfalo basal llamada banda diagonal horizontal. Muchas de las células que envían señales desde esta zona hacia las neuronas marcadas por Foxp2 usan acetilcolina, un mensajero implicado en la atención y la vigilia. Activar esta proyección colinérgica redujo la sensibilidad mecánica y las conductas de afrontamiento y alivió la hipersensibilidad inflamatoria, aunque no cambió de forma clara el tono emocional negativo del dolor. En el lado receptor, se encontró que las neuronas marcadas por Foxp2 estaban enriquecidas en un tipo particular de receptor de acetilcolina, conocido como receptor nicotínico α4β2. Administrar directamente un agonista selectivo α4β2 en la corteza prefrontal medial hizo que los ratones fuesen menos sensibles al calor y al tacto dolorosos, incluso en estados inflamatorios crónicos, y aumentó la actividad en las neuronas marcadas por Foxp2. Bloquear estas neuronas eliminó el beneficio del fármaco, demostrando que este receptor alivia el dolor específicamente al excitar este tipo celular. 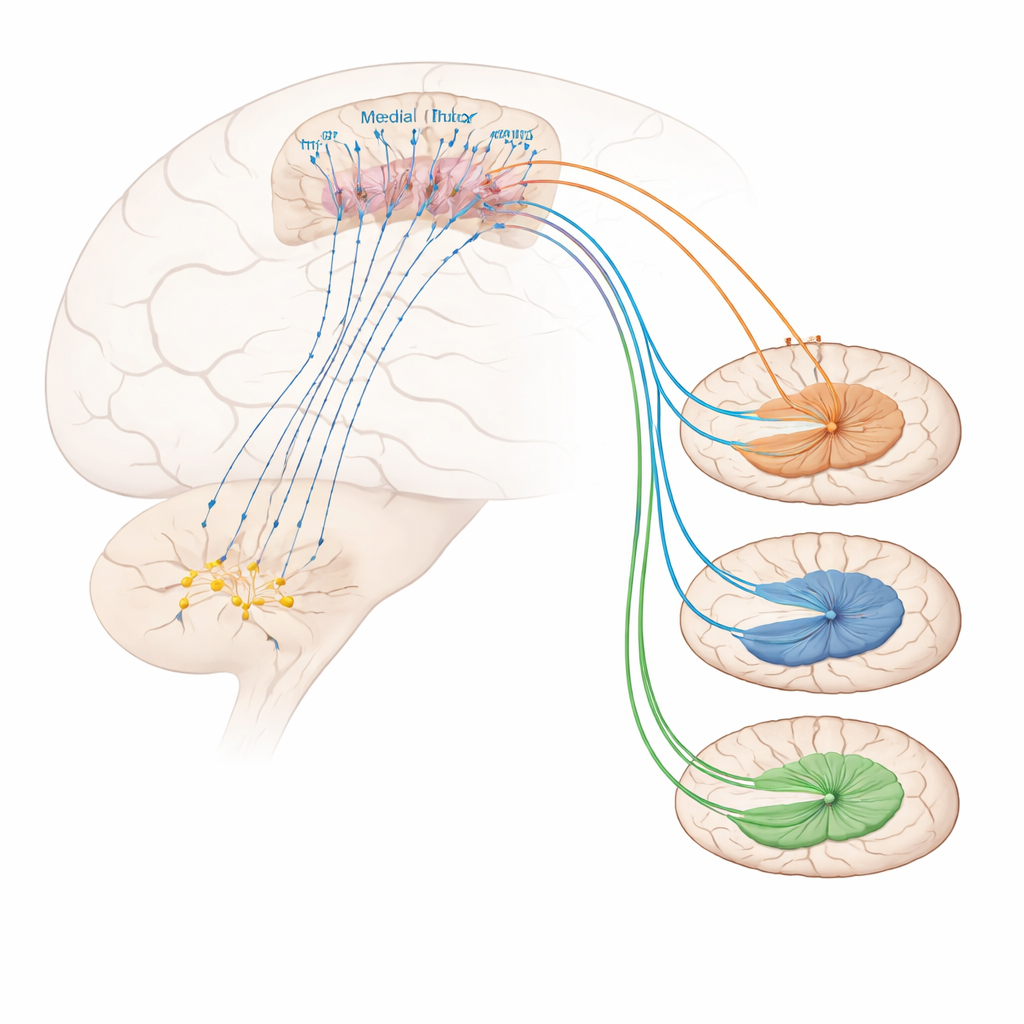
Qué significa esto para el tratamiento futuro del dolor
En términos prácticos, el estudio identifica una vía precisa de tres pasos: una región colinérgica «iniciadora» en el prosencéfalo basal, un conjunto especializado de células de control en la corteza prefrontal medial y centros de relevo distintos en el tálamo que gobiernan por separado cuán intenso se percibe el dolor, cuán desagradable se siente emocionalmente y cómo reaccionamos ante él. El dolor parece apagar este circuito; reactivarlo, ya sea mediante estimulación directa o mediante la diana de sus receptores de acetilcolina, reduce tanto la punzada como la angustia del dolor inflamatorio en ratones macho. Aunque queda mucho trabajo para traducir estos hallazgos a humanos y a otras formas de dolor crónico, los resultados subrayan una estrategia prometedora: en vez de insensibilizar toda la sensación, los tratamientos futuros podrían restaurar o afinar los propios circuitos antídoto del cerebro para una terapia a largo plazo más eficaz y posiblemente más segura.
Cita: Xie, G., Liu, Y., Qi, X. et al. A molecularly defined basalo-prefrontal-thalamic circuit regulates sensory and affective dimensions of pain in male mice. Nat Commun 17, 2134 (2026). https://doi.org/10.1038/s41467-026-69001-2
Palabras clave: dolor crónico, corteza prefrontal medial, tálamo, señalización colinérgica, receptores nicotínicos