Clear Sky Science · es
La microbiota induce EI24 que mejora la homeostasis pero dificulta la función de los macrófagos alveolares mediante la regulación metabólica
Por qué importan los pequeños guardianes del pulmón
Cada respiración no solo aporta oxígeno a los pulmones, sino también polvo, microbios y otros intrusos. Patrullando esta frontera están los macrófagos alveolares: células inmunitarias especializadas que engullen desechos y ayudan a defender frente a infecciones y cáncer. Este estudio revela una forma sorprendente en que nuestros microbios cotidianos «adiestran» a estas células: una molécula llamada EI24, activada por la microbiota, mantiene a los centinelas pulmonares estables y tranquilos, pero a costa de reducir su capacidad para combatir virus y tumores. Comprender este intercambio podría abrir nuevas vías para inmunoterapias más seguras y eficaces.
Conoce a los limpiadores residentes del pulmón
Los macrófagos alveolares se sitúan en los diminutos sacos de aire del pulmón, donde tiene lugar el intercambio gaseoso. Permanecen allí durante años, renovándose y eliminando silenciosamente surfactante, células muertas y partículas sueltas, evitando una inflamación innecesaria que dañaría el delicado tejido. Los autores se centraron en una proteína llamada EI24, previamente asociada a respuestas al estrés celular y al reciclaje celular, pero poco entendida en la inmunidad pulmonar. Descubrieron que, entre muchos tipos de macrófagos tisulares del cuerpo, los macrófagos alveolares expresan niveles particularmente altos de EI24, lo que sugiere que esta proteína podría ser crucial para la vida en la superficie expuesta del pulmón.
Estabilidad frente a fuerza en los defensores pulmonares
Para ver qué hace realmente EI24, los investigadores criaron ratones que carecían de esta proteína específicamente en los macrófagos. Estos animales se desarrollaron con normalidad y produjeron un número normal de precursores jóvenes de macrófagos en el pulmón, pero a medida que maduraban, aproximadamente la mitad de sus macrófagos alveolares desapareció. Las células sobrevivientes mostraron signos claros de un aumento de muerte celular impulsado por una enzima clásica de la apoptosis, la caspasa-3. Sin embargo, las pocas células restantes no eran débiles: exhibían un perfil más «de servicio», con mayor captación de bacterias en pruebas de laboratorio y una producción más intensa de moléculas inflamatorias al ser estimuladas. Los análisis genéticos y de cromatina mostraron que cientos de genes implicados en la presentación de antígenos, la eliminación celular y las respuestas inflamatorias estaban aumentados, mientras que las vías reguladoras que normalmente frenan la activación se aflojaron.
Metabolismo acelerado con un coste escondido
Profundizando más, el equipo halló que los macrófagos deficientes en EI24 habían reconfigurado su metabolismo. En lugar de apoyarse principalmente en un estado tranquilo y eficiente en energía, mostraron niveles más altos tanto de quema de azúcares (glicólisis) como de producción energética mitocondrial. Estas vías energéticas potenciadas ayudaron a alimentar respuestas inflamatorias más fuertes y una ingestión más vigorosa de microbios y células tumorales. Pero este sobreimpulso metabólico también aumentó los subproductos reactivos de oxígeno dentro de las mitocondrias, lo que a su vez activó la caspasa-3 y empujó a las células hacia la muerte programada. Bloquear estas vías metabólicas o neutralizar las moléculas reactivas redujo tanto la inflamación excesiva como la propensión a morir, enlazando el uso de energía de la célula, su capacidad letal y su longevidad.
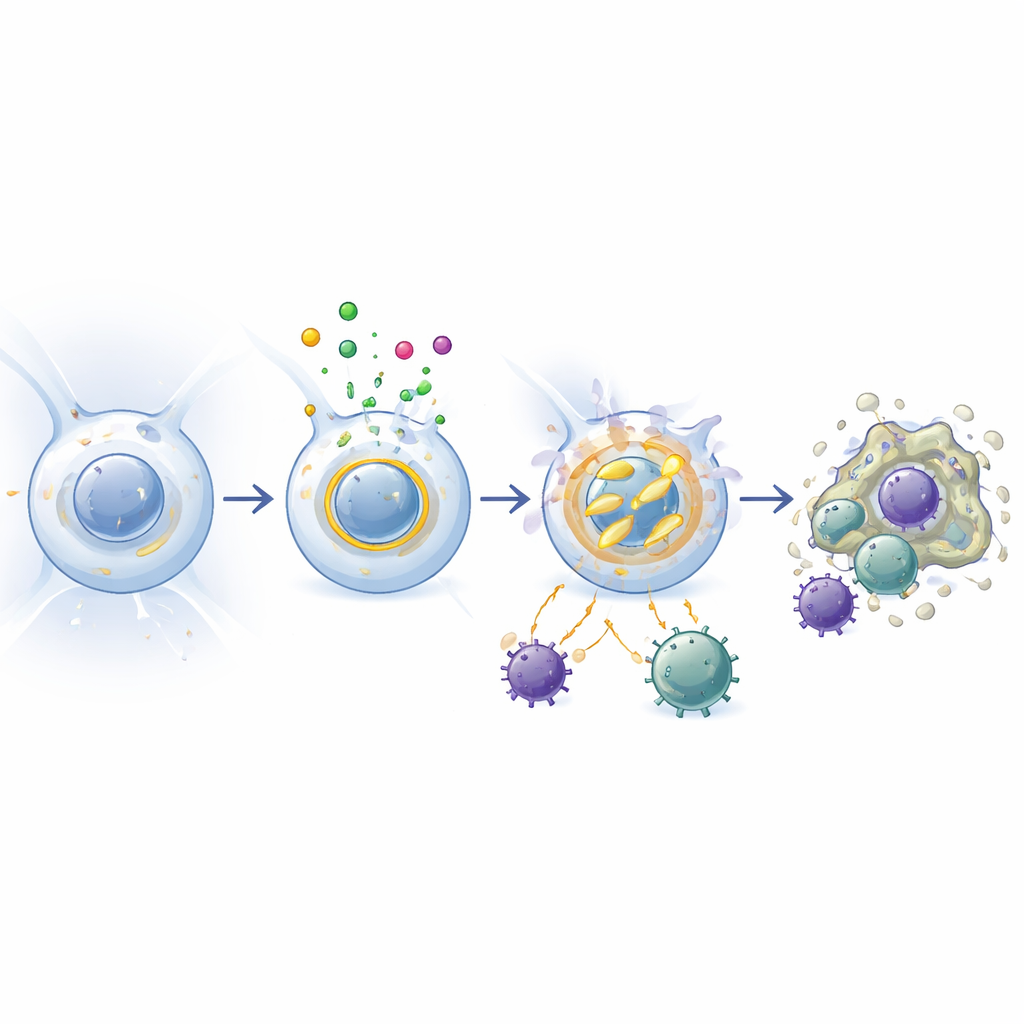
Cómo los microbios amigables regulan el comportamiento
El pulmón no es una cámara sellada; encuentra constantemente microbios inofensivos y beneficiosos procedentes del aire y del intestino. Los investigadores compararon ratones normales con animales criados en condiciones libres de gérmenes. En los ratones libres de gérmenes, los macrófagos alveolares producían mucho menos EI24, y la eliminación de EI24 tuvo poco impacto en su número o comportamiento. Cuando estos ratones fueron expuestos posteriormente a microbios normales, sus macrófagos pulmonares aumentaron la producción de EI24. Experimentos con vías sensoras microbianas mostraron que señales detectadas por los receptores tipo Toll 2 y 4 —«timbres» moleculares para componentes bacterianos— eran responsables de este incremento. En efecto, la microbiota empuja a los macrófagos alveolares hacia un estado más estable y menos reactivo al elevar EI24, ayudando a mantener la calma en un entorno que de otro modo dispararía alarmas inmunitarias constantes.
Reducir EI24 para potenciar la terapia
A pesar de tener menos macrófagos, los ratones que carecían de EI24 en estas células estuvieron mejor protegidos contra una infección grave por influenza y contra metástasis pulmonares experimentales de melanoma. Eliminaban el virus con mayor eficiencia, producían más interferones antivirales en los espacios aéreos y sus macrófagos engullían con más facilidad las células tumorales. Es importante que estos animales no desarrollaron daño pulmonar crónico ni pérdida de función respiratoria, lo que sugiere que eliminar selectivamente EI24 puede mejorar la defensa sin perjuicios evidentes a corto y medio plazo. El equipo también mostró que macrófagos derivados de médula ósea diseñados para carecer de EI24 eran más eficaces cuando se transfirieron a otros ratones, superando a los macrófagos normales en limitar tanto la infección viral como la diseminación tumoral en los pulmones.
Qué significa esto para tratamientos futuros
Para el lector general, el mensaje central es que nuestros microbios residentes ayudan a mantener vivas y relajadas a las células inmunitarias pulmonares activando EI24, pero este mismo mecanismo de seguridad puede atenuar la capacidad de las células para combatir infecciones y cáncer. Al rebajar con cuidado EI24, los científicos pueden empujar a los macrófagos hacia un estado más enérgico y agresivo que elimina mejor virus y células tumorales, al tiempo que preserva la salud pulmonar general en animales experimentales. Este trabajo sugiere que apuntar a EI24, o a los circuitos metabólicos que controla, podría algún día convertir a las terapias basadas en macrófagos en aliados más potentes contra las infecciones respiratorias y el cáncer metastásico.
Cita: Huang, Y., Su, M., Zhang, Y. et al. Microbiota-induced EI24 improves homeostasis but impedes function of alveolar macrophages via metabolic regulation. Nat Commun 17, 2227 (2026). https://doi.org/10.1038/s41467-026-69000-3
Palabras clave: macrófagos alveolares, inmunidad pulmonar, microbiota, metabolismo de macrófagos, defensa frente a cáncer y virus