Clear Sky Science · es
Modificación covalente de un ácido glutámico inspirada en la tecnología HaloTag
Convertir “anclas” proteicas en dianas farmacológicas
Muchos fármacos modernos contra el cáncer actúan fijándose a proteínas dentro de nuestras células. Pero algunas de las proteínas más importantes no ofrecen “asas” fáciles para que los medicamentos se agarren. Este estudio presenta un ingenioso truco químico, inspirado en una herramienta de laboratorio muy utilizada llamada HaloTag, para fijarse a un punto normalmente de difícil acceso en una proteína que ayuda a controlar señales de crecimiento relevantes para el cáncer. El trabajo podría abrir nuevas vías para fármacos que inhiban vías que impulsan tumores de forma más duradera.
Por qué la mayoría de los fármacos covalentes van al mismo sitio
En los últimos años, los llamados fármacos covalentes dirigidos se han convertido en una clase prometedora de medicamentos. Incorporan un grupo químico moderadamente reactivo que forma un enlace permanente con un aminoácido específico de la proteína, fijando el fármaco en su lugar. Casi todos estos fármacos atacan la cisteína, un aminoácido relativamente raro pero muy reactivo. En contraste, otros dos aminoácidos, el aspartato y el glutamato, son mucho más comunes y a menudo cruciales para la forma y función de una proteína, pero sus grupos ácidos de carboxilato son mucho menos reactivos en el ambiente acuoso de la célula. Eso dificulta su modificación selectiva, y solo existían pocos ejemplos exitosos de fármacos covalentes dirigidos a glutamato o aspartato antes de este trabajo.
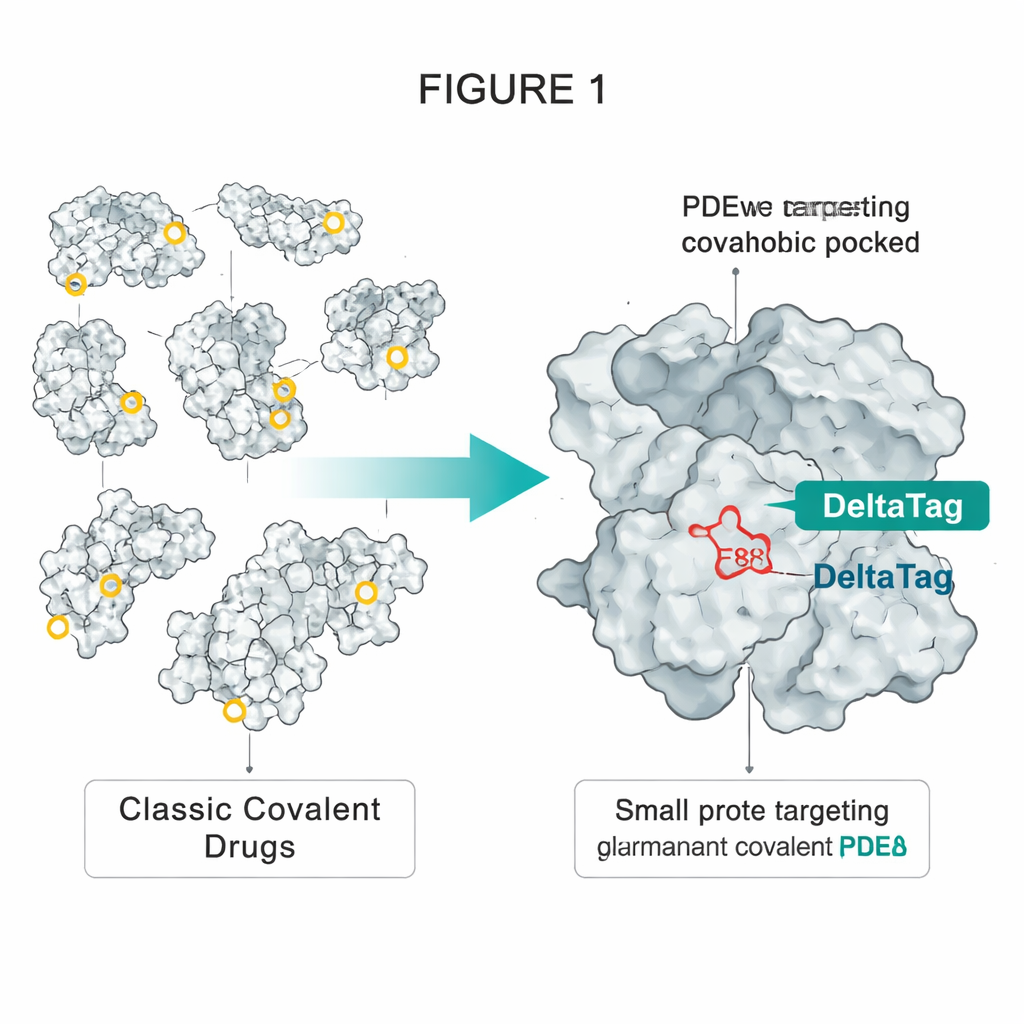
Tomando prestado un truco de la tecnología HaloTag
Los autores se inspiraron en HaloTag, una proteína diseñada de uso extendido que puede etiquetarse de manera permanente con tintes fluorescentes. En HaloTag, un aspartato especialmente colocado en el interior de una cavidad hidrofóbica reacciona con una sencilla cadena de cloroalcano en el tinte, formando un enlace éster estable. El equipo observó que otra proteína, PDEδ, tiene una cavidad hidrofóbica algo similar que contiene un único glutamato accesible, llamado E88. PDEδ transporta proteínas señalizadoras modificadas con lípidos, como la pequeña GTPasa Rheb, por la célula, ayudándolas a alcanzar las membranas donde se activan complejos promotores del crecimiento como mTORC1. Inhibidores no covalentes anteriores de PDEδ podían bloquear este transporte, pero su efecto era limitado porque otra proteína, Arl2, puede desalojarlos de la cavidad con el tiempo.
Diseñando DeltaTag para fijarse al glutamato
Para superar este problema del “desalojo”, los investigadores partieron de un conocido bloqueador de alta afinidad de PDEδ y re‑diseñaron una de sus cadenas laterales para que portara una “cabeza de guerra” haloalcano similar a las usadas en ligandos de HaloTag. Tras varias rondas de ajuste estructural guiadas por estructuras cristalinas de la proteína, llegaron a un compuesto llamado DeltaTag. Su rasgo clave es un grupo fenetil bromuro colocado de forma que, una vez que la molécula se acopla en la cavidad lipídica de PDEδ, el bromuro queda precisamente alineado para reaccionar con E88. Medidas biofísicas y estructuras de rayos X de alta resolución confirmaron que DeltaTag forma un enlace éster covalente específico con este glutamato y que otros aminoácidos potencialmente más reactivos en PDEδ permanecen intactos. El compuesto es lo bastante reactivo para etiquetar eficientemente la proteína, pero lo bastante estable en agua y en presencia del principal antioxidante sulfurosado de la célula, el glutatión, como para evitar daños indiscriminados y generalizados.
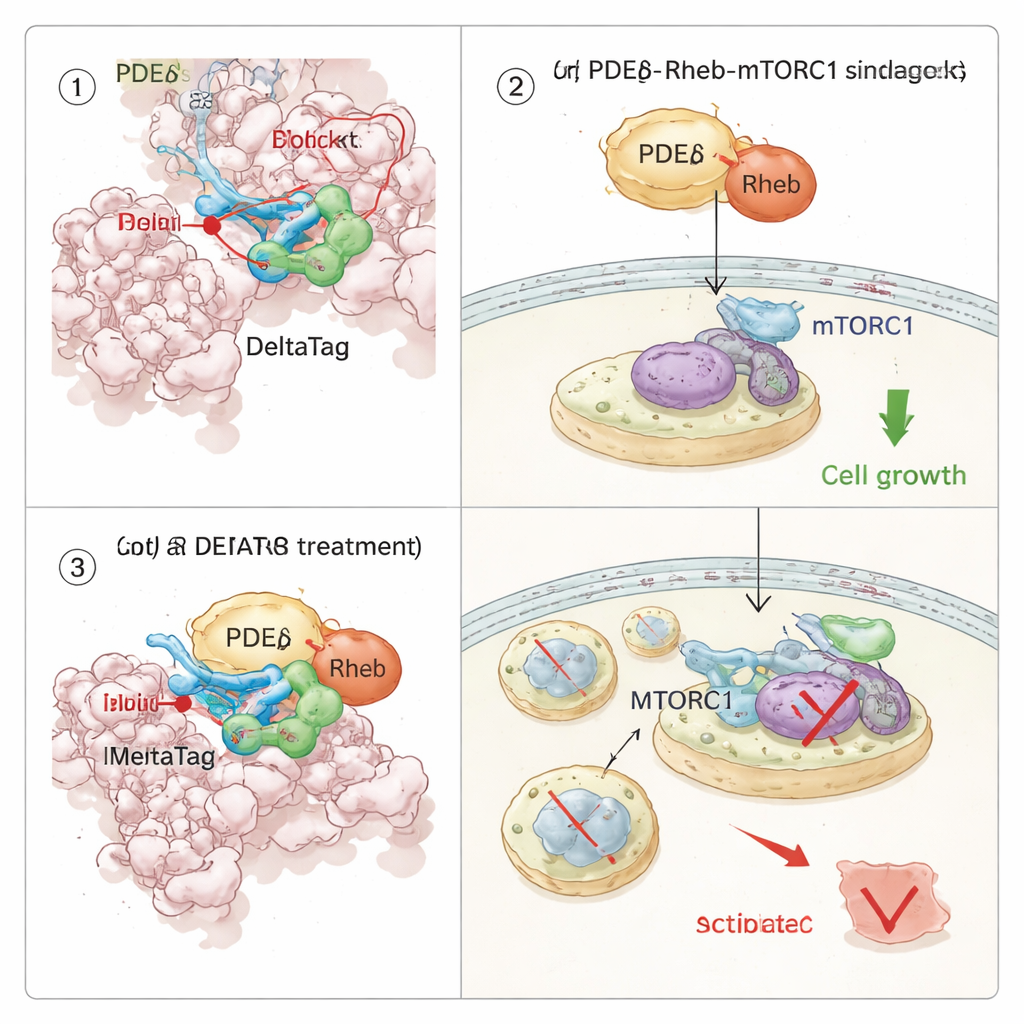
Reconfigurando una vía de crecimiento dentro de células cancerosas
Puesto que PDEδ chaperonea a Rheb, y Rheb a su vez activa la vía de crecimiento mTORC1, el equipo investigó cómo la inhibición covalente de PDEδ reverberaría en la señalización celular. Mediante perfiles de estabilidad térmica a lo largo de miles de proteínas, mostraron que DeltaTag se une selectivamente a PDEδ en extractos celulares y altera proteínas vinculadas al eje Rheb–mTOR. En experimentos de imagen en células vivas, DeltaTag provocó que Rheb se redistribuyera desde un patrón difuso en el interior celular hacia membranas internas más agrupadas, coherente con la interrupción de su transporte normal. La fosfoproteómica global y ensayos de Western dirigidos revelaron que la actividad de mTORC1, seguida por la fosforilación de una proteína ribosomal llamada S6, disminuyó con el tiempo, mientras que aumentaron señales compensatorias en vías relacionadas. Importante: en varias líneas celulares humanas cancerosas impulsadas por KRAS mutante y dependientes de una señalización mTOR fuerte, DeltaTag ralentizó la proliferación celular de forma más eficaz que inhibidores reversibles estrechamente relacionados, y su efecto fue menor en células carentes de PDEδ, lo que apoya que su acción principal es “on‑target”.
Abrir una puerta a nuevos tipos de dianas terapéuticas
Este trabajo demuestra que es posible diseñar pequeñas moléculas que formen un enlace permanente y altamente específico con un único glutamato enterrado en una cavidad lipofílica de una proteína, usando una química de haloalcanos relativamente simple tomada de HaloTag. En el sistema modelo PDEδ, ese enlace covalente produce un bloqueo más duradero de una vía de crecimiento relevante para el cáncer que los fármacos reversibles anteriores. En términos más generales, la misma lógica de diseño podría aplicarse a otras proteínas que tengan cavidades hidrofóbicas pero carezcan de los aminoácidos “reactivos” habituales, siempre que presenten un glutamato o aspartato estratégicamente situado. Con optimización adicional, los inhibidores covalentes dirigidos al glutamato como DeltaTag podrían convertirse en herramientas valiosas para la biología química y, en última instancia, en candidatos para nuevas terapias que aborden proteínas actualmente difíciles de modular farmacológicamente.
Cita: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
Palabras clave: inhibidores covalentes, dirigido al glutamato, PDEδ, señalización mTOR, diseño de fármacos contra el cáncer