Clear Sky Science · es
Ingeniería de células sintéticas con dominios intramembrana que poseen asimetrías bilaterales distintivas
Por qué importan las pequeñas burbujas sintéticas
Cada célula viva está envuelta por una membrana que se comporta como una piel inteligente y flexible. Esta piel no es uniforme: los lados interior y exterior, e incluso distintos parches a lo largo de su superficie, pueden tener composiciones y formas muy diferentes. Esas diferencias ayudan a las células a enviar señales, unir proteínas e incluso dividirse. Sin embargo, ha sido extraordinariamente difícil construir membranas modelo simples y controlables que capturen esta complejidad. Este estudio presenta una forma práctica de fabricar “células sintéticas” del tamaño celular cuyas membranas son asimétricas en ambas caras y están lateralmente segmentadas en regiones distintas, abriendo una vía hacia imitaciones celulares más realistas y al estudio de cómo los patrones de membrana impulsan la gemación y la división. 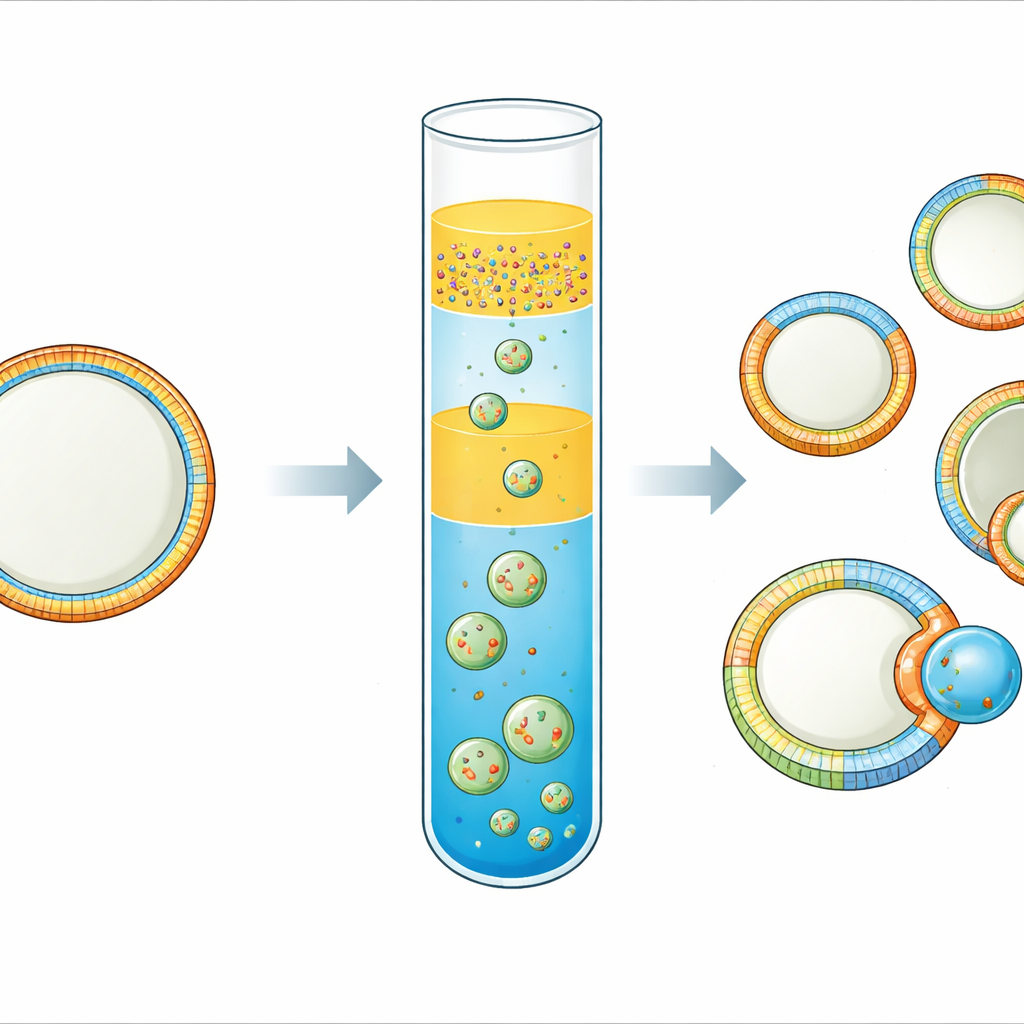
Construyendo mejores imitaciones celulares
Las membranas reales de las células son asimétricas: el lado interno es rico en lípidos cargados negativamente que reclutan proteínas de señalización, mientras que el lado exterior presenta lípidos diferentes que median el reconocimiento célula–célula. Muchos métodos de laboratorio pueden generar vesículas gigantes—esferas huecas de moléculas parecidas a grasas—pero sus dos hojas suelen terminar siendo iguales, y el interior es difícil de acceder. Otros enfoques que sí crean asimetría a menudo requieren dispositivos complejos, lípidos especiales o dejan las vesículas pegadas a una superficie. Los autores se propusieron crear vesículas libres, del tamaño celular, que combinen un alto encapsulamiento de biomoléculas con una asimetría robusta y ajustable, más parecida a la de una célula viva.
Una receta de tres capas para membranas asimétricas
El equipo perfeccionó una técnica de “emulsión invertida”, en la que diminutas gotas de agua recubiertas de lípidos se hacen pasar por una interfaz aceite–agua para formar vesículas. Su innovación clave es una disposición de aceite en tres capas. En el fondo se encuentra un aceite que contiene los lípidos destinados a la monocapa externa de la membrana. Encima de este colocan un aceite espaciador fino que no contiene lípidos, y sobre él una emulsión de gotas acuosas rodeadas por un segundo aceite que transporta los lípidos para la monocapa interna. Durante un breve paso de centrifugación, las gotas atraviesan el espaciador y la capa inferior, incorporando una segunda capa de lípidos y cerrándose en vesículas. Elegir dos aceites de diferente densidad e incluir el espaciador limita drásticamente la mezcla entre las reservas de lípidos, de modo que las monocapas interna y externa conservan composiciones distintas.
Comprobando que los dos lados permanecen diferentes
Para verificar que realmente tenían hojas distintas, los investigadores usaron lecturas químicas y basadas en proteínas. En una serie de pruebas, añadieron un lípido fluorescente solo a una monocapa y luego expusieron las vesículas a un químico en la solución exterior que apaga la fluorescencia pero no puede atravesar la membrana. Cuando el lípido fluorescente estaba en la cara externa, la señal cayó casi por completo; cuando estaba en la cara interna, apenas cambió, lo que demuestra que la mayoría de los lípidos marcados permanecieron donde se pretendía. En un segundo conjunto de experimentos, colocaron lípidos que unen proteínas específicas—como lípidos marcados con biotina para estreptavidina o grupos de cabeza especiales para proteína fluorescente verde con etiqueta His—en una sola monocapa. Las proteínas añadidas al compartimento opuesto (dentro o fuera) se unieron únicamente cuando su lípido emparejado estaba en el mismo lado de la membrana, confirmando tanto una fuerte asimetría como la preservación de la función proteica.
Creación de balsas y observación de la gemación de membranas
Las membranas celulares reales también contienen “balsas”: pequeños parches enriquecidos en ciertos lípidos como colesterol y esfingomielina, que pueden agrupar proteínas e influir en la forma. Lograr tal separación de fases con el método de emulsión invertida había sido difícil porque el colesterol tendía a permanecer disuelto en el aceite en lugar de incorporarse a la membrana. Al usar escualeno en la capa de aceite inferior, que retiene el colesterol menos fuertemente que el aceite mineral estándar, los autores pudieron formar de manera reproducible vesículas cuyas membranas se dividían en regiones coexistentes ordenadas y desordenadas en fase líquida, muy parecidas a las balsas. Luego combinaron este patrón lateral con la asimetría de las monocapas: un dominio llevaba un ligando en la hoja interna que unía estreptavidina en el interior, mientras que otro dominio llevaba glicolípidos que unían la toxina del cólera en el exterior. 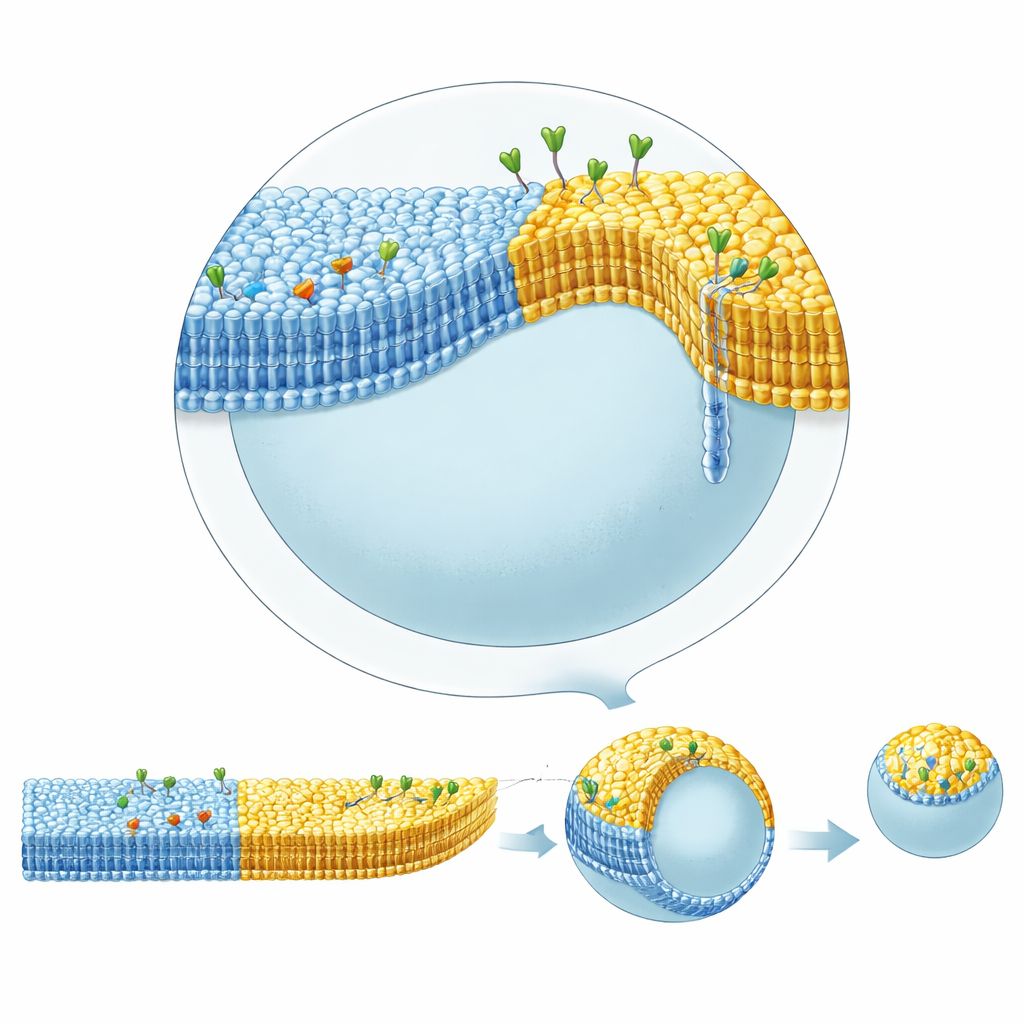
Cómo las proteínas y los patrones impulsan los cambios de forma
Estas vesículas complejas mostraron dinámicas de forma llamativas. Cuando la toxina del cólera se unió a los glicolípidos en el dominio ordenado del lado externo, ese dominio se abultó hacia afuera formando una protuberancia curva conectada por un cuello estrecho, y bajo una ligera desinflación osmótica pudo separarse por completo como una vesícula hija. Esta gemación no requirió moléculas portadoras de energía como el ATP ni maquinaria de división especializada; surgió puramente de la interacción entre la composición lipídica, los límites de dominio y la unión asimétrica de proteínas. Al aumentar la cantidad de estreptavidina unida en la cara interna del dominio desordenado, el equipo pudo contrarrestar la curvatura hacia afuera del dominio ordenado y restaurar gradualmente una forma más esférica. El análisis geométrico detallado de los contornos de las vesículas mostró que la curvatura de la membrana salta en la frontera entre dominios, y que los cuellos estrechos que se cierran durante la gemación deben soportar fuerzas de al menos decenas de piconewtons—cuantificando cómo la estructura de los dominios y el hacinamiento proteico pueden esculpir mecánicamente las membranas.
Qué significa esto para las futuras células sintéticas
En términos cotidianos, los autores han desarrollado una receta para fabricar burbujas blandas del tamaño celular cuyas pieles están pautadas y tienen dos caras de manera muy parecida a las membranas celulares reales. Debido a que el método es relativamente simple, funciona con muchos lípidos diferentes y permite atrapar proteínas y otras moléculas grandes en el interior, allana el camino para construir células artificiales más verosímiles desde cero. Tales células sintéticas podrían ayudar a los científicos a desentrañar cómo los patrones de membrana controlan la señalización, el tráfico y la división, y podrían eventualmente utilizarse como vectores inteligentes de fármacos que cambian de forma o se parten a demanda dentro del cuerpo.
Cita: Yandrapalli, N., Seemann, T., Lipowsky, R. et al. Engineering synthetic cells with intramembrane domains possessing distinct bilayer asymmetries. Nat Commun 17, 2620 (2026). https://doi.org/10.1038/s41467-026-68997-x
Palabras clave: células sintéticas, membranas lipídicas, asimetría de membrana, separación de fases, gemación de membrana