Clear Sky Science · es
Plataforma de nanodiscos de glicoproteínas virales para análisis de vacunas
Convertir las proteínas virales en blancos medibles
Las vacunas modernas dependen cada vez más de versiones cuidadosamente diseñadas de las proteínas que recubren la superficie de los virus. Estas proteínas son los principales objetivos de los anticuerpos protectores, pero son notoriamente difíciles de estudiar en su forma natural unida a la membrana. Este artículo describe una nueva plataforma de laboratorio que incorpora proteínas de superficie virales de longitud completa en pequeñas partículas lipídicas planas llamadas nanodiscos. Este sistema permite a los científicos medir hasta qué punto los candidatos vacunales imitan a los virus reales, cómo se unen a ellos los anticuerpos y cómo rediseñar estas vacunas para mejorar la protección.
Por qué importa recrear la superficie viral
Muchas de las proteínas virales más importantes están ancladas en una membrana grasa, tal como ocurre en un virus real. Los enfoques tradicionales de laboratorio recortan la porción de membrana para facilitar la producción y purificación de las proteínas en solución. Pero ese atajo elimina regiones cercanas a la membrana que alojan dianas de anticuerpos especialmente valiosas, incluido un segmento del VIH conocido como región externa próxima a la membrana (MPER). Estas regiones próximas a la membrana pueden verse y comportarse de forma diferente cuando no están insertas en un entorno lipídico realista, lo que significa que los fragmentos proteicos solubles pueden ofrecer una imagen incompleta o engañosa de cómo rendirá una vacuna en el organismo.
Construcción de una plataforma de nanodiscos versátil
Los investigadores desarrollaron un flujo de trabajo optimizado de cinco días para obtener proteínas de superficie virales de longitud completa de células humanas, conservar sus segmentos transmembrana naturales intactos e insertarlas en un disco lipídico controlado. Primero expresaron glicoproteínas modificadas de VIH y Ébola en la superficie celular, luego las extrajeron suavemente con detergente y las capturaron en una matriz de purificación. Mientras las proteínas aún estaban unidas, añadieron lípidos definidos y una proteína andamio en forma de cinturón que se autoensambla en una pequeña membrana con forma de disco. Al retirar el detergente, las proteínas virales se acomodaron en estos nanodiscos. Las preparaciones resultantes eran de alta pureza, estables durante meses en refrigeración y presentaban recubrimientos de glicanos (azúcares) muy similares a los que tienen las espículas virales nativas. 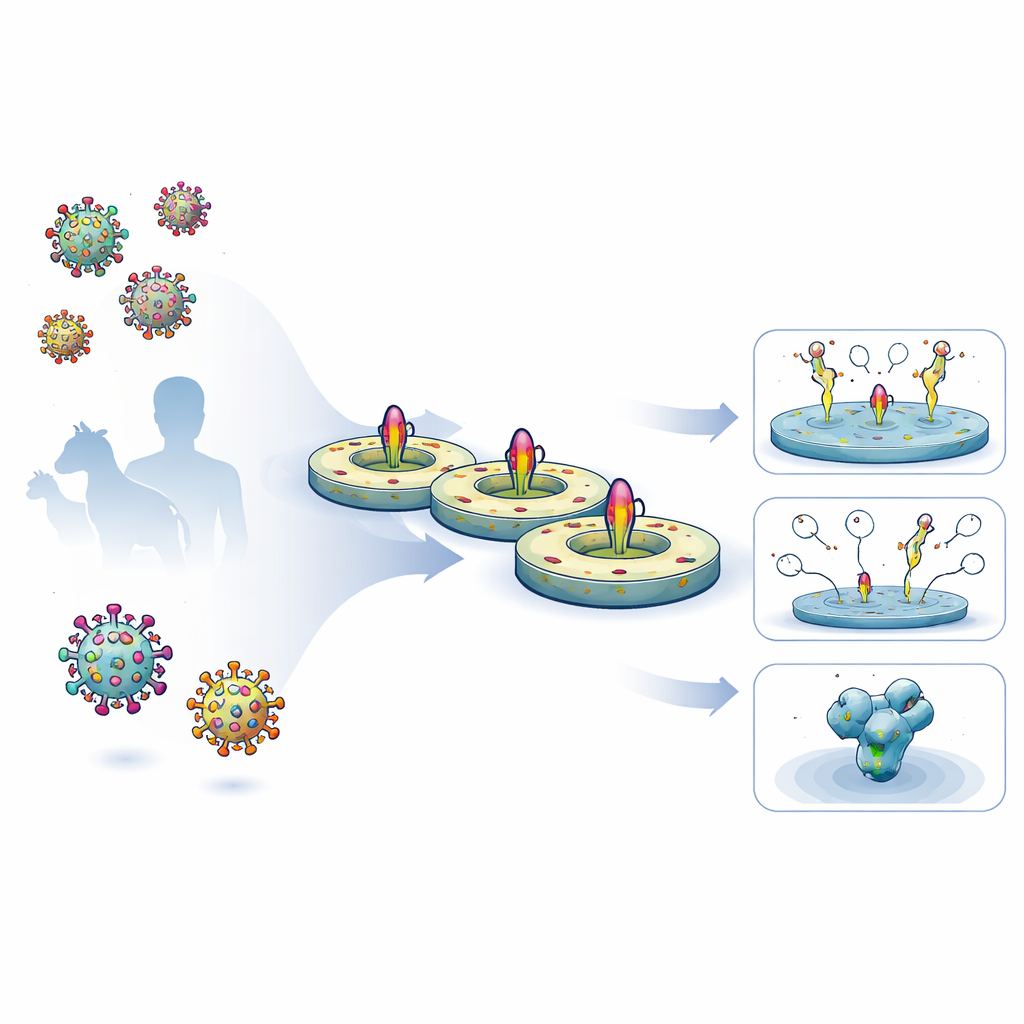
Leer la unión de anticuerpos y las respuestas inmunitarias
Con proteínas incrustadas en nanodiscos, el equipo evaluó qué tan bien distintos anticuerpos podían unirse utilizando varios montajes de resonancia de plasmones de superficie (SPR), una técnica que sigue la unión en tiempo real. Usando nanodiscos de VIH diseñados para exponer la región MPER, mostraron que un potente anticuerpo ampliamente neutralizante llamado 10E8 se unía aproximadamente 70 veces con más afinidad al constructo diseñado que a un diseño anterior, principalmente porque se disociaba mucho más lentamente. Mutaciones de control que alteraron la región MPER eliminaron por completo la unión de 10E8, confirmando que la plataforma puede informar con sensibilidad cómo los cambios de diseño afectan epítopos clave. Los mismos nanodiscos sirvieron como sondas en citometría de flujo, donde ayudaron a capturar células B de ratones y monos inmunizados que reconocían la forma transmembrana completa de la proteína del VIH, incluidas partes ausentes en sondas solubles estándar. 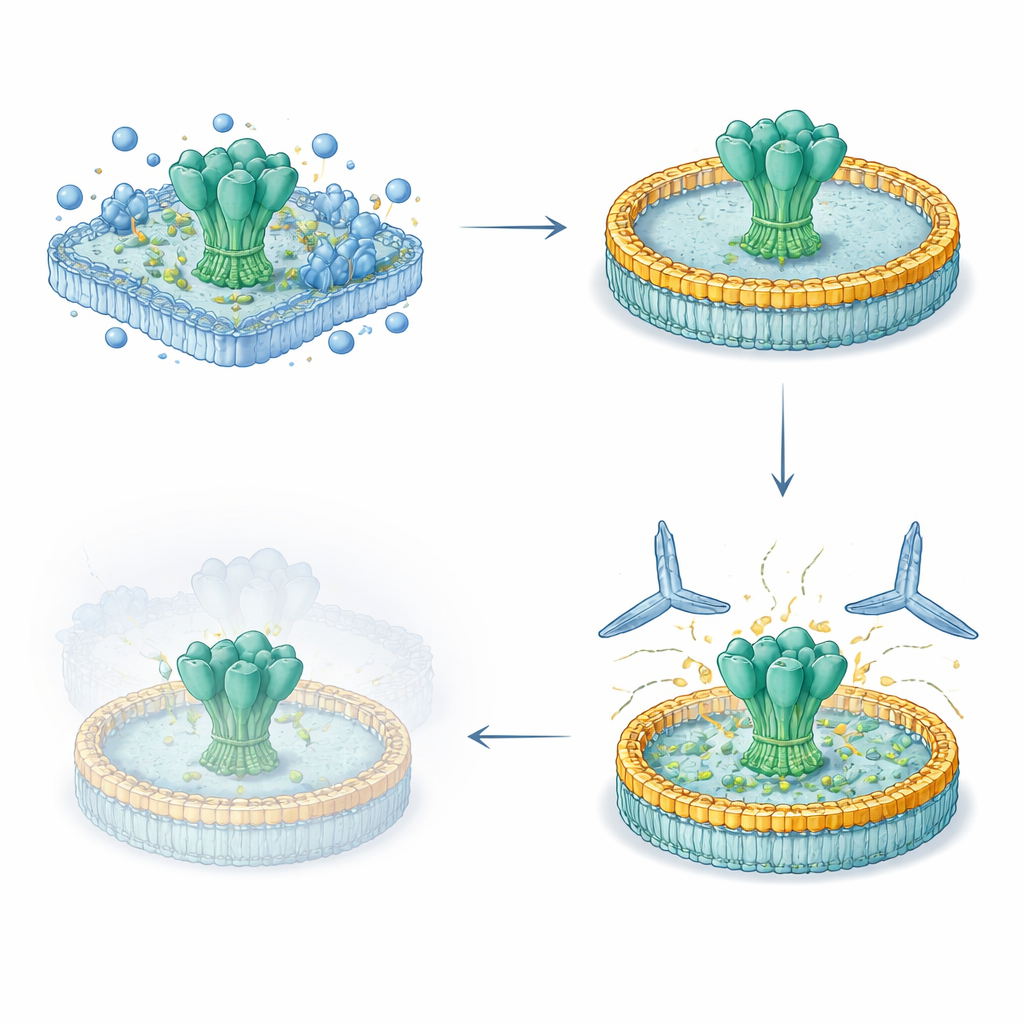
Ver el blanco completo en detalle atómico
Para entender exactamente cómo los anticuerpos reconocen la MPER en su entorno nativo, los autores emplearon microscopía electrónica criogénica para obtener imágenes de los nanodiscos de VIH unidos a tres anticuerpos ampliamente neutralizantes diferentes. Obtuvieron una estructura a 3,5 angstroms de un anticuerpo, 10E8, interactuando con el segmento MPER mientras el resto de la espícula del VIH permanecía anclado en el disco lipídico. Esto reveló una red continua de contactos entre 10E8 tanto con la MPER como con porciones cercanas de la proteína externa, incluida una cavidad profunda en la unión entre dos subunidades. Al comparar esta estructura con imágenes previas de 10E8 unido únicamente a un péptido corto, el equipo mostró que el entorno de membrana y la espícula de longitud completa permiten contactos y movimientos dinámicos adicionales que eran invisibles en modelos más simples, y que aminoácidos específicos del virus influyen fuertemente en la facilidad con que 10E8 puede neutralizarlo.
Usos amplios para vacunas más inteligentes
En términos prácticos, esta plataforma de nanodiscos ofrece a los diseñadores de vacunas una forma de evaluar candidatos vacunales transmembrana con las mismas herramientas analíticas potentes que durante mucho tiempo se reservaron para fragmentos proteicos solubles. Funciona con distintos virus, permite mediciones detalladas de unión, posibilita el aislamiento y la secuenciación precisos de células B inducidas por la vacuna y produce estructuras de alta resolución que capturan epítopos realistas próximos a la membrana. Para un lector no especializado, la conclusión es que los científicos disponen ahora de un banco de pruebas más fiel para proteínas de superficie viral, que puede mostrar qué diseños de vacuna realmente se parecen y se comportan como el virus real y cómo ajustarlos para generar respuestas de anticuerpos más fuertes y amplias. Esto debería acelerar el desarrollo de vacunas de nueva generación no solo para el VIH, sino para muchos otros virus envueltos.
Cita: Rantalainen, K., Liguori, A., Ozorowski, G. et al. Virus glycoprotein nanodisc platform for vaccine analytics. Nat Commun 17, 2561 (2026). https://doi.org/10.1038/s41467-026-68985-1
Palabras clave: nanodiscos, vacunas contra el VIH, glicoproteínas virales, anticuerpos ampliamente neutralizantes, crio-ME