Clear Sky Science · es
Footprinting de radicales en sangre completa de mamífero
Ver las proteínas en acción en sangre real
Las proteínas en nuestra sangre cambian constantemente de forma mientras realizan funciones vitales como combatir infecciones, transportar hierro y responder a la enfermedad. Hasta ahora, la mayoría de las herramientas para examinar esos pequeños cambios de forma solo funcionaban en muestras simplificadas de laboratorio o en células aisladas. Este estudio demuestra, por primera vez, que los científicos pueden leer las conformaciones proteicas directamente en sangre mamífera intacta, abriendo la puerta a observar los procesos de la enfermedad tal como ocurren en el cuerpo.
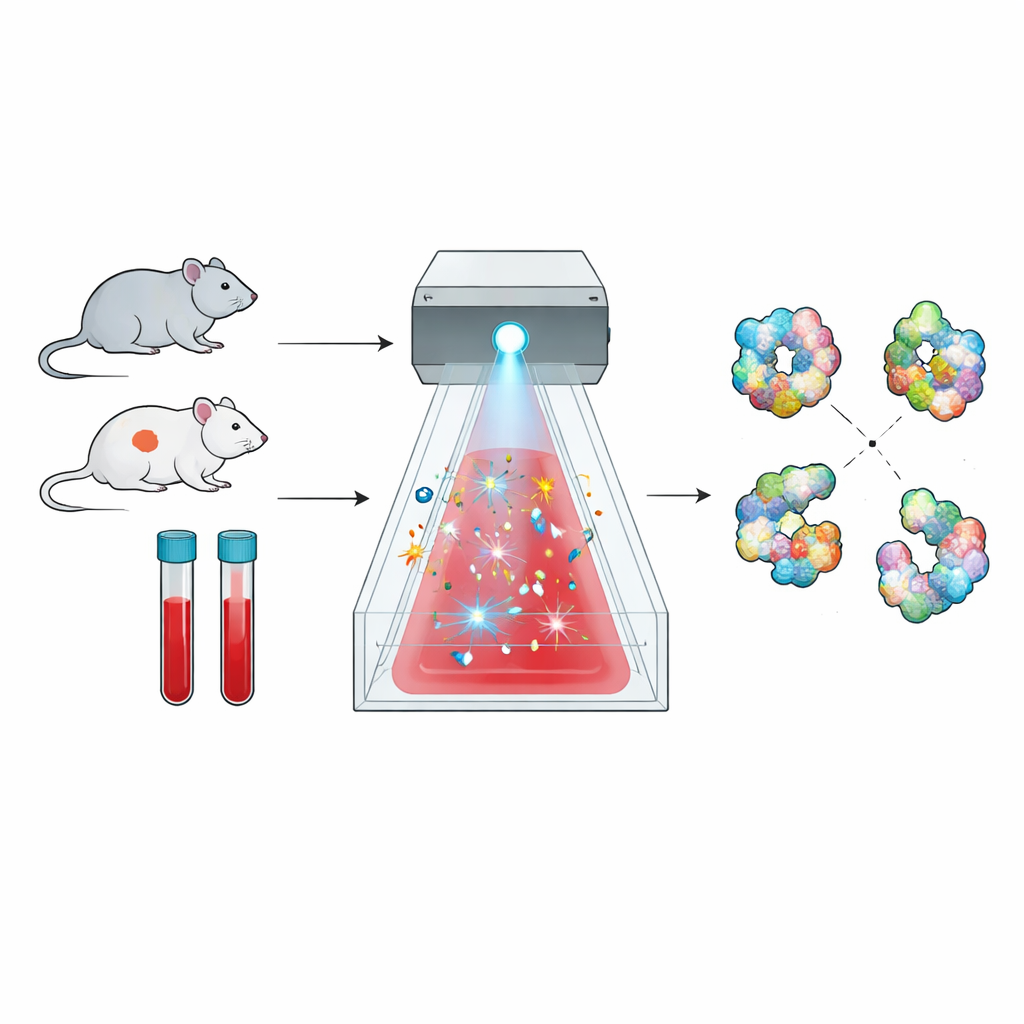
Una nueva manera de mapear las formas de las proteínas
Las proteínas no son perlas rígidas; se pliegan en formas tridimensionales complejas y esas formas determinan lo que pueden hacer. El método explorado aquí, llamado footprinting de proteínas por radicales, aprovecha este hecho. Ráfagas breves de moléculas altamente reactivas actúan como un “destello fotográfico” químico, golpeando solo las partes de una proteína que están expuestas al líquido que la rodea. Después, la espectrometría de masas se utiliza para contar dónde se produjeron esos impactos químicos, produciendo una especie de mapa de superficie, o huella, de la conformación de cada proteína. Los cambios en esa huella entre estados sanos y enfermos revelan desplazamientos sutiles en cómo está plegada la proteína o en cómo interactúa con otras moléculas.
Hacer que la técnica funcione en sangre completa
Aplicar este enfoque directamente a la sangre ha sido un desafío de larga data. La sangre absorbe fuertemente la luz ultravioleta y está llena de enzimas, como la catalasa, que destruyen rápidamente los químicos habituales generadores de radicales antes de que puedan marcar las proteínas. Los investigadores resolvieron esto cambiando a persulfato de sodio, que puede dividirse mediante un destello brillante de luz de banda ancha en potentes radicales sulfato. Usando un sistema comercial llamado FOX, demostraron que el persulfato puede activarse de manera fiable y que una lectura de dosimetría incorporada puede seguir cuántos radicales se producen, permitiendo un control cuidadoso de la “exposición” que recibe cada muestra.
Proteger las células mientras se captura detalle
Dado que este método está pensado para estudiar proteínas en algo cercano a su estado natural, era crucial que las propias células sanguíneas no quedaran destruidas. Pruebas en sangre de ratón mostraron que añadir persulfato concentrado causaba solo cambios menores y reversibles en la forma de los glóbulos rojos y menos del dos por ciento de rotura celular, similar a soluciones salinas sencillas. El equipo también desarrolló una mezcla de “apagado” mejorada que absorbe rápidamente las especies reactivas sobrantes, evitando daños espurios por reacciones secundarias más lentas después del destello. En conjunto, estas mejoras les permitieron marcar proteínas en sangre de ratón intacta preservando la estructura celular y manteniendo el ruido de fondo muy bajo.
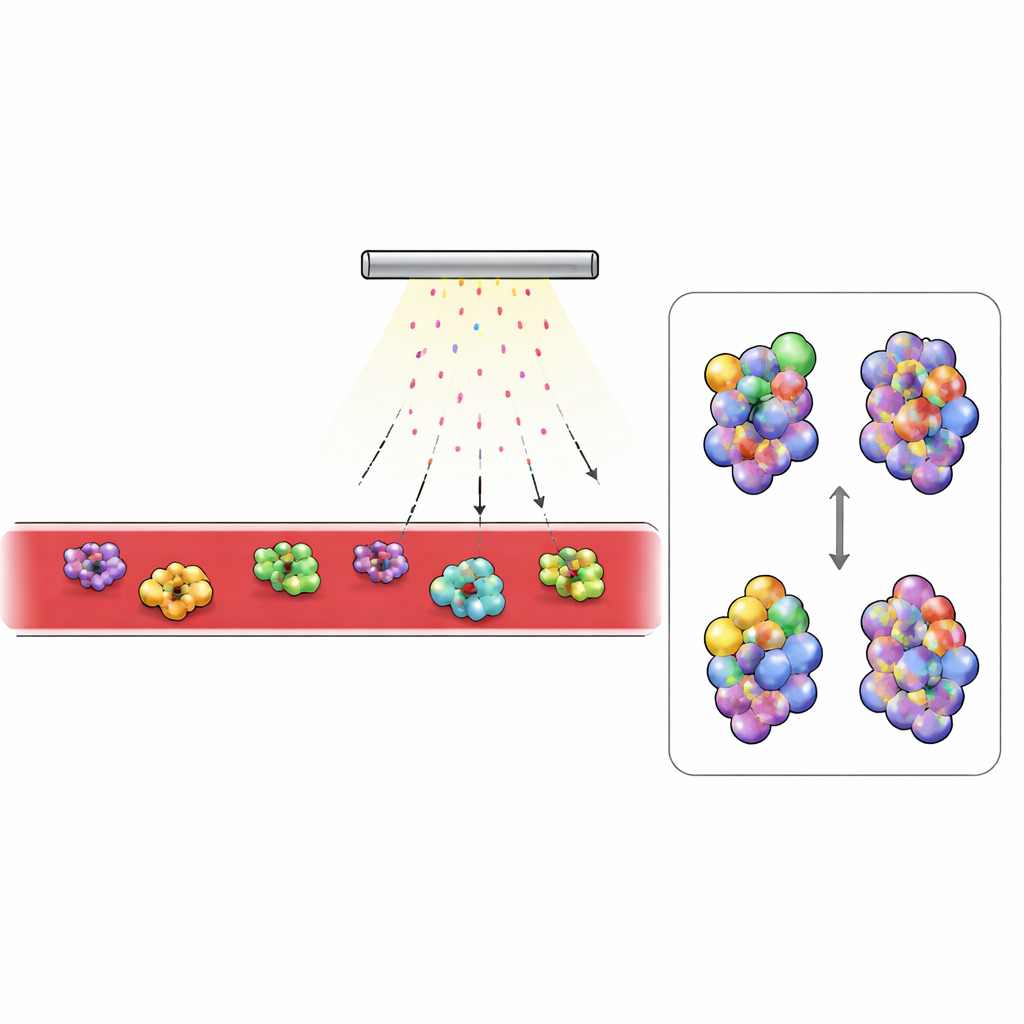
Qué cambia en la sangre diabética
Con esta plataforma en mano, los investigadores compararon sangre de ratones sanos y de un modelo común de diabetes tipo 2. Se centraron en las proteínas más abundantes detectadas, especialmente aquellas que circulan fuera de las células. Las proteínas extracelulares mostraron un marcado etiquetado en comparación con las intracelulares, lo que refleja una penetración limitada del persulfato en los interiores celulares. Dos proteínas sanguíneas destacaron: el complemento C3, un componente clave del sistema inmune, y la transferrina, que transporta hierro. En ratones diabéticos, las regiones de C3 que quedan enterradas cuando la proteína cambia a su forma activa mostraron menos etiquetado, mientras que regiones normalmente ocultas estaban más expuestas. Este patrón coincidió con el cambio estructural conocido cuando C3 se convierte en su fragmento activo, C3b, y pruebas sanguíneas confirmaron que los animales diabéticos tenían mucha más C3 activada. En la transferrina, las áreas cercanas al sitio de unión del hierro estaban más protegidas en la sangre diabética, coherente con que la proteína transportara más hierro. Mediciones independientes mostraron un mayor hierro sérico y una fracción mayor de transferrina saturada con hierro en ratones diabéticos.
Por qué esto importa para la salud y la medicina
Para un público no especializado, el mensaje esencial es que los autores han creado una forma de “tocar” las conformaciones de muchas proteínas a la vez directamente en sangre real y luego usar esos patrones de forma para inferir cómo la enfermedad está alterando la química del organismo. En este modelo murino de diabetes tipo 2, el método revela una señalización del complemento hiperactiva y una mayor carga de hierro en la transferrina—cambios que las pruebas clásicas podrían pasar por alto o detectar solo de forma indirecta. Dado que el enfoque funciona con pequeñas muestras de sangre y usa una fuente de luz estandarizada, podría eventualmente ayudar a identificar señales estructurales tempranas de enfermedad, rastrear cómo se comportan los fármacos biológicos en el torrente sanguíneo y orientar el diseño de tratamientos más efectivos.
Cita: Zhao, M., Tobin, L., Misra, S.K. et al. Radical footprinting in mammalian whole blood. Nat Commun 17, 2470 (2026). https://doi.org/10.1038/s41467-026-68982-4
Palabras clave: proteómica estructural, proteínas sanguíneas, diabetes tipo 2, sistema del complemento, metabolismo del hierro