Clear Sky Science · es
Variaciones en el extremo C de las proteínas afectan la proteostasis
Cómo el extremo final de las proteínas moldea la salud
Cada proteína en nuestras células termina con una pequeña “cola” de apenas unos cuantos bloques constructores. Estas colas pueden parecer un apéndice, pero este estudio demuestra que silenciosamente deciden qué proteínas perduran y cuáles se eliminan con rapidez. Dado que los niveles de proteínas subyacen en el cáncer, los trastornos genéticos y en cómo las células responden al estrés, comprender estas colas ofrece nuevas vías para interpretar el riesgo de enfermedad e incluso diseñar tratamientos futuros.
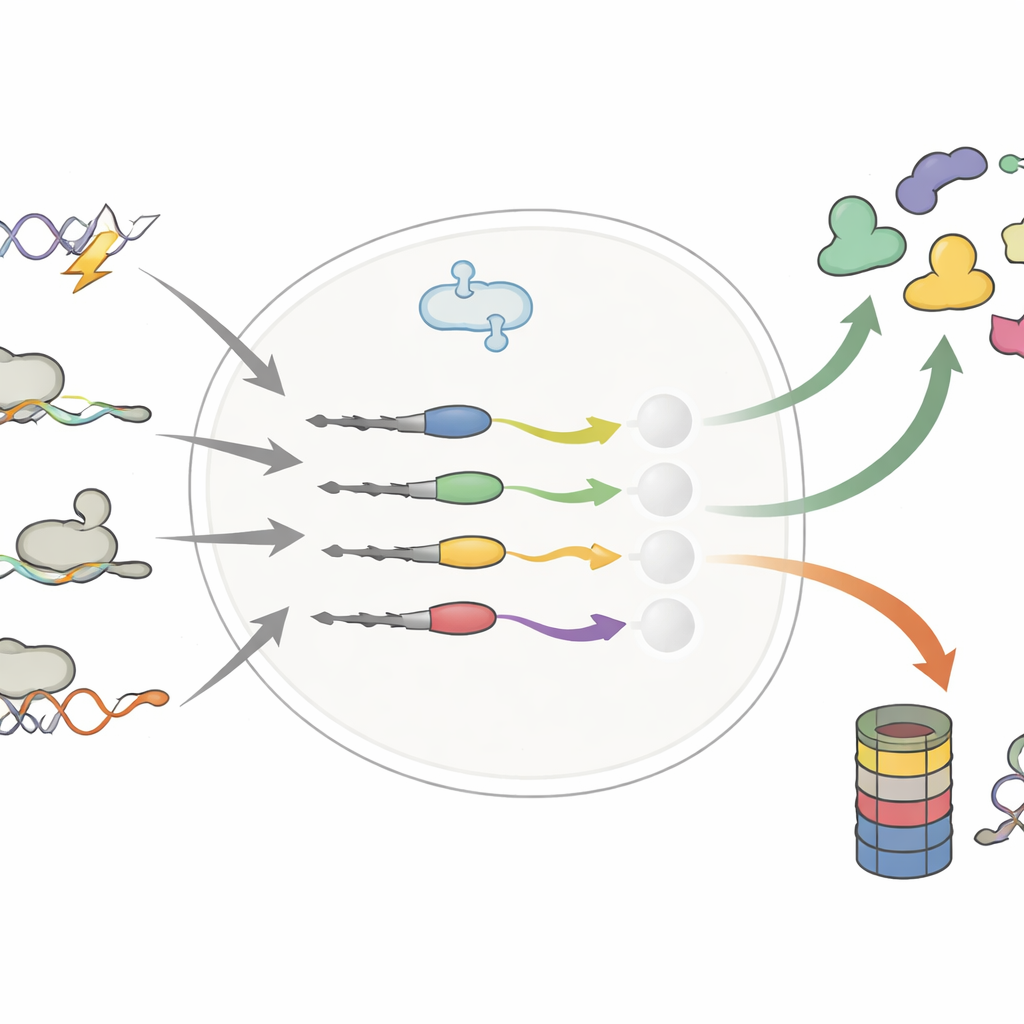
Pequeños cambios en la cola de la proteína, grandes variaciones en su vida útil
Los autores se centraron en el extremo distal de las proteínas—el C-terminal—donde incluso unos pocos bloques adicionales o sustituidos pueden aparecer por mutaciones del ADN, empalme alternativo del ARN o por ribosomas que leen más allá de la señal normal de paro. Trabajos previos sugerían que esas colas “erróneas” actuaban principalmente como etiquetas de desecho, enviando proteínas defectuosas a la trituradora celular. Al comparar sistemáticamente miles de colas normales y alteradas, este estudio derriba esa visión simplista. El equipo muestra que las colas alteradas pueden acortar o alargar la vida de una proteína, a veces estabilizando oncogenes o desestabilizando supresores tumorales.
Cuando los errores genéticos ayudan o perjudican a las proteínas
Una fuente importante de cambios en las colas son las mutaciones nonstop, que borran la señal de paro normal para que el ribosoma continúe en un tramo de ARN que normalmente permanece en silencio. Los investigadores probaron más de 3.000 variantes nonstop vinculadas a enfermedades usando un reportero bicolor que mide cuánto protege o debilita cada cola una proteína modelo. En promedio, las colas mutantes seguían haciendo las proteínas menos estables que sus contrapartes normales, pero una fracción considerable produjo el efecto contrario: aproximadamente una de cada diez mutaciones nonstop estabilizó proteínas, mientras que casi un tercio las desestabilizó. Estos cambios afectaron oncogenes y supresores tumorales conocidos, lo que implica que mutaciones que parecían sutiles pueden, de hecho, inclinar el equilibrio entre el crecimiento y la muerte celular.
Variedad incorporada por empalme y lectura más allá del paro
No todas las diferencias de cola son accidentes. Nuestros genes suelen producir múltiples versiones proteicas mediante empalme alternativo y lectura programada de codones de paro. Al explorar catálogos de genes humanos, los autores encontraron que casi dos tercios de los genes generan proteínas con más de un diseño de cola, y muchas difieren solo en los últimos pocos bloques constructores. Probar ejemplos seleccionados mostró que estas versiones casi idénticas a menudo tienen vidas medias claramente distintas. Algunas colas generadas por readthrough aumentaron la estabilidad de las proteínas, otras la disminuyeron. Esto sugiere que las células usan deliberadamente la variación en las colas como un mando de ajuste fino, regulando cuánto tiempo persisten formas proteicas específicas en distintos tejidos o condiciones.
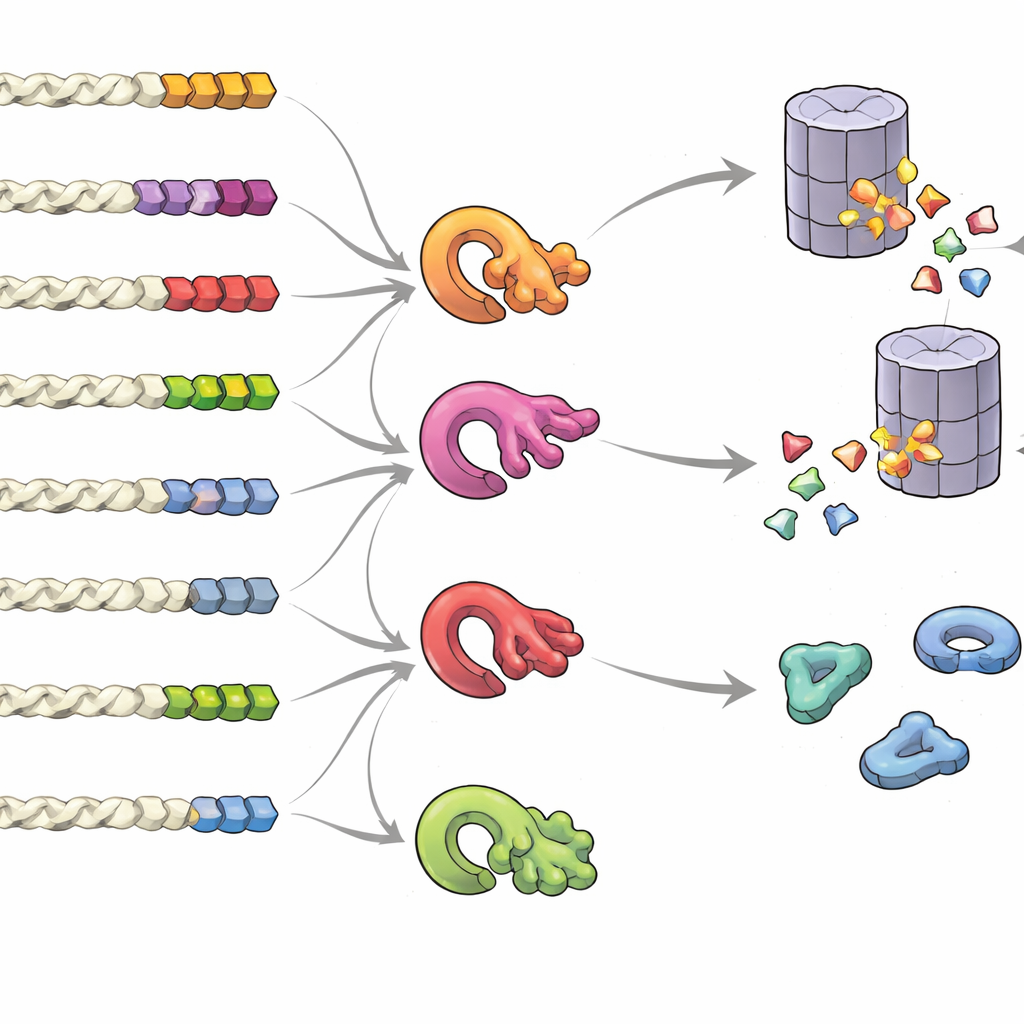
Qué convierte una cola en una señal de “consérvame” o “échame”
Para comprender qué rasgos de una cola inclinan el destino proteico, el equipo creó bibliotecas de colas aleatorias y midió su impacto en conjunto. Encontraron que no existe un único “motivo” fijo, sino que importan la composición global, la posición y la agrupación de ciertos bloques constructores. Las colas ricas en residuos pequeños o apolares, o en los menos comunes cisteína y triptófano, tendían a invitar a la degradación, especialmente cuando estos residuos se agrupaban. En contraste, las colas enriquecidas en residuos ácidos favorecían la estabilidad. Al comparar muchas especies, las colas proteicas normales mostraron señales claras de presión evolutiva para evitar patrones de riesgo, mientras que las colas resultantes de readthrough o de cambios de marco propensas al error tendían a composiciones desestabilizadoras. El grupo también descubrió que múltiples enzimas de control de calidad—diferentes ligasas de ubiquitina—se especializan en reconocer distintos patrones hidrofóbicos en las colas, formando una red intrincada que decide qué proteínas se destruyen.
Por qué esto importa para la medicina y la biotecnología
El trabajo redefine las colas proteicas de meros remates pasivos a reguladores activos de la abundancia proteica. Para un público general, esto significa que muchas enfermedades pueden surgir no solo por proteínas defectuosas, sino también por cambios sutiles en cuánto duran las proteínas, impulsados por pequeñas diferencias en sus extremos. También advierte que las terapias que promueven deliberadamente la lectura más allá de las señales de paro, usadas para tratar ciertos trastornos genéticos, podrían alterar inadvertidamente las vidas de muchas proteínas normales. Al mismo tiempo, los hallazgos sugieren estrategias nuevas y potentes: mediante el diseño de secuencias de cola o favoreciendo en las células formas de empalme o eventos de readthrough particulares, los científicos podrían algún día ajustar los niveles proteicos hacia arriba o hacia abajo con notable precisión.
Cita: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
Palabras clave: estabilidad proteica, cola C-terminal, degradación de proteínas, mutaciones genéticas, proteostasis